摘要
為使我國結核病治療不落人後,衛生署疾病管制局自2007年起迄今,投入大量人力物力推動多重抗藥性結核計畫(以下簡稱MDR計畫),期望能達成結核病十年減半的使命。目前MDR計畫共發放九種抗結核藥物,筆者以藥學雜誌24卷第三期「淺談我國MDR抗結核計畫」一文,簡明淺白介紹藥物相關資訊。而疾管局於2009年初以專案方式引進四種藥物供MDR計畫使用,增加藥物品項以利結核病治療所需的多重投藥法。
此四種藥物分別為PAS granule 4 gm/pack、Capreomycin 1 g/vial、Terizidone 250 mg/cap、Clofazimine 100 mg/cap,為詳盡完整介紹MDR計畫,故撰此文接續簡介,以期在結核病防治上貢獻綿薄心力。
關鍵字:
多重抗藥性結核、結核病、抗結核第二線藥物
壹、前言
結核病的歷史漫長悠久,不分國籍種族橫跨全世界,加上治療過程需要長時間持續就診追蹤,使得結核病總是給人難以根治的印象。往往醫療行為不當或人為因素的不配合,造成結核菌株逐漸出現抗藥性,也就是所謂多重抗藥性結核(multidrug-resistant tuberculosis,簡稱MDR-TB),疾病管制局於2007年開始MDR抗結核計畫,旨在藉由管理抗結核第二線藥物之發放,有效控制MDR-TB疫情,為MDR-TB個案開創新契機,也使我國結核病防治得以與國際接軌。
貳、MDR抗結核計畫現況
目前MDR抗結核計畫使用的藥物共九種(表一),詳情可見藥學雜誌24卷第三期之「淺談我國MDR抗結核計畫」,而今MDR抗結核計畫以專案進口四種二線藥物,為求完整介紹,僅以本文作為續談。
表一 目前MDR抗結核計畫所使用的九種藥物7
藥品名稱 |
每日劑量(最大用量) |
常見副作用 |
Prothionamide 250 mg ( Tubax 250 mg/tab ) |
15~20 mg/kg (1 gm) |
胃腸不適、肝功能障礙 |
para-aminosalicylic acid 500 mg ( PAS 500 mg/tab ) |
150 mg/kg (12 gm) |
胃腸不適、肝毒性、 過敏性皮膚炎、關節痛 |
Levofloxacin 500 mg ( Vorotal 500 mg/tab ) |
500 mg ~ 1,000 mg |
胃腸不適、全身倦怠、過敏性反應、皮膚搔癢、光敏感性、心律不整 |
Moxifloxacin 400 mg ( Avelox 400 mg/tab ) |
400 mg |
過敏性反應、皮膚搔癢、光敏感性、心律不整、頭痛頭暈、胃腸不適 |
Cycloserin 250 mg ( Cyclocin 250 mg/cap ) |
10~15 mg/kg (1 gm) |
中樞神經系統毒性,精神病患者忌用。另有皮疹、發熱、白血球減少 |
Kanamycin 1 g/vial |
15 mg/kg (1 gm) |
腎毒性、聽毒性、注射部位出現吸收不全或疼痛、結節 |
Streptomycin 1 g/vial |
15 mg/kg (1 gm) |
腎毒性、聽毒性 |
Amikacin 250 mg/vial |
15 mg/kg (1 gm) |
聽毒性、注射部位出現吸收不全或疼痛、結節 |
Rifabutin 150 mg ( Mycobutin 150 mg/cap ) |
5 mg/kg (300 mg) |
胃腸不適、肝毒性、白血球降低 |
MDR抗結核計畫始於2007年5月,由衛生署疾病管制局(以下簡稱疾管局)統籌五大照護團隊,培訓MDR關懷員追蹤結核病患就醫及服藥情形,以瞻前顧後之原則控管發放抗結核第二線藥物,期許達成結核病十年減半目標。
根據結核病診治指引,治療MDR-TB需多重組合式投藥,並且依照病患體重評估用藥品項與劑量增減1。在保障病人安全與治療成果的前提下,疾管局經過多次委員會議審慎討論後,決定以專案方式進口四種抗結核藥物,增加可使用之藥物品項,並於2009年正式增修抗結核免費藥物申請單之藥物品項。
參、MDR專案新藥申請須知
專案新藥的申請流程與過去九種免費二線藥的申請並無差異,但非所有MDR團隊病患都能申請此類專案藥物,因此團隊申請時須留意以下幾點:(1)四種專案新藥僅供MDR團隊使用,非團隊醫院不得提出用藥申請。(2)申請專案新藥時必須確認病患診斷為MDR-TB,且入MDR專案內管理追蹤,方可提出專案新藥申請。(3)申請專案新藥之病人需同時具備MDR-TB且受MDR專案管理的雙重條件,缺一不可。(4)醫師開立專案新藥時須徵求病患同意,請病患簽署專案新藥專屬之病患用藥同意書。(5)進入審核流程時,得連同2009年新版二線藥物申請單與其他審核須檢附的相關資料,以及病患簽署之用藥同意書,一併傳真給團隊審核醫師。(6)需低溫冷藏之藥物,申請醫院使用時請注意儲藏及運送方式,避免溫度變化導致藥品變質。
肆、MDR專案新藥簡介
專案新藥共計四種,分別為PAS granule 4 gm/pack、Capreomycin 1 g/vial、Terizidone 250 mg/cap、Clofazimine 100 mg/cap (表二、圖一),以下分別做簡單的藥物介紹2-7。
表二 專案藥物
藥品名稱 |
每日劑量(最大用量) |
常見副作用 |
PAS granule 4 gm ( Paser 4 gm/pack ) |
150 mg/kg (12 gm) |
胃腸不適、肝毒性、 過敏性皮膚炎、關節痛 |
Capreomycin 1 g (Capastat sulfate 1 g/vial) |
兒童15~30 mg/kg 成人1 gm |
腎毒性、聽神經毒性、前庭神經毒性、暈眩、頭暈、聽力減退 |
Terizidone 250 mg ( Terizidon 250 mg/cap ) |
750 mg ~ 1,000 mg |
胃腸不適、頭痛、暈眩。偶爾會出現羊癲癇的抽搐以及抑鬱或躁鬱的心理反應。 |
Clofazimine 100 mg ( Lamprène 100 mg/cap ) |
100 mg |
體液變色、視力減弱、乾眼症、皮膚癢、噁心、嘔吐、胃腸不適 |

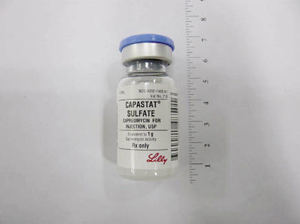
PAS granule (Paser) 4gm/Pack Capreomycin (Capastat sulfate) 1gm/Vial
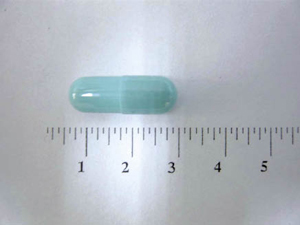

Terizidone (Terizidon) 250mg/Cap Clofazimine (Lamprène) 100mg/Cap
圖一 專案新藥圖片
一、PAS granule 4 gm/pack
商品名Paser,顧名思義為PAS之顆粒劑型,屬抗結核第二線藥物,每包含para-aminosalicylic acid 4 gm,顆粒呈灰白色。
(一)、藥理作用
Paser為顆粒狀劑型,本品須冷藏於15℃以下,藥物顆粒具有耐酸性塗層,在微酸性溶液如蘋果汁、柳橙汁中可緩慢釋放para-aminosalicylic acid,主要是抑制結核菌細胞壁合成來達成抗菌作用,用於治療對para-aminosalicylic acid敏感之各式活動性結核。
Paser多由腎臟排泄,故嚴重腎病變者禁用。由於表面有耐酸性塗層,所以病患偶爾會在糞便中看見消化不完全的空殼顆粒,這是正常情形。
(二)、治療劑量
每日二~三次,每次一包,必須以酸性飲料如蔓越莓汁、柳橙汁、蘋果汁或優格配服。服藥後六小時會達到最大藥物血中濃度,為維持藥物血中濃度,不建議每日一次用藥3。
(三)、副作用
最常見為腸胃道副作用,如腹痛、噁心嘔吐、腹瀉。其他還有發燒、皮膚發疹、白血球降低、血小板減少(皮膚出現紫斑,出血點,牙齦出血)、肝炎、Loeffler's syndrome (嗜酸性紅血球增多、疲倦、發燒、喘、肺部浸潤) 、血管炎等。
(四)、注意事項
本品需冷藏於攝氏15度以下,以酸性飲料或優格配服,若藥品包裝膨脹或藥物顆粒呈現紫黑色,表示藥物已變質請勿服用。
二、Capreomycin 1 gm/vial
商品名Capastat sulfate,簡稱CM,屬抗結核第二線藥物,也是專案藥品中唯一的針劑。
(一)、藥理作用
Capreomycin是一種cyclic polypeptide的抗生素,直到目前為止對於它的藥物作用機轉並不是很清楚,藥物半衰期約4至6小時,capreomycin與viomycin、kanamycin、neomycin有藥物交互拮抗性,腎毒性強,大多伴隨尿液排洩。
(二)、治療劑量
兒童15~30 mg/kg/day,每日最大劑量為1 gm;成人每日1 gm,不得超過20 mg/kg/day。
(三)、副作用
腎毒性、聽神經毒性、前庭神經毒性、暈眩、頭暈、聽力減退、注射部位疼痛或產生硬塊、電解質不平衡、蕁麻疹或皮膚潮紅。
三、Terizidone 250 mg/cap
商品名Terizidon,屬抗結核第二線藥物,簡稱TZN。每顆含Terizidone 250 mg,外觀為淺藍色膠囊。
(一)、藥理作用
屬於抑菌作用的抗結核藥,通常對結核分枝桿菌複合體、其他分枝桿菌、金黃色葡萄球菌有效。口服後大部分會由胃腸道緩慢吸收,在2至3小時內到達最高血中濃度,藥物吸收幾乎不受食物影響。半衰期約21個小時,但在早產兒、新生兒和腎功能受損的病人,半衰期會延長。
一般而言,Terizidon主要是經由腎臟排除,也可經由血液透析來排除,部份由糞便排出。
(二)、治療劑量
每日750~1,000 mg,分3~4次服用。
(三)、副作用
病患易有中樞神經失調的現象如頭痛、暈眩、煩躁不安、顫抖、失眠。偶爾會出現羊癲癇的抽搐以及抑鬱或躁鬱的心理反應。腸胃道不適,如噁心、嘔吐、腹痛、脹氣和腹瀉或便秘,以上症狀停藥後可緩解。
(四)、注意事項
由於對中樞神經的副作用,在一定量的使用之後,會影響到病患的反應能力,特別是和酒精一併使用會增強不良反應。
四、Clofazimine 100 mg/cap
商品名Lamprène,簡稱CFM,屬抗結核第二線藥物,外觀為橢圓形咖啡色膠囊,有GEGIY、G . M白色字樣。
(一)、藥理作用
Clofazimine最常用於治療痲瘋,當clofazimine用於治療結核病時,主要藉由和結核菌DNA的鏈結,加以抑制結核菌複製生成,達成抑菌作用。
Clofazimine具強脂溶性,會累積在人體脂肪組織和網狀內皮系統,病患經長時間治療後在體液、組織、臟器可發現藥物存積。
(二)、治療劑量
每天一次,每次100 mg。
(三)、副作用
結膜、角膜、淚液、汗水、唾液、尿液、糞便、臉部、鼻分泌物、精液、乳汁會變色。視力減弱、乾眼症、發炎、皮膚癢、噁心、嘔吐、腹痛、腹瀉。皮膚毛髮變色由淡紅到棕黑色,可能在停藥後幾個月或幾年才消失。
伍、結論
即使醫療科技日新月異,但由於人為或社會環境諸多因素,以及結核病治療過程漫長,使得世界各地陸續有廣泛抗藥性結核(extensively drug-resistant tuberculosis,簡稱XDR-TB)案例的發生,結核菌株年復一年變得棘手頑強,治療結核病所使用的多重投藥法也因抗結核藥物種類不多而受到阻礙。
為了取得治療先機,疾管局專案引進四種抗結核藥物,但設下較嚴格的藥物管控限制,以避免國內結核菌株抗藥性增強,提早面臨無藥可用的窘境。
與結核病的抗爭是條漫漫長路,即使路途崎嶇難行,我們依然堅定面對未知挑戰,期望每位醫療同仁都與我們並肩向前,迎接戰勝結核的光明未來。
參考資料:
1. 陸坤泰、余明治、李聰明等著:結核病診治指引第三版。台北:行政院衛生署疾病管制局,2008。
2. N. Sarita Shah, Abigail W, Gill-Han B, et al: Worldwide emergence of extensively drug-resistant tuberculosis. Emergeing infectious diseaes 2007; 13: 380-387.
3. Charles AP, Shaun EB, Gwen AH, et al: Once-daily and twice-daily dosing of p-aminosalicylic acid granules. Am J Respir Crit Care Med. 1999; 159: 932-934.
4. Conte FL, Gallou GP, Struillou DB, et al. Pharmacokinetics, toxicity, and efficacy of liposomal capreomycin in disseminated mycobacterium avium beige mouse model. Antimicrobial agents and chemotherapy 1994; 38: 2695-2701.
5. Joia SM, Michael LR, Adrienne RS, et al. Programes and principles in treatment of multidrug-resistant tuberculosis. The lancet 2004; 363: 474-481.
6. Venkata MR, Geeta N, Donna D, et al. Antituberculosis activities of clofazimine and its new analogs B4154 and B4157. Antimicrobial agents and chemotherapy 1996; 40: 633-636.
7. Giovanni DP, Stefano B. Which agents should we use for the treatment of multidrug-resistant Mycobacterium tuberculosis? JAC 2004; 54: 593-602.
MDR Plan from Center for Disease Control: part II
Po-Wen Ko, Wen-tin Kuo
Department of Pharmacy, Chest Hospital, Department of Health, Executive Yuan
Abstract
In order to treat tuberculosis, Center for disease control in Taiwan (CDC) has provided various resources to promote MDR plan since 2007. We introduced the nine anti-tuberculosis drugs of MDR plan in the Journal of Taiwan Pharmacy (vol.24) previously. For fixed-dose combination, CDC has introduced additional four drugs for its anti-tuberculosis regimen.
More specifically, PAS granule 4gm/pack, Capreomycin 1 g/vial, Terizidone 250 mg/cap, Clofazimine 100 mg/cap are four drugs included in this MDR plan. The current article is the follow up of the previous article serving to complete the introduction of CDC's MDR plan. We hope this article will contribute to the fight against tuberculosis.
Key word:
multi-drug resistant tuberculosis、tuberculosis、anti-tuberculosis second-line drug

