摘要
體外心肺支持系統—葉克膜有「靜脈—靜脈」(venovenous, VV) 及「靜脈—動脈」(venoarterial, VA) 兩型,兩者皆提供了肺臟呼吸功能的支援,而VA同時還支援心臟血液動態的調整,故「靜脈—靜脈」葉克膜的適用對象為呼吸衰竭患者,而「靜脈—動脈」葉克膜的適用對象則為心衰竭或呼吸衰竭患者。葉克膜雖具高度侵入性且所費不貲,但如能牢牢掌握住黃金時機適時介入,常能有效扭轉危急的病情於一時。不過仍需留意葉克膜頻傳的併發症,包括:出血、血栓栓塞與heparin所引發的血小板低下,另外,與插管相關的併發症則包括:血管穿孔合併出血、遠端缺血、動脈剝離或錯置插管的疏失。
關鍵字: 葉克膜、急性呼吸窘迫症、respiratory failure、cardiac failure、oxygenator
壹、前言
葉克膜 (ECMO, extracorporeal membrane oxygenation) 是一高度侵入性體外心肺支持系統,醫療費用極為昂貴,不過對於病情幫忙很大。葉克膜的功能,對肺臟而言,不但可取代肺臟行使氣體交換,從而減少患者對呼吸器的依賴,同時也讓肺臟比較有適度休息與恢復的機會;對心臟而言,則可增加組織灌流、改善循環、減輕衰竭心臟的工作量、減少強心劑用量,當然也能讓心臟比較有適度休息與恢復的機會。再者,藉由葉克膜來引流一部分靜脈血液到體外來,既可降低前負荷 (preload),亦可因而緩解鬱血性心衰竭的症狀。只是,葉克膜終究還是無法將疾病治癒,「爭取時間」才是葉克膜真正角色扮演之所在1, 2。
葉克膜最常應用於心肺繞道手術及急性呼吸窘迫症 (ARDS , acute respiratory distress syndrome),因為葉克膜有「靜脈—靜脈」(VV) 及「靜脈—動脈」(VA) 兩型,兩者皆提供了肺臟呼吸功能的支援,而VA同時還支援心臟血液動態的調整。「靜脈—靜脈」葉克膜 (VVECMO,圖一) 的適用對象為呼吸衰竭患者,「靜脈—動脈」葉克膜 (VAECMO,圖二) 的適用對象為心衰竭或呼吸衰竭患者1。
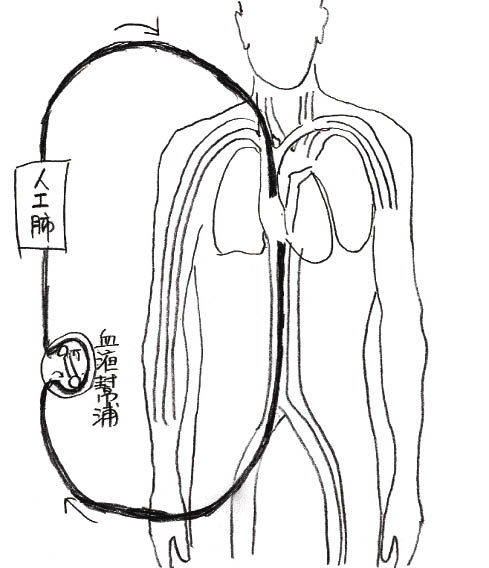
圖一 「靜脈—靜脈」葉克膜 (VVECMO)
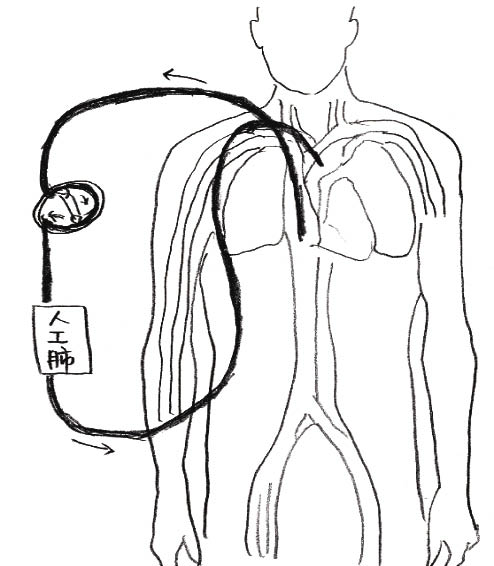
圖二 「靜脈—動脈」葉克膜 (VAECMO)
貳、葉克膜
一、葉克膜適應症
(1)呼吸衰竭:1970年代葉克膜成功應用於臨床上的案例報導正是急性呼吸窘迫症及肺炎等嚴重呼吸衰竭病患。(2)心臟衰竭:心臟手術後一時無法脫離心肺繞道之心衰竭病患或心臟功能停止之病患。不過若葉克膜介入前病患早已出現PH<7.1嚴重酸中毒或使用呼吸器超過七天,其死亡率很有可能偏高1。
二、葉克膜適用對象
葉克膜的適用對象為可逆性急性嚴重心肺衰竭病患;不適用對象為出血、剛完成手術不久、近期內曾發生過顱內受傷、不可逆性心肺衰竭、抗凝血劑使用禁忌、使用呼吸器超過七天、肺腎衰竭、主動脈瓣缺損、高齡、病態性肥胖、神經性失能等病患1。
三、葉克膜裝置技術
(1)幫浦 (即人工心臟):主司先將血液引流到體外,然後再循環回體內。(2)氧合器 (即人工肺臟):主司讓循環於體外的血液充分達到含氧飽合與移除二氧化碳。(3)熱交換器:主司防止循環於體外的血液失溫。(4)連續靜脈注射抗凝血劑:病患在葉克膜使用期間,通常需連續靜脈注射肝素 (heparin),以防止血栓的形成。為了調整肝素的注射速度,應每8小時測量ACT值 (activated clotting time),務使ACT維持於210 ~ 230秒之間。除了肝素之外,還有許多屬於off-label uses的肝素替代用藥的抗凝血劑可選用,例如:血小板抑制劑 (epoprostenol , tirofiban)、thrombin直接抑制劑 (lepirudin , bivalirudin, argatroban)、低分子量肝素danaparoid (danaparoid sodium)3。(抗凝血劑請參考表一4) (5)血小板數目監測:需維持於>100,000/mm3。(6)ACT (activated clotting time) 值監測:需維持於210 ~ 230秒之間1。
表一 抗凝血劑
藥理特性 |
作用機制 |
半衰期 |
劑量調整 |
|
(一)血小板抑制劑 |
||||
epoprostenol sodium (Flolan) |
是一種天然的前列腺素(prostaglandin),會被代謝為花生烯酸(arachidonic acid) |
直接促進肺動脈、全身動脈的擴張以及抑制血小板的凝集 |
3~5 分鐘 |
|
tirofiban hydrochloride (Aggrastat) |
是一種非胜肽血小板醣蛋白抑制劑(non- peptide platelet glycoprotein antagonist) |
經由可逆性抑制纖維蛋白原(fibrinogen)與醣蛋白IIb/IIIa接受器的結合而抑制血小板凝集 |
2~3 小時 |
Clcr <30 mL/minute, 劑量須減半 |
(二)thrombin直接抑制劑 |
||||
lepirudin (Refludan) |
是一具有高度專一性的凝血酵素抑制劑aPTT值的增減會隨著lepirudin的劑量而增減,但lepirudin的藥效與抗凝血酵素Ⅲ(antithrombin Ⅲ)及血小板因子Ⅳ(platelet factor 4)完全無關 |
以1:1的比例(即一分子的lepirudin結合一分子的thrombin)直接抑制血流中的凝血酵素(thrombin) |
0.8~2小時 |
Clcr <60 mL/minute 劑量即須減半 |
bivalirudin(Angiomax) |
是一具有高度專一性的抑制劑 |
直接抑制血流中的凝血酵素(thrombin) |
25分鐘 |
隨腎功能調整 |
Argatroban |
是一凝血酵素(thrombin)直接抑制劑 |
可逆性、選擇性並直接結合在thrombin的活化位置 |
30~51分鐘 |
隨肝功能調整 |
(三)低分子量肝素 |
||||
danaparoid sodium |
是一低分子量heparinoid, 由heparan sulfate(83 %)、dermatan sulfate、 chondroitin sulfate所組成 |
抗凝血作用機制乃經由與heparin cofactor I、heparin cofactor II結合而抑制thrombin |
18-28小時 |
|
參、討論
一、葉克膜的特殊考量
(1)血流量 (blood flow):VVECMO的血流量應設限在極大值,以利於氧氣交換最高極限的達成;反之,VAECMO的血流量則應設限得恰到好處,因一方面既不容許preload超負荷,另一方面更需提供適當的灌流壓及中央靜脈血氧濃度 (ScvO2)。(註:中央靜脈壓 (the central venous pressure, CVP) 是很好的血管內體液容積監測工具,代表著右心室的前負荷,其正常值為0-4 mmHg。中央靜脈血氧濃度 (the central venous oxyhemoglobin saturation, ScvO2),代表心臟打出的血量是否能滿足身體需求的生理指標,正常人為75%5 )。(2)利尿 (diuresis):在葉克膜剛介入初期,患者大多呈體液滯留狀態,因此只要VVECMO患者的狀況一穩定下來,應立刻採取積極的利尿行動;但對於VAECMO的患者,反而須暫緩利尿行動的介入,因為保護腎功能畢竟仍是心衰竭患者的當務之急。(3)監控左心室功能 (left ventricular monitoring) :VAECMO的左心室輸出應予以嚴密監控,因為即便病人已介入了VAECMO,左心室功能的惡化還是有可能發生。而造成左心室輸出持續下降的病因,其實是多因性的,除了患者本身已經存在的左心室衰竭之外,VAECMO的血流亦有可能造成afterload大增;另外,從肺循環或右心室抵達左心室的血流不足亦是原因之一。左心室輸出之所以逐步下降,大多起因於左心室擴大、左心房高血壓或肺出血,此時若投與dobutamine或milrinone等心肌收縮劑,則可有效增強心收縮、降低afterload、提高左心室輸出量。(4)卸除葉克膜 (discontinuation):當肺衰竭患者的動脈達到氧飽和或心衰竭的病患左心室輸出與主動脈脈衝同步時,就是準備卸除葉克膜的好時機。在準備卸下VVECMO之前,往往需先花數小時的時間來移除氧合器內逆向流經的氣體並進行測試。而準備卸下VAECMO之前,則須暫時夾住所有的引流管線與輸注管線,僅保留動脈—靜脈枝作為循環的橋樑,以防止血栓在葉克膜循環內的形成。為了讓血栓形成的風險盡可能的降低,VAECMO的測試時間比VVECMO的測試時間相對的短一些,亦可投與protamine以杜絕heparin殘留的出血傾向,並且需在動脈插管處止血至少30分鐘1。
二、葉克膜的併發症 (complications)
(1)出血 (bleeding):在葉克膜使用期間,通常需連續靜脈注射肝素 (heparin),以防止血栓的形成,可是heparin極易引發血小板功能低下,導致患者發生出血的機率偏高,甚至因而致死,所以當務之急應將ACT穩定在目標值,同時血小板數亦不得小於100,000/mm3。萬一不幸因而發生體腔內出血的情況,則往往需仰賴手術來處置。而在用藥方面也應立刻暫停heparin的輸注並投予屬於plasminogen抑制劑的aminocaproic acid。(2)血栓栓塞 (thromboembolism):由於heparin的連續靜脈輸注,患者發生血栓栓塞的機率並不高。一旦突發血壓階梯性變化,那極可能是血栓栓塞症發生之徵兆。(3)與插管相關的併發症 (cannulation–related):包括血管穿孔合併出血、遠端缺血、動脈剝離或錯置插管的疏失。(4)heparin所引發的血小板低下 (heparin induced thrombocytopenia , HIT):葉克膜通常採用"傳統肝素"(unfractionated heparin , UFH) 來防止血栓,可是由於葉克膜的HIT發生率持續日增,連帶的造成患者因HIT而致死的機率也隨之升高,為了因應如此嚴重的問題,如果我們考慮改由半衰期較短的非heparin抗凝血劑argatroban來取代heparin,一樣的也能有效達成ACT的目標值。根據最新公告的HIT治療準則,建議選擇低分子量肝素danaparoid作為heparin的替代用藥,投與劑量為400 IU/h,其抗第Xa凝血因子的效價為0.6 – 0.8 U/mL (每天須監測兩次)。不過danaparoid並無解毒劑,而且半衰期長 (19–25 h),故很有可能會延誤葉克膜的卸除。法國已核准使用thrombin直接抑制劑lepirudin及低分子量肝素danaparoid。Lepirudin亦無解毒劑,但半衰期短 (60-90 min),對肝素所誘發的抗體並無交叉反應,算是一不錯的選擇用藥。目前雖然尚無實證可以告訴我們到底什麼樣的抗凝血劑才是最佳的選擇,但我們仍然可由患者的腎功能、醫師的個人經驗、特殊藥品供需的方便性以及文獻參考的依據來作取捨。
肆、結語
一如洗腎機之於洗腎患者,葉克膜其實就是一部體外人工心臟與人工肺臟。對於危急的心衰竭或呼吸衰竭患者,如能掌握黃金時機適時的介入葉克膜,常能有效扭轉危急的病情。展望未來葉克膜在急重症醫療的應用上,我們預期將會逐漸增多;不過較為可惜的一點是葉克膜終究是一套極度耗費人力、物力、財力的醫療系統,因此,在使用上務必嚴守三原則:慎選病例、及早使用、積極照顧6。
參考資料:
1. Jonathan Haft, MD; Robert Bartlett, MD: Extracorporeal membrane oxygenation (ECMO) in adults. In: UpToDate (17.1) Jan. 2009
2. Mugford M, Elbourne D, Field D: Extracorporeal membrane oxygenation for severe respiratory failure in newborn infants. In: The Cochrane Database of Systematic Reviews 2009 Issue 3.
3. Christian Bauer, Zuzana Vichova, Patrick Ffrench, et al: Extracorporeal Membrane Oxygenation with Danaparoid Sodium After Massive Pulmonary Embolism. Anesth Analg 2008; 106: 1101-1103.
4. Drug Comparison: Epoprostenol Sodium , Tirofiban Hydrochloride, Bivalirudin, Lepirudin, Argatroban , Danaparoid Sodium. In : MICROMEDEX® 1.0 (Healthcare Series)
5. 孔明河:第十六章 血行動力學的監測。林少琳,重症醫學與護理,台北市,藝軒圖書出版社,2003:1-15。
6. 劉治民:請問:葉醫師是哪位? ECMO簡介。楓城新聞,2007;162:電子版。
Extracorporeal Membrane Oxygenation
Mei - Lin Huang, Hua - Mei Lin
Tao-Yuan General Hospital Department of Health , Department of Pharmacy
Abstract
Although extracorporeal membrane oxygenation (ECMO) is a very invasive and potentially expensive procedure, the benefits of this procedure are high. ECMO refers to prolonged mechanical cardiopulmonary support. There are two types of ECMO — venoarterial (VA) and venovenous (VV). Both provide respiratory support, but only VA ECMO provides hemodynamic support. VV ECMO should be used in patients with respiratory failure. VA ECMO should be used in patients with cardiac failure. Complications are frequent during ECMO. They include bleeding, thromboembolism, and heparin-induced thrombocytopenia. Cannula-related complications include vessel perforation with hemorrhage, arterial dissection, arterial occlusion with distal ischemia, and incorrect location.

