摘要
藥物誘導溶血性貧血為不常見卻嚴重的副作用,抗生素、非固醇類解熱鎮痛劑、oxaliplatin、α-methyldopa 等皆為造成藥物誘導溶血性貧血常見的藥物。此個案使用 diclofenac 後血色素及血容比驟降,幸即時停藥及處理,預後良好。Diclofenac 誘導溶血嚴重者可導致急性腎衰竭、瀰漫性血管內凝集、休克甚至死亡,然而 diclofenac 為一廣泛被使用的藥品,文獻亦提出 diclofenac 誘發的溶血性貧血難與暖型抗體 (warm-reactive autoantibodies) 造成的自體免疫溶血性貧血區分而造成誤診,在此概述藥物誘發溶血性貧血的分類與機轉,藉此提醒醫療同業留意此不良反應。
關鍵字:藥物誘發溶血性貧血、藥物不良反應、diclofenac
壹、前言
藥物誘發溶血性貧血可以是突然的或逐漸的增加體內紅血球的破壞,依溶血位置可分為血管內溶血及血管外溶血,前者為受損的紅血球於循環中被破壞,後者被存在於脾、肝或骨髓中的巨噬細胞吞噬。紅血球表面是否有抗體或補體可由抗球蛋白試驗測試。
貳、案例報告
我們的個案為一位33歲年輕女性,曾於2010年3月因泌尿道感染入院治療,當次住院期間用了2天 diclofenac potassium (25 mg/tab) 口服1# TID,Hb:10.6 g/dL、Ht:30.5 %。2012年8月7-9日入院生產及14-22日因會陰傷口感染所使用的消炎止痛藥皆為 mefanemic acid (500 mg/tab) 口服1# QID。出院後患者於8月31日開始解茶色尿、噁心、嘔吐、食慾不佳、全身倦怠及反覆發燒寒顫至診所求治,因未改善於9月2日至本院急診,急診生化檢查 GOT:80 IU/L、BUN/Cr:18/0.7 mg/dL、Hb/Ht:8.8 g/dL/25.1%,患者雖已在家吃過退燒藥但血色素仍未下降,膚色正常、婦科檢查正常(包括會陰處傷口),急診帶藥除8月住院用過抗生素外另加解熱鎮痛藥 diclofenac 及胃藥 strocain (oxethazaine 5 mg , polymigel 244 mg) 各1# Q6H 需要時用。隔日因症狀未改善至門診,婦產科醫師懷疑患者黃疸轉腸胃科後收入院。患者自述無喝酒及B肝、C肝病史,對蝦過敏。入院後9月4日 GOT:104 IU/L、BUN/Cr:32/1.4 mg/dL、Hb/Ht:5.4 g/dL/15.7 %,投與抗生素及鐵劑、葉酸並停用解熱鎮痛藥,患者Hb/Ht慢慢爬升,約20天後Hb:10.1 mg/dL、Ht:29.3 %。另外住院中的9月4日、6日、10日及出院後13日門診追蹤血液檢體紅血球呈現冷凝集現象,顯示溶血造成患者紅血球呈現冷凝集,9月24日再次門診追蹤已無此現象。個案由血液內科醫師通報疑似 NSAID-diclofenac 引起的溶血不良反應。患者藥歷及實驗室檢查請見表一與表二。
表一 患者藥歷
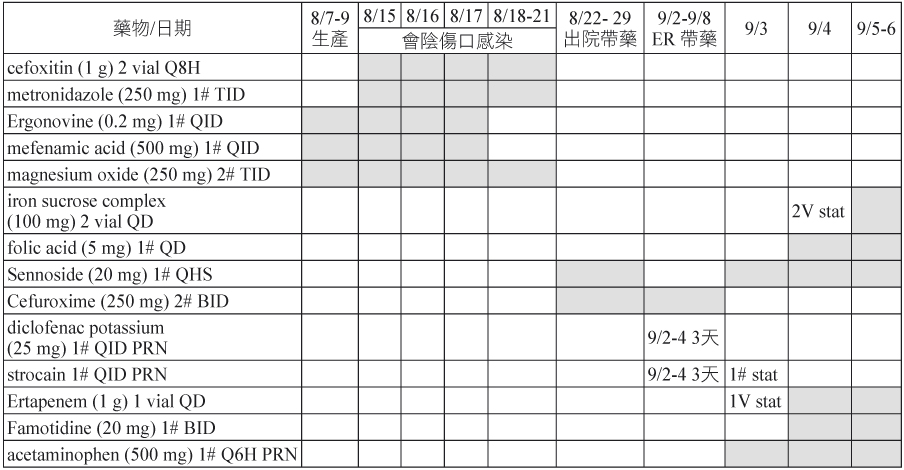
表二 檢驗數據記錄
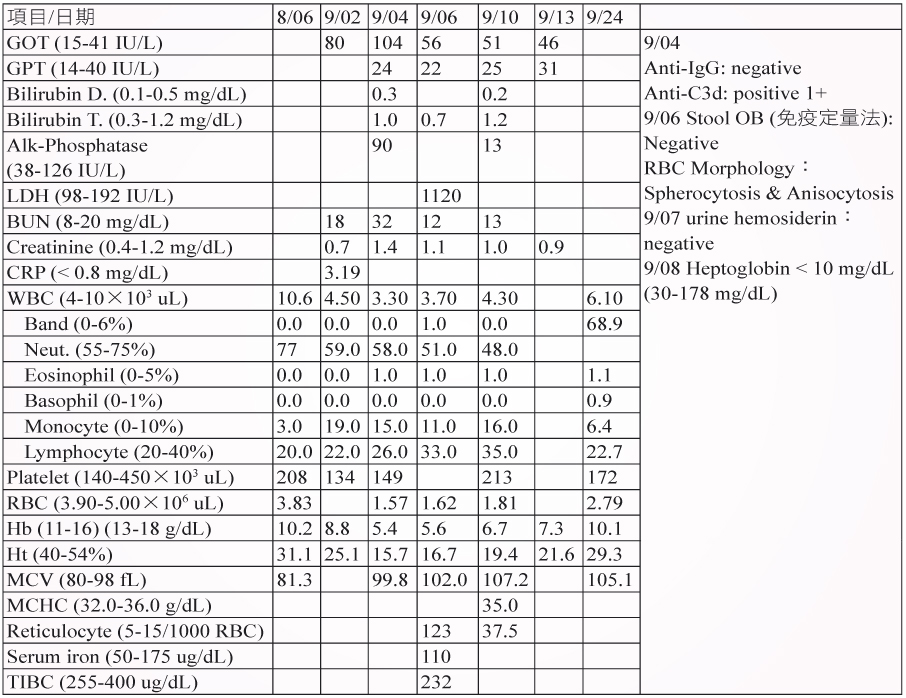
參、藥物誘發免疫溶血的分類與機轉
藥物誘發免疫溶血的機轉大致分兩類3型,亦有教科書細分成四類。
一、 第一類藥物誘發自體抗體 (autoantibodies;aAb)
藥物改變紅血球上的 Rh 抗原導致抗體產生,抗體直接與紅血球上 Rh 複合物產生反應,此抗體亦會與未改變抗原的紅血球反應,藥物不須共同參與抗原抗體反應,直接抗球蛋白試驗 (direct antiglobulin test or direct coombs' test) anti-IgG 為陽性、anti-C3則為陰性1,此型於臨床症狀上與血清學上很難與原發性溶血 (idiopathic form) 區分2。此類的代表藥物為 α methyldopa、L-dopa、procainamide、mefanemic acid3,通常發生在用藥數週或數月後,溶血為慢慢進展由輕微至中度,停藥後溶血仍然會持續數週或3-4個月 (紅血球的壽命),可投與類固醇加速復原1。
二、 第二類藥物成為抗原的一部分參與抗原抗體反應
(一)Penicillin 型
非補體活化藥物依賴型抗體 (non-complement-activating drug-dependent antibodies; ddAb),亦稱為藥物吸附型,藥物本身或代謝物會引發抗體且藥物或其代謝物會共價的結合在紅血球表面,抗體 IgG 會和紅血球表面的藥物或代謝物反應,溶血是因巨噬細胞吞噬作用移除有 IgG 抗體的紅血球,主要發生在脾臟為血管外溶血3,病人可能出現輕微、中度至嚴重的貧血,症狀有蒼白虛弱、不舒服、心悸、呼吸困難、頭痛和黃疸。此型的藥物代表有 penicillin,溶血通常發生在長期大劑量的使用 penicillin ( > 2千萬單位/day)3,發生溶血時病人的直接抗球蛋白試驗 anti-IgG 為陽性、anti-C3 則為陰性,間接抗球蛋白試驗 (indirect antiglobulin test or indirect coombs' test) 於正常紅血球呈陰性、以 penicillin 覆蓋的紅血球呈陽性,此表示病人的細胞覆蓋 IgG 抗體,這些抗體只有當 penicillin 結合到紅血球表面時才會附著上去3。藥物停用後溶血會於數天內停止,直接抗球試驗也會逐漸的轉為陰性,若貧血狀況嚴重則須輸血,一般不須投與類固醇2。
(二)免疫複合型
補體活化藥物依賴型抗體 (complement-activating drug-dependent antibodies),藥物或其代謝物與血漿蛋白結合形成具免疫原的共軛物 (immunogenic conjugated) 誘發抗體產生,抗體與此共軛物反應形成免疫複合物黏到紅血球上,活化補體至紅血球造成血管內溶血,藥物或其代謝物不會穩固的結合到紅血球表面,當補體黏上紅血球後,抗原抗體免疫複合物即離開與下一個紅血球結合,補體又黏上來,所以小劑量即可能產生嚴重的血管內溶血3,病人可能出現發燒、寒顫、噁心、嘔吐、頭痛、腹痛、心悸及呼吸困難,溶血嚴重甚至造成急性腎衰竭。一旦藥物停用溶血會快速緩解,根據藥物於體內的清除率1。病人的直接抗球蛋白試驗 anti-IgG 為陰性、anti-C3 則為陽性1。
臨床上藥物導致溶血性貧血通常為混合型包含藥物產生藥物依賴型抗體與自體抗體,藥物誘發的溶血性貧血若為第一次用藥至少須6天產生免疫反應,之後此反應可發生於持續治療或間歇治療 (continous or intermittent therapy) 或再次暴露於致敏藥物時立即產生4。Diclofenac 為一常用的非固醇類消炎止痛藥,其誘發溶血的機轉為 diclofenac 或 diclofenac 的代謝物存在下由補體活化 IgG 和 (或) IgM 抗體與紅血球反應。Diclofenac 或其代謝物產生藥物依賴性抗體和 (或) 產生抗紅血球的自體抗體5。Diclofenac-induce hemolysis 造成急性血管內溶血、急性腎衰竭甚至死亡。病人出現腹部疼痛、疲倦、蒼白或黃疸等急性免疫性溶血症狀5,實驗值檢查顯現血色素及血容比降低、乳酸去氫酶上升、間接膽紅素 (indirect bilirubin) 上升、血紅素血症 (hemoglobinemia)、血紅素尿症 (hemoglobinuria)、網狀紅血球 (reticulocyte) 增加、血紅素結合蛋白 (haptoglobin) 降低,血液抹片顯現球狀血球 (spherocytes) 和帶核紅血球 (nucleated red blood cells)。
肆、案例討論
個案呈現溶血的症狀如黃疸、紅血球形態大小不一 (anisocytosis) 及出現球狀紅血球 (spherocytosis)、網狀紅血球增多、血紅素結合蛋白降低、乳酸去氫酶 (LDH) 破千代表血管內溶血,另外9月4日抗體篩檢為陽性、anti-IgG:negative、anti C3d:postive。Diclofenac 誘導溶血為免疫複合型,因活化補體,小劑量即能產生溶血,一旦停藥溶血會快速緩解,diclofenac 排除半衰期約2小時,故9月7日尿液 hemosiderin:negative 代表已無血管內溶血。因 diclofenac 亦會產生抗紅血球的自體抗體,故9月13日門診追蹤血液檢體紅血球仍呈現冷凝集現象,代表血管外溶血仍存在。另外使用抗生素期間血色素皆未降低,使用其他藥品與發生溶血性貧血的時序上不符及參考文獻,應可排除為其他用藥造成。本案例經 Naranjo score 評量後得分為4分 (請見表三),列為可能由 diclofenac (25 mg/tab) 引起的溶血不良反應。
表三 Diclofenac 藥物不良反應評估單 (Naranjo score)

伍、結論
Diclofenac 誘發的溶血性貧血與暖型抗體 IgG 造成的自體免疫溶血性貧血,患者一開始表現的症狀皆可能為腹痛、嘔吐、黃疸,間接膽紅素 (indirect bilirubin) 和乳酸去氫酶上升、血紅素結合蛋白降低,出現球狀紅血球及網狀紅血球增多,醫師可能誤判為自體免疫造成的溶血5,這是須要特別留意的,若病人是因藥物造成則應避免再次使用該藥物,若為自體免疫造成則須投與類固醇或免疫抑制劑,兩者處理方式不同。
參考資料:
1. Wendell F Rosse, Stanley L Schrier: Pathogenesis of autoimmune hemolytic anemia: Warm agglutinins and drugs. UpToDate online. Available at http://www.uptodate. com (cited: 22/11/2012).
2. Abdulgabar Salama Drug-induced immune hemolytic anemia Expert Opin Drug Saf. 2009 Jan; 8(1): 73-9.
3. Samuel I. Raoaoirt 原著/王正宏編譯 血液學第二版 藝軒圖書出版社, 2002.
4. J. S. Jürgensen, A. Seltsam, A. Jörres: Fatal acute diclofenac-induced immune hemolytic anemia Ann Hematol (2001) 80: 440-442.
5. Norbert Ahrens, Ramona Genth, Holger Kiesewetter, et al: Misdiagnosis in patients with diclofenac-induced hemolysis: New cases and a concise review. Am J Hematol. 2006 Feb; 81(2): 128-31.
Suspected Diclofenac-Induced Hemolytic Anemia
Hsueh-Chin Wen, Hsiao-Lan Wang, Mei-Hui Wu, Hui-Ru Lai
Department of Pharmacy, Mackay Mermorial Hospital Tamsui Branch
Abstract
Drug-induced immune hemolytic anemia is a rare but a serious adverse reaction. Antibiotics, nonsteroidal anti-inflammatory drug, oxaliplatin, alpha-methyldopa etc are the drugs that most frequently cause immune hemolytic anemia. The case of a 33-year-old woman who developed Hb/Ht dropping sharply after treated with diclofenac (25 mg) prn used for fever. Diclofenac was discontinued and the patient was treated with ferrous and folic acid. She was discharged in good prognosis. Diclofenac induced immune hemolytic anemia in severe case may cause acute renal failure, disseminated intravascular coagulation, shock and even be fatal. Diclofenac is a widely used nonsteroidal anti-inflammatory drug. Nevertheless, it cause hemolytic syndrome very similar to autoimmune hemolytic anemia of warm type. In this review, the pathogenic mechanisms and types of drug induced immune hemolytic anemia for reminding the medical staff to be careful to the adverse drug reactions.

