摘要
大腸直腸癌治療藥物近年來不斷有進展,早期合併使用5-fluororuracil 及 oxaliplatin 或 irinotecan 使得存活率增加,而標靶治療藥物,像是血管內皮細胞生長因子抑制劑 bevacizumab (Avastin)、aflibercept (Zaltrap, 柔癌捕),及上皮生長因子受體抑制劑-cetuximab (Erbitux)、panitumumab (Vectibix),多重標靶酪胺酸激酶抑制劑 regorafenib,提供病人更多的治療機會。2016年美國國家癌症資訊網 (National Comprehensive Cancer Network, NCCN) 準則新增大腸直腸癌新藥 trifluridine/tipiracil (Lonsurf) 和 ramucirumab (Cyramza),trifluridine/tipiracil 用於已經用過其他治療藥品的轉移性大腸直腸癌病人,ramucirumab 則是與 FOLFIRI 併用,治療已經用過其他治療第一線藥品,像是 fluoropyrimidine、bevacizumab、oxaliplatin 的轉移性大腸直腸癌病人,免疫治療藥品像是 pembrolizumab 在台灣有針對轉移性大腸直腸癌病人的臨床試驗仍在進行中。
關鍵字:trifluridine/tipiracil、ramucirumab、colorectal cancer、chemotherapy、target therapy
壹、前言
衛福部國健署2016年4月公布2013年癌症發生統計,平均每5分18秒就有1人罹癌,較前一年增快8秒,大腸癌則是蟬聯8年新發癌症人數最多的癌別1。同時台灣大腸癌發生率全球第一 (圖一)2,3,因此大腸癌的用藥特別值得關注。目前大腸癌藥品常用的治療處方有5-FU 加上 leucovorin、tegafur-uracil、FOLFOX (5-FU + leucovorin + oxaliplatin)、capecitabine、FOLFIRI (5-FU + leucovorin + irinotecan) 搭配一種標靶藥品 (bevacizumab、aflibercept、cetuximab 或 panitumumab)、regorafenib。美國國家癌症資訊網 (National Comprehensive Cancer Network, NCCN) 公佈2016年第二版指引中,提到兩種新藥,分別是 Trifluridine/tipiracil 和 ramucirumab,本文將詳細介紹這兩種藥品。
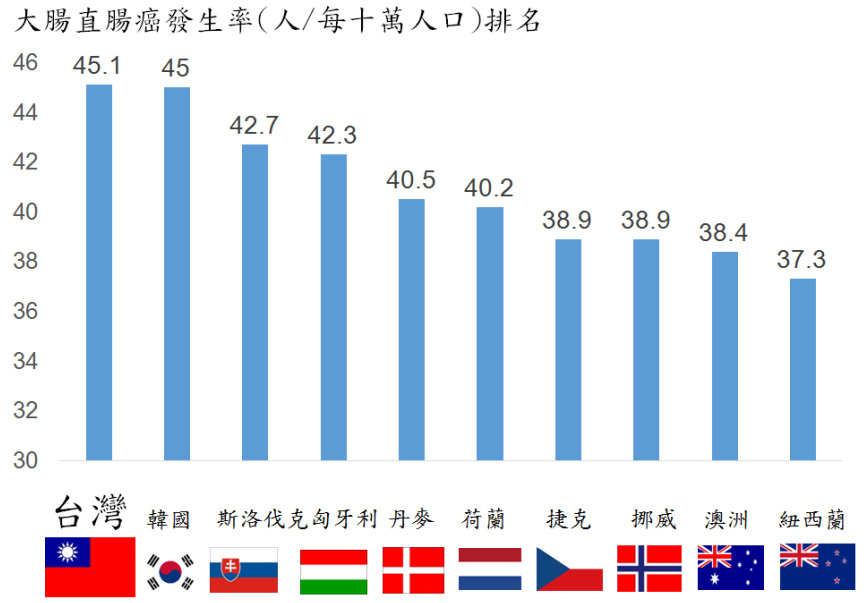
圖一 全球大腸直腸癌發生率前十大排名2,3
貳、藥物個論
一、Trifluridine/tipiracil
藥名學名 trifluridine/tipiracil,原廠商品名 Lonsurf,是源自於日本的新藥,在隨機分派雙盲臨床試驗中,收納800位第四期治療後復發的大腸直腸病人,以2:1的方式隨機分配至 trifluridine/tipiracil 組和安慰劑組,平均整體存活率安慰劑組為5.3個月,trifluridine/tipiracil 組則為7.1個月,具有統計上顯著差異,作用機轉方面,由於受試者大多是對 fluoropyrimidines 無效,學者推論其作用機轉與 fluoropyrimidines 不同4,trifluridine/tipiracil 藥理分類上屬於抗代謝藥物的嘧啶類似物,trifluridine 是胸腺嘧啶核苷類似物,tipiracil 是胸腺嘧啶 phosphorylase 抑制劑,可以減少 trifluridine 被胸腺嘧啶 phosphorylase 代謝,trifluridine 進入癌細胞後,嵌合入癌細胞的 DNA 中,抑制癌細胞增生。FDA 適應症 (服用時機) 為:用於已經接受過 fluoropyrimidine、oxaliplatin 和 irinotecan 為基礎的化學治療,和抗血管內皮生長因子生物製劑,和抗上皮生長因子受體的單株抗體 (如果 RAS 屬於野生型) 治療的轉移性大腸直腸癌病人5。如同傳統化療藥,trifluridine/tipiracil 具有胚胎-胎兒毒性,基於藥理和大鼠的實驗,推斷孕婦服用 trifluridine/tipiracil 可能引起胎兒致命性的傷害,仿單建議可能懷孕的女性服用 trifluridine/tipiracil 時應服用避孕藥,此外根據大鼠研究,乳汁中存在 trifluridine/tipiracil 和代謝物,服用 trifluridine/tipiracil 期間不建議哺乳,在最後一劑 trifluridine/tipiracil 後再等一天才能哺乳。
臨床試驗中,trifluridine/tipiracil 會引起嚴重或致命的骨髓抑制 (Grade 3-4),包含貧血 (18%)、嗜中性球低下 (38%)、血小板過低 (5%) 和嗜中性球低下合併發燒 (3.8%),有9.4%的病人需要施打顆粒性白血球聚落刺激因子,如同大多數的傳統化療藥,不分嚴重程度,則 trifluridine/tipiracil 引起噁心 (48%) 的機率多於嘔吐 (28%),約有2%的病人發生第三級以上的噁心,第三級以上的嘔吐也是2%,3%的病人發生第三級以上的腹瀉。約7%受試者出現落髮問題5。Trifluridine/tipiracil 服用方式特殊,trifluridine 35 mg/m2 BID,是在第1天至第5天然後第8 天服藥至第12天,每28天一個週期,每一劑最大劑量80 mg。服用後2小時達尖峰濃度,trifluridine 的蛋白結合率超過96%,tipiracil 則小於8%,trifluridine/tipiracil 不經由 CYP450酵素代謝,trifluridine 主要經由 thymidine phosphorylase 代謝成不活化的5-trifluoromethyl uracil (FTY)。2%的 trifluridine 尿液以原型藥排除,約19%以不活化的代謝物5-trifluoromethyl uracil 型式自尿中排除,而 tipiracil 約29%在尿液以原型藥排除6。穩定狀態下 trifluridine 半衰期約為 2.1小時,tipiracil 半衰期約為 2.4小時。仿單無已知的重要的藥物交互作用,以關鍵字 (trifluridine[title] AND interaction) 搜尋 pubmed 亦無任何文獻紀載交互作用。根據 NCCN 準則,trifluridine/tipiracil 致吐等級屬於中度至高度致吐性,可能需要 dexamethasone 止吐7。
二、Ramucirumab
藥名學名 ramucirumab,原廠商品名為 Cyramza,藥理分類屬於抗腫瘤藥物的單株抗體。2015年一項隨機分派雙盲試驗,收納1,072位第四期治療後復發的大腸直腸病人,以1:1隨機分配至 FOLFIRI (irinotecan、leucovorin 和 fluorouracil) + ramucirumab 組和 FOLFIRI + 安慰劑組,平均整體存活率 ramucirumab 組為13.3個月,安慰劑組則為11.7個月,具有統計上顯著差異。作用機轉方面,ramucirumab 是重組基因抗體,能抑制血管內皮生長因子受體-2(vascular endothelial growth factor receptor 2, VEGFR2)。Ramucirumab 對 VEGFR2具有高度親和力,阻止 VEGF-A、VEGF-C 和 VEGF-D 等配體 (ligand) 活化 VEGFR2,藉以抑制配體引起的內皮細胞增生和移動,可以減少腫瘤中微小血管之形成和腫瘤生長9。FDA 核准 ramucirumab 在大腸直腸癌的適應症為:與 FOLFIRI 併用,治療正在使用或使用過 bevacizumab、oxaliplatin 和 fluoropyrimidine 仍疾病惡化的轉移性大腸直腸癌10。由於 ramucirumab 抑制血管新生,而血管新生對人類胎兒至關重要,因此對胎兒可能造成傷害,有可能懷孕的婦女應考慮同時服用避孕藥,直到最後一劑 ramucirumab 打完後三個月。Ramucirumab 是人源性 (humanized) 免疫球蛋白 G1單株抗體 (抗體是免疫球蛋白),基於免疫球蛋白會被分泌到乳汁中,因此推斷 ramucirumab 會被分泌到乳汁中,不建議施打 ramucirumab的哺乳婦女使用。Ramucirumab 常見的是高血壓 (16%)、腹瀉 (14%)、紅血球減少而須輸血 (11%)、頭痛 (9%)、蛋白尿 (8-17%)、嗜中性球低下 (5%)、流鼻血 (5%),雖與 bevacizumab 相似,但 bevacizumab 毒性稍低,且費用相對較便宜,所以 NCCN 準則仍建議第一線應優先使用 bevacizumab。
Ramucirumab 排除半衰期為14天,須搭配 FOLFIRI,每兩週以8 mg/kg 之劑量輸注,ramucirumab 不可推注,建議採用0.22 μm 的過濾器並且設定輸注幫浦每次至少輸注60分鐘,直到疾病惡化或不能忍受毒性為止。仿單並未記載交互作用,以關鍵字 (ramucirumab [title] AND interaction) 搜尋 pubmed 亦無任何文獻紀載交互作用。要注意 ramucirumab 可能引起腸胃出血或腸穿孔,這類病人一旦出現此類症狀應永久停用,有心血管疾病的病人應注意心衰竭副作用。
參、結論
免疫療法藥物 Pembrolizumab 雖然也出現在2016年美國國家癌症資訊網準則之大腸癌新藥之列,但該準則仍不建議使用在大腸直腸癌病人身上,台灣藥品臨床試驗資訊網,有一篇名為「一項比較 Pembrolizumab (MK-3475) 治療與化學治療於高度微衛星不穩定性 (MSI-H) 或錯誤配對修復缺失 (dMMR) 第四期大腸直腸癌受試者的第三期臨床試驗 (KEYNOTE-177)」,還在進行臨床試驗中,期待能帶給這類患者正向的結果。Ramucirumab 目前屬於專案進口藥品,衛福部適應症仍是用於晚期或轉移性胃腺癌 (或胃食道接合處腺癌) 病人。Trifluridine/tipiracil 在衛福部藥品許可證查詢網頁、台灣藥品臨床試驗資訊網亦無相關資料,但值得繼續關注,總之,2016年版新增的 trifluridine/tipiracil 和 ramucirumab,提供原本藥物以外更後線的治療,讓多重藥物使用後仍疾病惡化的病人,有更多延長生命的治療方式。
New Antineoplastic Agents in 2016 NCCN Guideline of Colon Cancer
Hung-Yi Chen
Department of Pharmacy, National Cheng Kung University Hospital
Abstract
In recent years, there is a continuous progress in the treatment of colorectal cancer. In earlier period, combination therapy of 5-fluororuracil and oxaliplatin or irinotecan increased survival rate of colorectal cancer patient. Targeted therapy such as vascular endothelial growth factor (bevacizumab, aflibercept), epidermal growth factor receptor (cetuximab, panitumumab) and multi-kinase inhibitor (regorafenib) provide more opportunities for these patients. In 2016, the National Comprehensive Cancer Network (NCCN) published new guideline which contains two new antineoplastic agents, trifluridine/tipiracil (Lonsurf) and ramucirumab (Cyramza). Trifluridine/tipiracil is used to treat adults with metastatic colorectal cancer who have already been treated with, or who cannot be given, other available treatments.Ramucirumab is used in combination with FOLFIRI for the treatment of patients with metastatic colorectal cancer (mCRC) whose disease has progressed on a first line bevacizumab-, oxaliplatin- and fluoropyrimidine-containing regimen. On the other hand, immunotherapy agent such as pembrolizumab is still in clinical trial in Taiwan.
參考資料:
1. 聯合新聞網 http://goo.gl/4bBxDv
2. 蘋果日報http://goo.gl/1czXim
3. http://www.wcrf.org/int/cancer-facts-figures/data-specific-cancers/colorectal-cancer-statistics
4. Mayer RJ, Van Cutsem E, Falcone A, et. al: Randomized trial of TAS-102 for refractory metastatic colorectal cancer. N Engl J Med. 2015;372(20):1909-19.
5. Trifluridine/tipiracil仿單available at: http://www.accessdata.fda.gov/drugsatfda_docs/label/2015/207981s000lbl.pdf
6. Trifluridine and tipiracil: Drug information In: UpToDate (Accessed on June 3, 2016.)
7. https://www.nccn.org/professionals/physician_gls/pdf/antiemesis.pdf
8. Tabernero J, Yoshino T, Cohn AL, et. al: Ramucirumab versus placebo in combination with second-line FOLFIRI in patients with metastatic colorectal carcinoma that progressed during or after first-line therapy with bevacizumab, oxaliplatin, and a fluoropyrimidine (RAISE): a randomised, double-blind, multicentre, phase 3 study. Lancet Oncol. 2015;16(5):499-508.
9. Ramucirumab: Drug information In: UpToDate (Accessed on June 3, 2016.)
10. http://www.cancer.gov/about-cancer/treatment/drugs/fda-ramucirumab#crc

