摘要
Klebsiella pneumoniae carbapenemase (KPC)-producing Klebsiella pneumoniae 造成臨床感染問題日益普遍,針對此超級細菌可能有效的治療藥物為 tigecycline、polymyxins (colistin and polymyxin B)、及 aminoglycosides,選擇二至三種抗生素合併療法對於重度感染症病人或許可改善預後。面對此多重抗藥性菌株所造成的感染症,醫界已面臨無藥可用的困境,為今之計,落實感染管制措施及執行抗生素管理計畫,方能遏止多重抗藥性菌株於病人與病人間散播及預防因不當的抗生素使用而篩選出超級細菌。
關鍵字:Carbapenem-resistant Enterobacteriaceae (CRE)、Klebsiella pneumonia carbapenemas (KPC)、多重抗藥性菌株、合併療法
壹、前言
隨著 carbapenem-resistant Enterobacteriaceae (CRE,carbapenem 抗藥性腸內菌屬) 的出現,carbapenem 類抗生素的抗藥性成為全球注目之議題,回顧文獻報告,carbapenem 抗藥性細菌以腸內菌屬佔絕大部分,被研究較廣泛的抗藥性基因以 Klebsiella pneumonia carbapenemas (KPC,克雷伯肺炎桿菌產碳氫黴烯酶) 最為重要,而攜帶 KPC 抗藥基因的菌株又以 KPC-producing Klebsiella pneumonia最為常見。KPC 自1996年於美國北卡羅納州首次發現後,迄今已散布至全世界,此抗藥基因位於細菌質體,且不局限於克雷伯菌屬,可跨菌株、跨屬、跨種間水平基因轉移 (horizontal gene transfer) (表一),使 KPC 抗藥基因得以在醫院內和醫院間傳播,因此,引發醫界對此類 CRE 的高度關注1,2。由於 carbapenem 類抗生素現今仍是腸內菌嚴重感染症的首選用藥,隨著這些多重抗藥性菌株的出現,醫界已面臨無藥可用的困境。為此,執行有效的感染管制措施以遏止 CRE 散播,儼然成為現今醫療的重要課題。
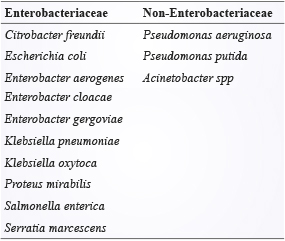
表一 克雷伯肺炎桿菌仍是帶有 KPC 抗藥基因最常見的菌株,回顧文獻中已被分離出帶有 KPC 抗藥基因之格蘭氏陰性菌如下表所示2
貳、流行病學
根據流行病學調查,CRE 發生率為2.93/100,000住院人次3,美國 Centers for Disease Control and Prevention (CDC) 指出,carbapenem-resistance K. pneumoniae 盛行率已由2000年小於1%上升至2007年8%4,而位於紐約州某醫學中心 carbapenem-resistance K. pneumoniae 抗藥菌株比率由2002年9%、2004年18%,上升至2008年38%2。2013-2015年台灣抗生素管理計畫調查全台示範中心 carbapenem-resistance K. pneumoniae 抗藥性比率約為8.5%-10%5。
參、臨床特徵
感染 KPC-producing K. pneumoniae 之危險因子包括:老年人、重症病人、使用過抗生素治療、移植病人、呼吸器使用及長期住院等。曾投予 carbapenem 類抗生素是否會衍生出 KPC 菌株感染目前尚未定論,而 fluoroquinolone 及廣效性 cephalosporin 等抗生素的使用則為產生 KPC 菌株感染或移生 (colonization) 之獨立危險因子2,6。此類菌株所造成的感染,延長了病人住院天數與增加醫療費用,且受限於抗生素的選擇性不多,往往預後不佳,以菌血症為例,死亡率為47%-66%7。微生物實驗室常規檢測 KPC 菌株有一定之困難度,連帶影響了抗生素用藥選擇時效性及病人預後。
肆、治療原則
KPC 菌株所造成的感染,治療療程選擇依其感染部位、嚴重度及藥敏試驗結果而定,臨床可供選擇的抗生素所剩無幾,通常僅剩 polymyxins、tigecycline 及部分的 aminoglycosides 等抗生素具感受性 (susceptible)。非複雜性之泌尿道感染一般可選用 aminoglycoside 類抗生素做為單一療法治療,若面對嚴重型感染,包括菌血症,由於死亡率極高、合併療法可能改善死亡率、單一抗生素治療可能誘發抗藥性及缺乏明確療效的替代藥物等因素,則建議使用二至三種抗生素合併療法 (combination therapy) 作為療程選擇,目前最佳合併療法之組合仍未有定論,對於重度感染,合併療法之選擇應包括 polymyxin 類抗生素,當 KPC 菌株對於 meropenem 之 MIC ≦ 8 mcg/mL,合併療法可考慮加入 meropenem,而其他可選用的抗生素還包括 tigecycline、aminoglycosides、aztreonam 及 ceftazidime-avibactam 等藥物。根據 Tumbarello 等人針對125位 KPC-producing Klebsiella pneumonia 菌血症病人所進行之研究,單一療法與合併療法之30天死亡率呈統計學差異 (54.3% vs 34.1%;P = .02),而敗血性休克、抗生素選用不當及高 APACHE III 分數則為死亡獨立危險因子,以 tigecycline、colistin 及 meropenem 作為合併療法療程選擇則可降低死亡率 (OR: 0.11; 95% CI: .02–.69; P = .01)8。Polymyxins 屬於環狀多肽類抗生素,分為 A-E 類,目前有 polymyxin B 與 E (colistin) 供臨床治療,過去因受限於腎毒性及神經毒性未被廣泛使用,polymyxin 對 KPC 菌株約90-100%具感受性,此類抗生素屬於濃度依賴型之殺菌模式 (concentration-dependent bactericidal killing),且對於 KPC 菌株所造成的菌血症是目前唯一可達適當血中治療濃度之抗生素。Tigecycline 屬於 glycylcycline 類抗生素,儘管是非仿單提及之感染適應症,通常仍被使用在 KPC 菌株及其他多重抗藥格蘭氏陰性菌所造成的感染,此藥品於血液及尿液濃度不高,不建議單獨用於治療菌血症及泌尿道感染。
伍、感染管制
腸內菌感染向來是院內感染之主要原因,及早偵測出 KPC 菌株為感染管制任務是否成功至關重要的條件。在特定的情況下,可藉由主動篩檢來偵測病人是否有 KPC 移生之情形以落實感染管制及預防橫向擴散。美國 CDC 則建議當出現 KPC 群突發事件時進行主動篩檢,即使非 KPC 盛行之機構應檢視過去6-12個月之臨床檢體,確定是否曾出現未被偵測出的 KPC 菌株9。積極的感染管制措施有助於降低 KPC 菌株於不同層級醫院之散播,組合式感染管制措施包括了加強環境清潔與消毒、主動篩檢、進行抗生素管理、遵守接觸隔離規定及執行手部衛生工作。
陸、結論
由於抗生素新藥開發不易,面對 KPC 菌株所造成的嚴重感染往往治療效果有限,意味著唯有加強感染管制措施並結合抗生素管理才能遏止多重抗藥性細菌於病人與病人間散播及預防因不當使用抗生素而篩選出超級細菌。
Treatment Options for KPC-producing Bacterial Infection
Hsuan-Ling Hsiao, Shin-Tarng Deng, Chi-Hua Chen
Department of Pharmacy, Chang Gung Memorial Hospital, Linkou
Abstract
Klebsiella pneumoniae carbapenemase (KPC)-producing Klebsiella pneumoniae are becoming increasingly prevalent in a variety of clinical settings. Possible candidate therapies for infections caused by KPC-producing organisms are tigecycline, polymyxins (colistin and polymyxin B), and aminoglycosides. Combination therapy may offer a survival benefit in severely ill patients. The shortage of new antimicrobial agents on the immediate horizon suggests that enhanced adherence with infection prevention procedures and antimicrobial stewardship programs are required to restrain patient-to-patient transmission and to reduce the selection of multidrug-resistant bacteria.
參考資料:
1.Munoz-Price LS, Poirel L, Bonomo RA, et al: Clinical epidemiology of the global expansion of Klebsiella pneumonia carbapenemases. Lancet Infect Dis 2013; 13: 785-96.
2. Arnold RS, Thom KA, Sharma S, et al: Emergence of Klebsiella pneumoniae carbapenemase-producing bacteria. South Med J 2011; 104: 40-45.
3. Guh AY, Bulens SN, Mu Y, et al: Epidemiology of Carbapenem- Resistant Enterobacteriaceae in 7 US Communities, 2012-2013. JAMA 2015; 314: 1479-87.
4. Centers for Disease Control and Prevention (CDC). Guidance for control of infections with carbapenem-resistant or carbapenemase-producing Enterobacteriaceae in acute care facilities. Morb Mortal Wkly Rep 2009; 58: 256-60.
5. 2015年抗生素管理計畫示範中心交流會議資料。
6. Gasink LB, Edelstein PH, Lautenbach E, et al: Risk factors and clinical impact of Klebsiella pneumoniae carbapenemase-producing K. pneumoniae. Infect Control Hosp Epidemiol 2009; 30: 1180-85.
7. Nadkarni AS, Schliep T, Khan L, et al: Cluster of bloodstream infections caused by KPC-2 carbapenemase-producing Klebsiella pneumoniae in Manhattan. Am J Infect Control 2009; 37: 121-26.
8. Tumbarello M, Viale P, Viscoli C, et al: Predictors of mortality in bloodstream infections caused by Klebsiella pneumoniae carbapenemase-producing K. pneumoniae: importance of combination therapy. Clin Infect Dis 2012; 55(7): 943-50.
9. Centers for Disease Control and Prevention (CDC). Guidance for control of infections with carbapenem-resistant or carbapenemase-producing Enterobacteriaceae in acute care facilities. Morb Mortal Wkly Rep. 2009; 58: 256-60.

