困難梭狀桿菌相關腹瀉治療的新進展
林口長庚紀念醫院藥劑部藥師 王筱君、周心怡、鄧新棠、蕭旋玲
摘要
困難梭狀桿菌相關的腹瀉 (Clostridium difficile-associated diarrhea;CDAD) 是造成醫療相關胃腸道疾病最主要的原因,並且對我們的健康照護體系造成很大的負擔。治療 CDAD 的首選藥物為 metronidazole 或口服 vancomycin,美國食品藥物管理局 (The US Food and Drug Administration;FDA) 於2011年核准 fidaxomicin 上市,與 vancomycin 相比,有較佳的長期療效,更重要的是能降低疾病復發率,因此美國感染症醫學會 (Infectious Diseases Society of America;IDSA) 與美國健康照護流行病學會 (Society for Healthcare Epidemiology of America;SHEA) 在2017年更新困難梭狀桿菌感染之治療指引時,正式將 fidaxomicin 列為治療成人 CDAD 第一線用藥的選擇之一。本文將探討 fidaxomicin 用於治療 CDAD 的新進展。
關鍵字: Clostridium difficile-associated diarrhea(CDAD)、fidaxomicin、vancomycin、metronidazole
壹、前言
困難梭狀桿菌 (Clostridium difficile,以下簡稱C. difficile) 是一種會產生孢子及毒素的革蘭氏陽性厭氧桿菌,屬於人體腸道內的正常菌叢,於正常狀態下與其他腸道菌相互競爭而達到平衡時,並不會致病;然而,若此平衡遭受破壞,困難梭狀桿菌便可伺機大量繁殖而造成人體致病性感染。常見之危險因子如:抗生素長期不當使用、年紀大之住院病患及接受胃酸抑制劑治療等1。
一旦形成感染,C. difficile 將大量產生毒素,造成人體腸道上皮組織發炎,臨床症狀為:腹瀉 (Clostridium difficile-associated diarrhea;CDAD)、腹脹、發燒、偽膜性腸炎、巨腸症、腸穿孔等2。
CDAD 是目前醫療機構常見的感染性腹瀉,並會藉由醫療照護過程加以傳染,嚴重者可能導致死亡。一篇台大醫院的前瞻性臨床研究指出,感染 C. difficile 的發生率為4.5人次/104 病人日,加護病房的比例更高達79人次/104病人日;成大醫院的回溯性臨床研究結果顯示,發生率為4.26人次/104病人日,加護病房則有11.06人次/104病人日3,4。
美國食品藥物管理局於2011年核准 fidaxomicin 用於治療 CDAD,根據近年臨床文獻指出,其治療效果與 vancomycin 相當甚至較佳,並能更有效地降低疾病復發率5。目前 fidaxomicin 已是美國感染症醫學會 (Infectious Diseases Society of America;IDSA) 與美國健康照護流行病學會 (Society for Healthcare Epidemiology of America;SHEA) 制定之成人困難梭狀桿菌感染治療指引中的第一線用藥選擇之一,而根據台灣健保給付規範,經使用 metronidazole 及口服 vancomycin 治療無效或復發後,且細菌培養或毒素分析報告證實為 CDAD,並經感染症專科醫師會診確認,檢附會診紀錄及相關之病歷資料方能使用 fidaxomicin。
貳、CDAD藥物治療
針對 CDAD 的治療,常見的用藥為 metronidazole 或口服 vancomycin,然而約有25 %的病患會於治療後30天內經歷第一次復發,且對後續治療所衍生的醫療費用支出造成負擔,因此在藥物的選擇上必須重新審視6。
根據新版的困難梭狀桿菌感染治療指引,用藥選擇必須依照病情的嚴重程度以及是否為首次感染或屬於復發的情況,考量不同之治療方針2。
治療 CDAD 的主要用藥包括:metronidazole、口服 rifaximin、口服 vancomycin 及口服 fidaxomicin,以下為各個藥物的介紹。
一、Metronidazole
Metronidazole 是一種殺菌劑,可用於專一性厭氧菌感染,治療 CDAD 方面則屬於非適應症的用法,口服給藥途徑方便且健保價格便宜,治療療程所需的費用較少,雖然疾病治癒率較低且復發率高,目前在台灣使用於非重度之 CDAD 病患,建議劑量為口服500 mg,一天3次,治療10天,而腸阻塞的病人可視情況每8小時靜脈投予500 mg2,7。
常見的副作用包括噁心、嘔吐、腹瀉、眩暈、周邊神經病變及運動失調等8。此外,新版治療指引不建議延長或重複 metronidazole 的治療療程,因其神經毒性累積可能造成不可逆的傷害2。
二、Rifaximin
Rifaximin 是由 rifamycin 半合成的巨環類抗生素,美國食品藥物管理局 (簡稱 FDA) 核准用於旅行者腹瀉、腸躁症腹瀉以及肝性腦病變,而台灣目前尚無藥品使用許可證。其口服吸收率低,在大腸與糞便中藥物濃度高,復發之病患使用 vancomycin 後可接續投予 rifaximin 口服400 mg,一天3次,治療20天2。目前臨床上使用的經驗有限,仍需要更多研究來證實 rifaximin 治療困難梭狀桿菌感染復發的療效。
三、Vancomycin
Vancomycin 是第一個 FDA 核准用於治療 CDAD 的藥物,建議劑量為口服125 mg,一天4次,治療10天;若為猛爆型感染者,須使用500 mg一天4次,口服或直腸投予;而復發時,視情況給予漸減合併脈衝性療程 (tapered and pulsed regimen)。研究指出,其療效較 metronidazole 佳,尤其對於重度 CDAD 的病患,能降低死亡率 (adjusted risk difference: –0.04; 95% CI: –0.07 to –0.01)9。其缺點是治療後可能產生抗藥性菌株,如:抗萬古黴素腸球菌(vancomycin-resistant enterococcus,VRE)10。Vancomycin 目前只有針劑劑型,使用前須將所需劑量配製成30 mL 的溶液,方能口服投予11。口服身體可用率低,全身性副作用相對較少,一般以噁心、嘔吐、腹痛等較為常見5。
四、Fidaxomicin
Fidaxomicin 屬於巨環類抗生素,能抑制困難梭狀桿菌的 RNA
polymerase,使得細菌無法製造蛋白質而造成細胞凋亡,達到殺菌的效果,是近30多年來,FDA
核准用於治療成人 CDAD 的突破性新藥。
根據臨床文獻指出,fidaxomicin 療效不比 vancomycin
差,且疾病復發率較低,對於腸道內正常厭氧菌叢影響較小,針對芽孢梭菌屬的抑菌濃度較對大腸桿菌屬的抑菌濃度低20倍,顯示
fidaxomicin 治療 C. difficile
的專一性,且能抑制其孢子形成,被認為是降低疾病復發率的可能原因12,13。
藥物動力學方面,fidaxomicin 屬於局部作用的藥物,全身性吸收率極低,在直腸糞便中藥物濃度高。其主要代謝物 OP-1118為 P-醣蛋白 (P-glycoprotein;P-gp) 的受質,考量到藥物交互作用可能導致 fidaxomicin 體內濃度增加,因此不建議併用 P-glycoprotein 強效抑制劑 (如:cyclosporine)。投藥方式為口服200 mg,一天2次,治療10天,不須依據肝腎功能調整劑量,惟中重度肝腎功能不全的病人因臨床數據有限,使用上須謹慎小心,留意病患臨床反應。常見的副作用為:噁心、嘔吐、腹痛等12。
參、臨床試驗:治療效益及藥物安全性5
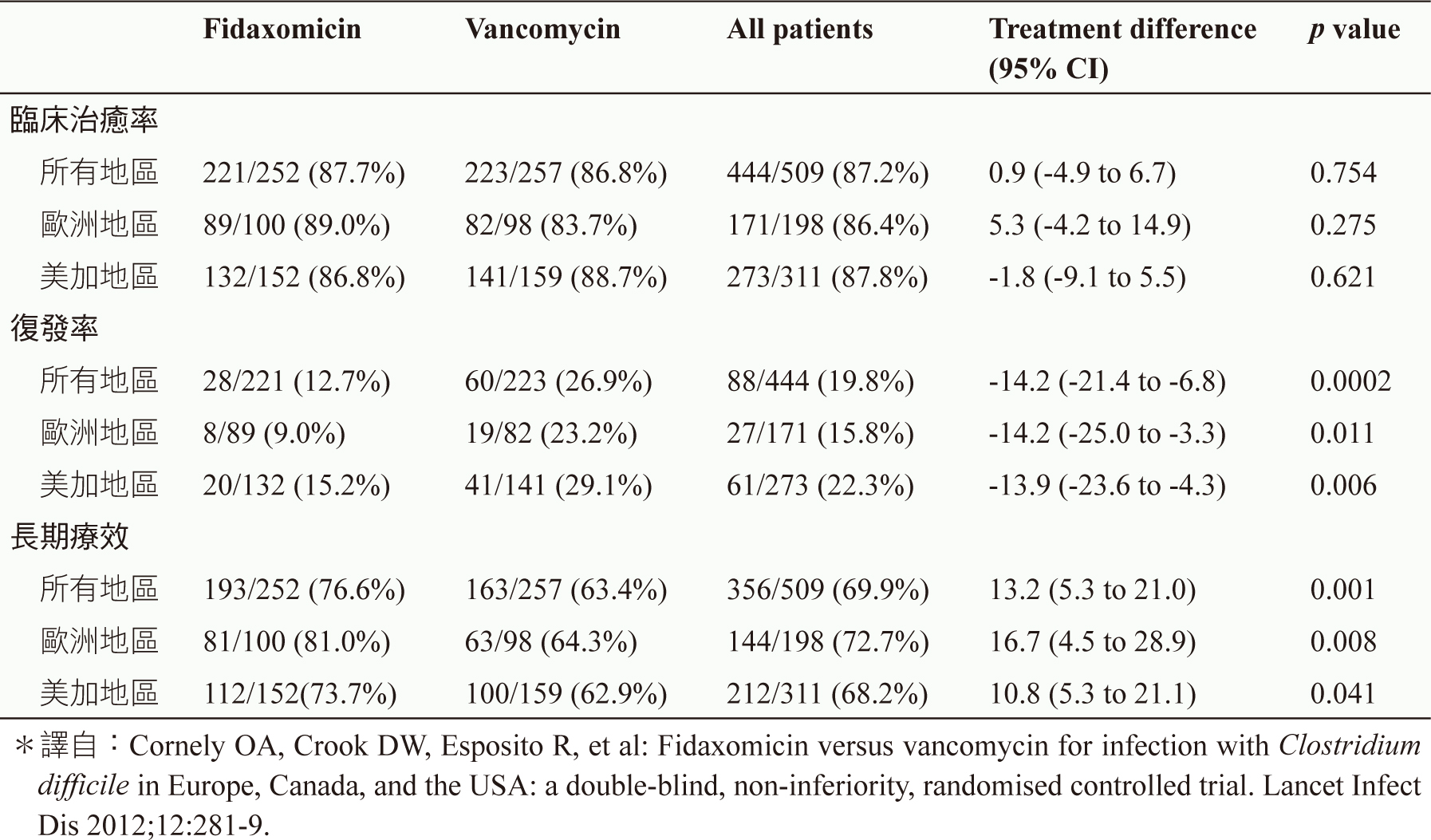
關於 fidaxomicin 的治療效益,在一篇多中心、前瞻性、雙盲且隨機分派的臨床試驗 (OPT-80-004) 中可證實,此試驗收納來自歐洲、美國及加拿大86個醫療院所共535位病人,並隨機分派至使用 fidaxomicin 組及使用 vancomycin 組。使用 fidaxomicin 組接受200 mg 每天2次治療,而 vancomycin 組則接受125 mg 每天4次治療,兩組療程皆為期10天。試驗結果顯示 (表一),在長期療效方面 (sustained response),達到腹瀉緩解且無復發的情況,fidaxomicin 組有較佳的成效 (改良式治療意向分析 [modified intention-to-treat;MITT],fidaxomicin 療效為76.6%,vancomycin 療效為63.4%[兩組治療差異為13.2%; 95% CI: 5.3%-21.0%,p = 0.001])。
藥物安全性方面,治療後出現的不良事件 (treatment-emergent adverse event;TEAE) 發生率在兩組之間沒有顯著差異,其中主要常見的不良事件是胃腸道症狀,如:噁心、嘔吐、腹瀉及腹痛。但由於試驗的收納族群已事先排除危及生命或猛爆型 C. difficile 感染 (白血球數 > 30x109/L、敗血性休克、體溫 > 40°C、低血壓 [收縮壓 < 90 mmHg]、腹膜感染症狀或嚴重脫水)、毒性巨結腸症、孕婦或哺乳婦女、在過去3個月內曾經發生 C. difficile 感染超過1次等,這些族群的療效及安全性尚未確立,有待更多試驗提供足夠的臨床證據。
表一 區域別的臨床治療結果 (改良式治療意向分析,modified intention-to-treat;MITT)5
肆、成人 CDAD 藥物治療指引2
IDSA 與 SHEA 於2017年更新困難梭狀桿菌感染之治療指引,摘要整理 (表二)。
表二 美國感染症醫學會 (IDSA) 與美國健康照護流行病學會 (SHEA) 制定成人困難梭狀桿菌感染建議治療指引(2017版)2
首次感染非重度 (non-severe) 或重度 (severe) 的病人,建議使用 vancomycin 口服125 mg,一天4次或 fidaxomicin 口服200 mg,一天2次,非重度的病人若無法使用上述兩種藥物時,則替代藥物為 metronidazole 口服500 mg,一天3次,治療療程皆為期10天。
而猛爆型的首次感染,意指病患伴隨低血壓、休克、腸阻塞或巨腸症,建議使用vancomycin 500 mg 口服或經鼻胃管給予,一天4次,若發生腸阻塞的狀況,則每6小時經直腸投予 vancomycin 500 mg/100 mL normal saline。此猛爆型感染者應同時靜脈投予metronidazole 500 mg,每8小時一次。
若為復發之 CDAD 病患,第一次復發時,若先前曾使用 metronidazole,則建議改以 vancomycin 口服125 mg,一天4次治療10天;若先前曾使用首次感染之標準治療療程,則建議改採用 vancomycin 漸減合併脈衝性療程 (tapered and pulsed regimen),即口服125 mg,一天4次,治療10-14天,而後投予頻次漸減成一天2次,療程7天,接著一天1次,治療7天,最後給予脈衝性治療,每2-3天投予1次,持續2-8週;若先前曾使用 vancomycin 標準治療療程,也可改採用 fidaxomicin 口服200 mg,一天2次,服用10天,作為治療的選擇。
當復發次數為2次 (含) 以上,有四種治療方式:(一)vancomycin 漸減合併脈衝性療程、(二)vancomycin 口服125 mg,一天4次,治療10天,接續給予 rifaximin 口服400 mg,一天3次,治療20天、(三)fidaxomicin 口服200 mg,一天2次,治療10天或(四)糞便微生物移植 (復發次數大於2次的病人才建議使用)。
伍、討論
由於抗生素廣泛的使用,造成困難梭狀桿菌感染的發生率升高,根據研究統計,台灣2003至2007年,大於65歲之老年人發生 C. difficile 感染事件增加5至6倍,此外,高復發率也是臨床上須考量的因素14,15。
隨著 IDSA/SHEA 所發表的最新治療指引,相較於先前的治療指引,fidaxomicin 成為藥物治療的新選擇,與 vancomycin 相比,除了具備較佳的長期療效外,藥物安全性方面並無太大的差異,此外,給藥頻率為一天2次,可增加其投藥方便性。雖然藥物費用方面,依照107年12月9日的健保價計算,每日治療藥費遠高於 vancomycin (fidaxomicin:4,388元/天;vancomycin 1 gm:239元/天,500 mg:87元/天),但以降低疾病復發率之層面而言,fidaxomicin 的使用或許在整體醫療費用支出較能符合經濟成本效益,這部分仍須更多藥物經濟學研究分析來加以佐證。
陸、結論
Fidaxomicin 為窄效性抗生素,可選擇性消滅 C. difficile,對其他大腸桿菌屬影響較小;除此之外,口服劑型方便給藥,對 CDAD 治癒率與 vancomycin 至少相當且有更低的復發率,因此 IDSA/SHEA 於最新版治療指引已將 fidaxomicin 並列為第一線選擇藥物之一。希望透過本文的介紹,增加醫療人員對於 CDAD 疾病以及治療藥物的了解,對往後臨床實務上能有所助益。
Update in the Treatment of Clostridium difficile-associated Diarrhea
Hsiao-Chun Wang, Hsin-Yi Chou, Shin-Tarng Deng,
Hsuan-Ling Hsiao
Department of Pharmacy, Chang Gung Memorial
Hospital, Linkou
Abstract
Clostridium difficile-associated diarrhea (CDAD) is a leading cause of hospital-associated gastrointestinal illness and places a high burden on our health-care systems. Metronidazole and oral vancomycin are recommended as first-line treatment. Fidaxomicin was approved by the US Food and Drug Administration (FDA) in 2011 for the treatment for adults with Clostridium difficile infection (CDI). The clinical cure rates of CDI for the treatment with fidaxomicin were noninferior to those for the treatment with vancomycin. Fidaxomicin was associated with a significantly lower recurrence rate of CDI as compared to those with vancomycin. Clinical practice guidelines for CDI were updated by the Infectious Diseases Society of America (IDSA) and Society for Healthcare Epidemiology of America (SHEA) in 2017. Either vancomycin or fidaxomicin is recommended as being superior to metronidazole for an initial episode of CDI. In this article, we will review the update in the treatment of CDAD and available data on fidaxomicin regarding the clinical place in therapy.
參考資料:
1. Eze P, Balsells E, Kyaw MH, et al: Risk factors for Clostridium difficile infections–an overview of the evidence base and challenges in data synthesis. J Glob Health 2017;7:010417.
2. McDonald LC, Gerding DN, Johnson S, et al: Clinical Practice Guidelines for Clostridium difficile Infection in Adults and Children: 2017 Update by the Infectious Diseases Society of America (IDSA) and Society for Healthcare Epidemiology of America (SHEA). Clin Infect Dis 2018;66:e1-e48.
3. Lee YC1, Wang JT, Chen AC, et al: Changing incidence and clinical manifestations of Clostridium difficile-associated diarrhea detected by combination of glutamate dehydrogenase and toxin assay in Northern Taiwan. J Microbiol Immunol Infect 2012;45:287-95.
4. Chung CH, Wu CJ, Lee HC, et al: Clostridium difficile Infection at a Medical Center in Southern Taiwan: Incidence, Clinical Features and Prognosis. J Microbiol Immunol Infect 2010;43:119–25
5. Cornely OA, Crook DW, Esposito R, et al: Fidaxomicin versus vancomycin for infection with Clostridium difficile in Europe, Canada, and the USA: a double-blind, non-inferiority, randomised controlled trial. Lancet Infect Dis 2012;12:281-9.
6. Kelly CP: Can we identify patients at high risk of recurrent Clostridium difficile infection? Clin Microbiol Infect 2012;18(Suppl 6):21-7.
7. Pepin J, Alary ME, Valiquette L, et al: Increasing risk of relapse after treatment of Clostridium difficile colitis in Quebec, Canada. Clin Infect Dis 2005;40:1591-7.
8. Metronidazole. In: IBM Micromedex® DRUGDEX® (electronic version). Available at: http://www.micromedexsolutions.com/ (accessed Dec 09, 2018)
9. Stevens VW, Nelson RE, Schwab-Daugherty EM, et al: Comparative Effectiveness of Vancomycin and Metronidazole for the Prevention of Recurrence and Death in Patients With Clostridium difficile Infection. JAMA Intern Med 2017;177:546-53.
10. Bartlett JG: Historical Perspectives on Studies of Clostridium difficile and C. difficile Infection. Clin Infect Dis 2008;46(Suppl 1):4-11.
11. Product Information: vancomycin hcl IV injection, vancomycin hcl IV injection. Abbott Laboratories, North Chicago, IL, 2003.
12. Product Information: DIFICID™, fidaxomicin. Optimer Pharmaceuticals, San Diego, CA, 2011.
13. Zhanel GG, Walkty AJ, Karlowsky JA: Fidaxomicin: A novel agent for the treatment of Clostridium difficile infection. Can J Infect Dis Med Microbiol 2015;26:305–12.
14. Bartlett JG: Narrative review: the new epidemic of Clostridium difficile-associated enteric disease. Ann Intern Med 2006;145:758-64.
15. Collins DA, Hawkey PM, Riley TV, et al: Epidemiology of Clostridium difficile infection in Asia. Antimicrob Resist Infect Control 2013;2:21.
通訊作者:王筱君/通訊地址:桃園市龜山區復興街5號
服務單位:林口長庚紀念醫院藥劑部藥師/聯絡電話:(O) 03-3281200 ext 2710