多重激酶抑制劑引起手足皮膚反應
劉錦鳳、楊璦瑜、陳彥文
高雄醫學大學附設中和紀念醫院藥學部
摘要
使用多重激酶抑制劑(Multitargeted Tyrosine Kinase Inhibitors, MTKIs)干擾腫瘤細胞生長時會出現副作用,從而降低病人的生活品質,進而導致停藥或中斷服藥。其中,手足皮膚反應(Hand-Foot Skin Reaction, HFSR)是最常見的皮膚不良反應。HFSR的特徵是紅斑、刺痛、過度角化和感覺異常,特別是在手掌和腳底。臨床研究顯示HFSR的發生可能與臨床反應效益及總生存率具相關性。本文將運用文獻回顧進行探討與比較。
關鍵字: 多重激酶抑制劑、手足皮膚反應、Hand-Foot Skin Reaction、Multitargeted Tyrosine Kinase Inhibitor
壹、前言
多重激酶抑制劑(Multitargeted Tyrosine Kinase Inhibitors, MTKIs)藉由抑制血管內皮生長因子受體(vascular endothelial growth factor receptor, VEGFR)下游的酪胺酸激酶(Tyrosine Kinase, TK),例如sorafenib、regorafenib、sunitinib等,已被證實可治療惡性腫瘤1,2。然而這類藥品因抑制VEGFR -TK的路徑可能發生藥物不良反應,影響病人的身體外觀、心理層面。其中手足皮膚反應(Hand-Foot Skin Reaction, HFSR)是MTKIs所引起最常見的皮膚不良反應。雖然少有致命的危險,但對病人的生活品質有很大的影響,可能需要減少使用劑量改善HFSR嚴重性,甚至須中止治療。HFSR的組織病理學與因細胞毒性化療藥品引起的手足症候群(Hand-Foot Syndro me, HFS)相似,但兩者的危險因子、臨床表徵有其差異2。本文將論述HFSR與HFS的差異性、HFSR的病理學,運用文獻回顧探討HFSR與腫瘤反應率(tumor response rate)、總生存率(overall survival rate)的相關性,並介紹HFSR預防與治療的相關事項,提供醫療人員臨床上的參考。
貳、HFSR和HFS之差異
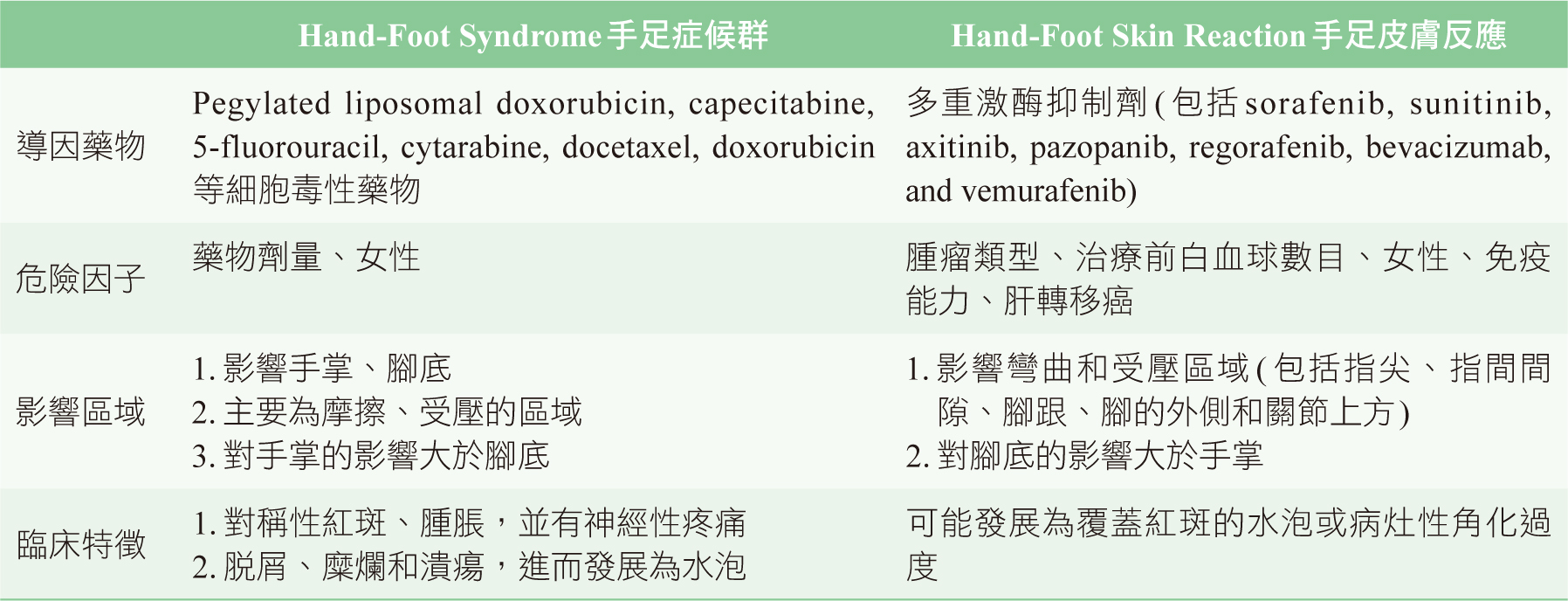
HFS也稱為肢端紅腫症(Palmar-Plantar Erythrodysesthesia, PPE),發生率6%~64%;HFSR發生率以sorafenib與sunitinib為例,分別為約10%~28%和10%~62%,研究結果差異性大,但因統計數據來源主要為病例系列文獻,難以準確評估。表一列出兩者的差異3。
表一 Hand-Foot Skin Reaction和Hand-Foot Syndrome比較表3
Common Terminology Criteria for Adverse Events (CTCAE) v5.0是美國國家癌症研究所用於評估癌症治療不良反應嚴重性的量表。HFSR不屬於CTCAE的類別,且目前沒有針對HFSR的嚴重度評估量表。HFS的分級可以用於HFSR,但須注意有其限制,如未評估病患對嚴重性的感受、HFSR的持續時間等2。
參、HFSR的病理學
HFSR一般在治療後1~6週內發生,先是手腳感覺異常,之後才出現疼痛、水腫、紅斑和角化病灶4。HFSR發生率與腫瘤型態有關,以及MTKIs彼此之間,若涉及不同分子途徑機轉,在臨床上就會有嚴重程度不同的副作用5。McLellan等人的研究提出不只與VEGFR下游受到阻斷有關,還可能與抑制血小板衍生之生長因子(Platelet-Derived Growth Factor Receptors, PDGFR)的路徑表現相關,目前支持此理論的MTKIs藥品有sorafenib、regorafenib和sunitinib1,5。
若MTKIs同時抑制VEGFR和PDGFR,會減弱上皮細胞的修復功能,更增加了HFSR的發生率與嚴重程度。但若只抑制PDGFR,例如imatinib是Bcr-Abl酪胺酸激酶抑制劑,為PDGFR的抑制劑,但無抑制VEGFR路徑,臨床上便沒有發現HFSR5,6產生。
肆、MTKIs抗腫瘤療效與HFSR的相關性
近年有研究顯示MTKIs抗腫瘤的效果可能與HFSR有相關性,包括sorafenib、regorafenib、pazopanib等2,以下運用文獻回顧探討:
一、 sorafenib
(一) Vincenzi等人評估sorafenib抗腫瘤的效果與HFSR的相關性。分析第一個月皮疹和HSFR的發生率,比較腫瘤控制和無疾病進展時間。結果顯示,有發生HFSR及無HFSR的腫瘤控制率分別為48.3%與19.4%,無疾病進展時間為8.1個月與4.0個月。研究建議須密切監測藥物皮膚毒性,因其可能是療效的替代指標7。
(二) Otsuka等人探討分子標靶藥物的毒性與癌症臨床療效的相關性。多變量分析中,皮膚毒性是重要的預後因素(危險比hazard ratio=0.522;95%信賴區間0.274-0.997)8。
(三) 2018年Wang等人針對sorafenib治療Hepatocellular carcinoma進行統合分析(meta-analysis),研究結果發現發生HFSR有顯著較佳的療效反應,是有意義的預測指標9。
二、 regorafenib
(一) 在法國進行的REBECCA(The REgorafeniB in mEtastatic Colorectal cancer: a French Compassionate program),研究發現開始治療的第一個月內發生HFSR的病人整體存活期(Overall Survival, OS)顯著較佳(HR 0.61,95% CI: 0.50-0.74)10。
(二) Kobayashi等人在日本進行的回顧性研究顯示,發生嚴重度較高的HFSR的病人有較佳的OS及無疾病惡化存活期(Progression-Free Survival, PFS)。研究結果推測,嚴重的HFSR可能是regorafenib療效的早期替代指標(early surrogate marker)4。
三、 pazopanib
Huang等人在台灣進行從HFSR,預測pazopanib在轉移性軟組織肉瘤的治療預後。多變量分析顯示,HFSR的發生是預後較佳的獨立影響因素(independent factors)11。
伍、HFSR與藥物累積劑量、藥物依順性
口服標靶藥物在癌症治療的使用上愈來愈普及,藥物的副作用經常會影響服藥依順性(drug adherence),建議有醫療人員介入。2018年日本學者進行的回顧性研究,在使用sorafenib治療Hepatocellular carcinoma期間,比較有無藥師介入對治療依順性、治療預後的影響。由專責癌症治療的藥師成立藥師門診,在病人回診前進行副作用評估、教導副作用的處置及剩餘藥物的相關議題。在病人看診時將匯整資訊提供給診間,醫師再根據病人狀況開立處方。研究結果顯示,有藥師的介入可以增加病人服藥依順性,病人服藥時間延長,藥物累積劑量增加,存活時間延長12。
陸、HFSR的預防與改善措施2,5
根據病人的症狀嚴重度,給予個別化的日常生活建議。MTKIs開始治療前可衛教病人採取預防措施:
一、使用溫和的潤膚劑或局部尿素基底乳霜,保持手和腳的皮膚濕潤。
二、避免劇烈運動(特別是在治療的第一個月),因為會對手掌或腳底帶來過大的壓力。
三、建議穿著有鞋墊的鞋子,以減少腳部壓力;戴厚棉手套或穿襪子,以防止受傷。
四、避免將手和腳浸泡於熱水中,會惡化症狀。
若已發生HFSR,提供支持性治療的藥物:
一、使用含10%尿素成份的乳膏,以軟化過度角質化的部位。
二、類固醇藥膏減輕皮膚發炎症狀。
三、局部鎮痛藥,緩解疼痛,更嚴重時使用全身性止痛藥。
柒、結論
目前尚無文獻證實那些特性的病人使用MTKIs會出現HFSR,臨床研究發現HFSR可能與存活率有關聯性。然而藥物的副作用經常會影響病人依順性,停藥會影響治療的效果。希望藉由醫療人員介入,以支持療法改善症狀,提升服藥順從性,服藥時間延長,藥物累積劑量增加,延長病人存活時間。
Multitargeted Tyrosine Kinase Inhibitors Induced Hand-Foot Skin Reaction
Chin-Feng Liu, Ai-Yu Yang, Yen-Wen Chen
Department of Pharmacy, Kaohsiung Medical
University Hospital,
Kaohsiung Medical University
Abstract
Using multitargeted tyrosine kinase inhibitors(MTKIs) may cause side effects, which will reduce the patient's quality of life, and stop or interrupt the treatment. Hand-foot skin reaction(HFSR) is the most common cutaneous adverse event caused by MTKIs. HFSR is characterized by erythema, tingling, focal hyperkeratosis and dysesthesia, particularly on the palms and soles. The studies have showed an association between the occur of HFSR and increased tumor response rate and overall survival rate. Therefore, this paper reviewed literatures with about these clinical issues, made a discussion and comparison.
參考資料:
1. Massey PR, Okman JS, Wilkerson J, et al: Tyrosine kinase inhibitors directed against the vascular endothelial growth factor receptor (VEGFR) have distinct cutaneous toxicity profiles: a meta-analysis and review of the literature. Support Care Cancer 2015;23(6):1827-35.
2. Hand-foot skin reaction induced by multitargeted tyrosine kinase inhibitors. [uptodate] Literature review current through: Nov 2019. This topic last updated: Jul 01.2019.
3. Miller KK, Gorcey L, McLellan BN. Chemotherapy-induced hand-foot syndrome and nail changes: a review of clinical presentation, etiology, pathogenesis, and management. J Am Acad Dermatol 2014;71(4):787-94.
4. Kobayashi K, Kawakami K, Yokokawa T, et al: Association of Hand-Foot Skin Reaction with Regorafenib Efficacy in the Treatment of Metastatic Colorectal Cancer. Oncology. 2019;96(4):200-206.
5. McLellan B, Ciardiello F, Lacouture ME, et al: Regorafenib-associated hand-foot skin reaction: practical advice on diagnosis, prevention, and management. Ann Oncol. 2015 Oct;26(10):2017-26.
6. Nonomiya Y, Yokokawa T, Kawakami K, et al: Regorafenib-Induced Hand-Foot Skin Reaction Is More Severe on the Feet Than on the Hands. Oncol Res. 2019 May 7;27(5):551-556.
7. Vincenzi B, Santini D, Russo A, et al: Early skin toxicity as a predictive factor for tumor control in hepatocellular carcinoma patients treated with sorafenib. Oncologist 2010;15(1):85-92.
8. Otsuka T, Eguchi Y, Kawazoe S, et al: Skin toxicities and survival in advanced hepatocellular carcinoma patients treated with sorafenib. Hepatol Res 2012;42(9):879-86.
9. Wang P, Tan G, Zhu M, et al: Hand-foot skin reaction is a beneficial indicator of sorafenib therapy for patients with hepatocellular carcinoma: a systemic review and meta-analysis. Expert Rev Gastroenterol Hepatol 2018;12(1):1-8.
10. Adenis A, de la Fouchardiere C, Paule B, et al: Survival, safety, and prognostic factors for outcome with Regorafenib in patients with metastatic colorectal cancer refractory to standard therapies: results from a multicenter study (REBECCA) nested within a compassionate use program. BMC Cancer. 2016 Jul 7;16:412.
11. Huang PW, Chou WC, Shen WC, et al: Hand-foot skin reaction predicts treatment outcome of pazopanib in patients with metastatic soft tissue sarcoma: A multicenter study in the Asian population. Asia Pac J Clin Oncol 2018;14(4):353-360.
12. Ochi M, Kamoshida T, Ohkawara A, et al: Multikinase inhibitor-associated hand-foot skin reaction as a predictor of outcomes in patients with hepatocellular carcinoma treated with sorafenib. World J Gastroenterol 2018;24(28):3155-3162.
通訊作者:劉錦鳳/通訊地址:高雄市三民區自由一路100號 高雄醫學大學附設中和紀念醫院藥學部
服務單位:高雄醫學大學附設中和紀念醫院藥學部/聯絡電話:(O) 07-3121101 ext
7173、7175