壹、前言
巴金森氏病(Parkinson's disease)是一種進行性的神經退化性疾病,發病年齡多在50-70歲左右。肇因於腦部協調運動的多巴胺(dopamine)神經元細胞退化,進而有肢體顫抖、僵硬、動作緩慢與身體不平衡等症狀。早在1817年,英國內科醫師James Parkinson首次發表文獻詳細描述此病症表現後,相同的病例就陸續被發表論述。美國的統計顯示此疾病約占六十歲以上老年人口的1%,台灣的資料顯示盛行率為130.1/100,000,發生率為10.4/100,0001。
貳、病理學
巴金森氏病在組織病理上的一大特徵就是在大腦中的黑質緻密部(substantia nigra pars compacta, SNc)的多巴胺神經元產生退化、腦幹細胞核的色素沈著,以及在黑質緻密部殘存的神經元表現出路易體(Lewy body, LB)。然而巴金森氏病所見的神經元喪失並不僅止於腦中,其他存在於自主神經節(autonomic ganglia)、基底核(basal ganglia)、脊椎以及新皮質(neocortex)的神經元也都有所損傷2。
黑質的多巴胺神經元發出的神經傳導路徑由基底核、丘腦等數個傳遞站最後到達大腦皮質控制正常的運動,當黑質的神經元細胞退化無法正常生產多巴胺時,應輸送到控制運動和平衡的紋狀體(striatum)之多巴胺逐漸減少,多巴胺和乙醯膽鹼(acetycholine)兩種神經傳導素無法維持平衡,巴金森氏病的運動障礙症狀因此而出現。而臨床症候是在細胞逐漸凋亡70%至80%以上才會出現3,這樣的病理所見是巴金森氏病的特點,其他疾病或是老化無此表現。至於何種機制引起多巴胺神經細胞凋亡,目前仍無定論,但認為和氧化壓力、發炎反應(inflammation)、粒腺體功能障礙、一氧化氮中毒或細胞自噬(autophagic cellular mechanisms)等有關聯。
參、診斷及表現
巴金森氏病的診斷須靠臨床診斷,其核心的症狀有:動作緩慢(bradykinesia)、靜態性顫抖(resting tremor)與肢體僵硬(rigidity),步態不穩(postural abnormality)亦是核心症狀,但通常較晚發生。巴金森氏病的病情因人而異,依臨床表現可分期別(表一)4,期別與症狀有關,與時間無關,病患可能在幾年之內進展數期,也可能數年維持在同一期。
肆、藥物治療
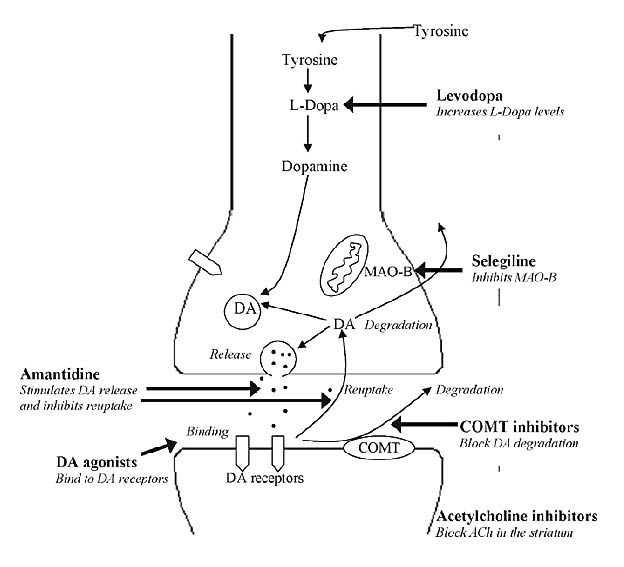
針對巴金森氏病,目前已有多種藥物可供使用,然而都只能做到改善症狀,無法抑止巴金森氏病的病程進展。藥物治療的時機仍有爭議,有些神經科醫師認為應及早治療,有些認為當症狀已經令病患困擾時才用藥,目前巴金森氏病的治療藥物有以下幾類(表二),相關的作用位置如圖一5:
一、Levodopa
Levodopa為多巴胺的前驅物(precursor),可經由L-aromatic amino acid decarboxylase酵素催化而轉變成多巴胺,於1960年代發展至今仍是巴金森氏病最有效的症狀改善藥物6。由於腦部有所謂的血腦障壁,而多巴胺本身無法通過此屏障,只有levodopa才可以穿過血腦障壁形成多巴胺,為了防止levodopa在進入大腦內之前就被decarboxylase 轉化成多巴胺,一般常和decarboxylase抑制劑併用,使更多的levodopa到達腦部,這些decarboxylase抑制劑本身不會通過血腦屏障,所以不會影響levodopa在中樞神經的代謝。市面常用製劑有Sinemet®(levodopa + carbidopa)或Modopar®(levodopa + benserazide)。
長期使用levodopa容易造成巴金森氏病患者產生多種運動性併發症(motor complication),最常見的是藥效一消失,病患的運動功能就立即消失無法移動肢體(end-of-dose “wearing off”)和藥效高峰期時產生的異動症(dyskinesias),如運動不協調、痙攣或不規則笨拙動作7。當巴金森氏病患者出現運動功能障礙(如顫抖、僵硬或動作緩慢)時,稱之為“off”期;反之,運動功能正常協調時,稱之為“on”期。患者隨著levodopa的使用及病程的惡化出現“on-off”的運動波動(motor fluctuations)現象會逐漸增加,有些病人甚至在使用levodopa治療5-6月後就發生這種現象8,主要是因為SNc的神經元慢慢退化,內生性多巴胺的儲存量及合成量越來越少,患者變得更依賴外來補充的levodopa,而levodopa的半衰期短,約為1小時,與carbidopa或benserazide併用可延長為1.5小時,但當levodopa藥效一過患者就會有“off”的狀況。為了減少病人出現“off”期,增加“on”期的時間,除了增加levodopa-carbidopa/benserazide的服用頻率,還可以併服monoamine oxidase-B(MAO-B)或catechol-O-methyltransferase(COMT)抑制劑來延長levodopa的作用時間9,或者併用多巴胺致效劑(dopamine agonist)來緩解“off”狀態。當病人胃排空的速率變慢,會使得levodopa到達小腸的時間較慢,而延遲藥物吸收的時間,造成藥效延遲(delayed-on)或者沒反應(no-on)的狀況,因此會建議病人空腹服藥,或改用口含錠劑型,避免使用長效緩釋劑型來改善症狀的發生。“on”期發生的異動症通常是因為多巴胺量高造成神經傳導過度刺激而產生的不自主運動,所以可以適度的降低levodopa的劑量或併用amantadine來緩解腦中樞過度刺激的現象。
二、MAO-B抑制劑
MAO-B抑制劑可以阻礙大腦中的多巴胺被分解,與levodopa併用可以降低levodopa的用量並延長levodopa的作用時間,減少“off”的時間10。目前美國FDA核准的MAO-B抑制劑有selegiline及rasagiline。
Selegiline經衛生署所通過的藥品許可証核淮之適應症僅為“巴金森病症之輔助治療劑”, 但有些研究顯示selegiline不管是巴金森氏病的早期或晚期皆有幫助,所以仍然很多學者建議當巴金森氏病早期仍不須使用levodopa時,selegiline可作為症狀治療來延緩需要使用levodopa的時間或降低levodopa劑量的需求。
Rasagiline為第二代的MAO-B抑制劑,2006年5月美國核准用於早期巴金森氏病之起始單一治療,或和levodopa併用治療中期和晚期巴金森氏病患者,減少藥效波動,目前台灣仍未核准上市。
有研究主張MAO-B抑制劑因阻礙多巴胺的氧化代謝可以減少氧化自由基(oxygen free radical)對神經細胞的傷害,但目前仍無足夠證據來支持MAO-B抑制劑對巴金森氏病患者具有神經保護作用。
三、COMT抑制劑
目前臨床上使用之COMT抑制劑有entacapone和tolcapone,能藉由抑制COMT酵素阻礙levodopa被分解代謝,進而提高levodopa的生體可用率,增加並延長腦中levodopa的數量和效用9。COMT抑制劑單獨使用對於巴金森氏病並無療效,必需和levodopa併用才具臨床效果。
服用tolcapone有嚴重肝毒性的副作用11,因此開始服藥六個月內病人需定期監測肝功能,目前並未在台灣核准上市。為了增加病人服藥的順從性,台灣目前有levodopa+carbidopa+entacapone的三合一製劑以方便控制巴金森氏病之運動波動。
四、多巴胺致效劑
多巴胺致效劑的結構類似多巴胺,它不用經過腦細胞轉化,主要是透過直接刺激大腦內的多巴胺接受器(dopamine receptor),增加神經訊號的傳送,以代替腦部分泌不足的多巴胺來治療巴金森氏病。可以用於早期巴金森氏病之單一治療,延緩需要使用levodopa的時間,或者和levodopa併用治療中期和晚期巴金森氏病患者6。
治療藥物分為兩類,一是非麥角類(non-ergot)衍生物(如:pramipexole、ropinirole),其藥物安全性及療效較佳;另一為麥角類(ergot)衍生物(如:bromocriptine、pergolide),因副作用大,臨床使用受到限制,bromocriptine有造成肺部纖維化的風險而且療效不如其他致效劑12,pergolide因有造成心瓣膜損害的危險13,美國已於2007年3月回收下市,台灣衛生署目前仍在評估中。
五、抗乙醯膽鹼劑(anticholinergics)
抗乙醯膽鹼劑是最早被用來治療巴金森氏症的藥物,它會阻擾化學神經傳導物質-乙醯膽鹼的作用,以維持紋狀體內乙醯膽鹼和多巴胺的平衡。這類藥物可以改善病人顫抖、肌肉僵硬的症狀,以及加強巴金森氏病患者對肌肉的控制6。但因為有口乾、便秘、小便失禁、視力模糊、失憶、錯亂等副作用,如果有其他藥物可取代,年老的患者通常不使用這類藥物。
六、Amantadine
Amantadine為抗病毒藥物,臨床上發現它對巴金森氏病是有助益的,尤其是抑制levodpa引起的異動症9,而真正的作用機轉仍不清楚,可能是作用在黑質體細胞上,促進殘存於神經末梢內的多巴胺釋放,減少多巴胺在神經突觸末端的回收,並提升多巴胺接受器的活性,使患者的症狀得以緩解。
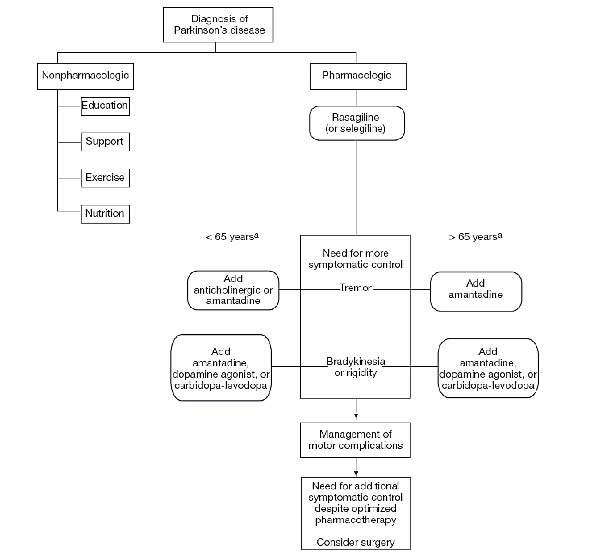
在藥物治療上(圖二)14,初期病人還沒有太多症狀產生時,可使用MAO-B抑制劑,如果病人年紀較輕亦可考慮使用巴多胺致效劑。而嚴重症狀出現時,可加入levodopa,在levodopa使用之後如果出現藥效波動,應考慮加上COMT抑制劑來延長levodopa的作用時間或者是加入MAO-B抑制劑。病人服用levodopa期間若有異動症的發生,可併加amantadine來改善。基本上,巴金森氏病的治療目標主要是維持日常的生活能力,而不是想要消除所有的症狀。為了監測評估巴金森氏病藥物治療的效果,下列幾點應告知病人或病患家屬:(1)監測病人藥物服用時間:Sinemet®或Modopar®最好空腹服用,如果發生胃腸不良反應,可併用一點流質食物或小點心。Selegiline不宜於晚上服用以免造成失眠。(2)讓病人或照顧者了解處方藥物的用法與目的:例如COMT抑制劑需與levodopa併服才有療效,不可作為單一治療劑。(3)監測服藥後可能發生的不良反應:例如異動症、妄想、失憶、情緒改變、失眠等症狀,並和醫師討論改善方案。(4)監測病人是否有使用其它加速病情惡化的藥物:例如多巴胺阻斷劑。(5)監測藥物使用後的症狀反應,以便有效的調整治療藥物或使用劑量。
伍、結論
腦部的運動控制系統極為複雜,我們必需了解任何一種巴金森氏病藥物都只能對運動障礙達到部分的改進。藥物治療只能補充患者體內多巴胺濃度之不足,無法抑制退化的持續進行。因此,何時開始藥物治療、如何調整藥物的使用劑量、何時併用輔助治療劑來減少副作用的發生,以維持長期良好的症狀控制是巴金森氏病藥物治療最大的挑戰。由於每一位患者病情的變化不盡相同,巴金森氏病的治療是因人而異的,需要根據患者罹病年齡、發生的運動障礙,尤其是認知能力的狀況來決定。
參考資料:
1. Chen RC, Chang SF, Su CL et al: Prevalence, incidence, and mortality of PD: A door-to-door survey in Ilan County, Taiwan. Neurology 2001; 57: 1670-86.
2. Braak H, Del Tredici K, Rub U et al: Staging of brain pathology related to sporadic Parkinson's disease. Neurobiol Aging 2003; 24: 197-211.
3. Bernheimer H, Birkmayer W, Hornykiewicz O et al: Brain dopamine and the syndrome of Parkinson's and Huntington: clinical, morphological, and neurochemical correlations. J Neurol Sci 1973; 20: 415-55.
4. Hoehn MM, Yahr MD: Parkinsonism: onset, progression, and mortality. Neurology 1967; 17: 427.
5. Singh N, Pillay V, Choonara YE: Advances in the treatment of Parkinson's disease. Prog Neurobiol 2007; 81: 29-44.
6. Movement Disorders Society: Management of Parkinson's disease: an evidence-based review. Mov Disord 2002; 17(suppl4): S1-166.
7. Hauser RA, McDermott MP, Messing S: Factors associated with the development of motor fluctuations and dyskinesias in Parkinson disease. Arch Neurol 2006; 63: 1756-60.
8. Parkinson Study Group: Levodopa and the progression of Parkinson's disease. N Engl J Med 2004; 351: 2498-508.
9. Pahwa R, Factor SA, Lyons KE et al: Practice Parameter: treatment of Parkinson disease with motor fluctuations and dyskinesia (an evidence-based review): report of the Quality Standards Subcommittee of the American Academy of Neurology. Neurology 2006; 66: 983-95.
10. Fernandez HH, Chen JJ: Monoamine oxidase-B inhibition in the treatment of Parkinson's disease. Pharmacotherapy 2007; 27: 174S-185S.
11. Assal F, Spahr L, Hadengue A et al: Tolcapone and fulminant hepatitis. Lancet 1998; 352: 958.
12. McElvaney NG, Wilcox PG, Churg A et al: Pleuropulmonary disease during bromocriptine treatment of Parkinson's disease. Arch Intern Med 1988; 148: 2231-6.
13. Zanettini R, Antonini A, Gatto G et al: Valvular heart disease and the use of dopamine agonists for Parkinson's disease. N Engl J Med 2007; 356: 39-46.
14. Chen JJ, Swope DM: Pharmacotherapy for Parkinson's disease. Pharmacotherapy 2007; 27: 161S-173S.
表一 巴金森氏病的分期
期 別 |
重點描述 |
第一期 |
症狀限於身體一側 |
第二期 |
症狀及於身體兩側,姿勢平穩 |
第三期 |
平衡受損,容易跌倒 |
第四期 |
需要扶持方能走路,且出現其他嚴重症狀 |
第五期 |
須使用輪椅或終日臥床 |
表二 巴金森氏病的治療藥物(台灣核准上市)
藥物 |
使用劑量(天) |
副作用 |
Amantadine |
100-300 mg |
口乾、皮膚斑點、幻覺、姿態性低血壓、腳腫脹 |
Anticholinergics Biperiden Trihexyphenidyl |
1-4 mg bid-qid 6-15 mg divided tid-bid |
口乾、便秘、小便困難、視覺模糊、意識錯亂 |
Dopaminergics Carbidopa-levodopa Benserazide-levodopa Carbidopa-levodopa-entacapone |
75/300-500/2000 mg divided tid-qid 75/300-200/800 mg divided tid-qid max: entacapone 2000 mg |
噁心、口乾、便秘、姿態性低血壓、昏眩、情緒不穩、幻覺、妄想、異動症和藥效波動 |
Dopamine Agonists Bromocriptine Pergolide Pramipexole Ropinirole |
10-40 mg divided tid 1-4 mg divided tid 1.5-4.5 mg divided tid 3-12 mg divided tid |
反胃、口乾、姿態性低血壓、昏眩、幻覺、 |
COMT inhibitors Entacapone |
200-2000 mg |
反胃、腹瀉、異動症、皮膚膚色及尿液顏色變黃 |
MAO-B inhibitors Selegiline |
5-10 mg |
失眠、口乾、便秘、姿態性低血壓、昏眩、情緒不穩、異動症 |
圖一 巴金森氏病治療藥物的作用位置
圖二 巴金森氏病的處理原則