摘要
巴拉刈為農業上常用的除草劑,致死劑量低、毒性強且無特定解毒劑。中毒後除給予標準支持療法外,治療策略以減緩吸收、促進排出和降低對器官傷害為目標。減緩吸收,為清潔接觸的到皮膚和給予鼻胃管灌洗,降低全身性吸收;促進排出,以活性碳做為吸附劑的血液灌注效果較佳,血液透析適用於急性腎衰竭的患者;降低器官傷害,證據較多的為使用 cyclophosphamide 每天1克使用2天加上 methylprednisolone 每天1克使用3天,之後採 dexamethasone 的維持治療為主,而其他抗氧化的藥物治療療效並不顯著。
關鍵字: 巴拉刈、吸附劑、血液灌注、cyclophosphamide、類固醇
壹、前言
巴拉刈為四級胺的水溶性除草劑,1962年上市後廣泛用於農業,國內多以24%流通,如速草淨、全草滅、草蕪松…等,外觀呈現藍綠色或褐色,略帶阿摩尼亞味。除草效果快且強效,會被土壤中的細菌分解不易殘留,正確地使用不會對操作者及環境產生不良影響,為應用上的優點。但巴拉刈毒性強,口服低劑量 (未稀釋10 mL) 即會造成不可復原的傷害,且無有效解毒劑,因此在國內列入劇毒農藥管理,對於購買者有身分上限制及流向管制。
貳、巴拉刈中毒機轉與診斷
人類中毒的機轉和應用於植物的除草機轉是一致的,主要藉由干擾細胞內電子傳遞鏈,抑制光合作用中 nicotinamide adenine dinucleotide phosphate (NADP) 還原,造成氧分子形成O2-和自由基,破壞細胞膜及胞器,造成死亡。當體內不斷有自由基形成和破壞性的氧化發生時,會引發更多的發炎細胞,造成多重器官傷害1,2。
巴拉刈中毒診斷可經由測定血液及尿液濃度加以確診。血中濃度和患者的預後有絕對相關性,可依服用後時間跟血中濃度預估其存活率3,如圖一所示,但在執行上容易受到設備的限制。尿液檢測則是迅速診斷的利器,將低亞硫酸鈉加入尿液中顏色由黃轉藍 (顏色越深表是體內濃度越高) 即表示中毒。
參、臨床毒性症狀
巴拉刈服後只有5-10%會被吸收,但吸收速度快,0.5至2小時內會達血液中最高濃度,5至7小時會在肺臟中會達到最高濃度,並極易分佈到肺、肝、腎、肌肉中及深層組織中。90%的巴拉刈會在12至24小時內以原型由腎臟排出,但嚴重中毒且中毒時間超過24小時的患者,因腎清除率顯著下降,需要數天至數星期才能排除已分佈到深層組織中之巴拉刈1。皮膚吸收程度與皮膚完整性有關,受損的皮膚將會增加吸收量。
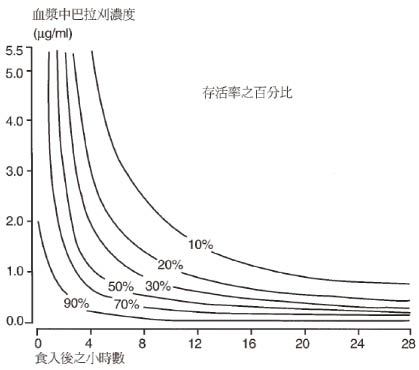
圖一 巴拉刈中毒存活率估測4
中毒的臨床特徵和暴露量有相當的關係,可區分為猛烈中毒、重度及輕度中毒。猛烈中毒為口服劑量超過每公斤40 mg,數小時或幾天後將因多重器官衰竭致命;重度中毒為口服劑量介於每公斤20-40 mg,會有急性腎衰竭和肺臟損傷,2-3周內死於呼吸衰竭;輕度中毒,口服劑量小於每公斤20 mg,輕微的腸胃道傷害為主要表徵,通常是可恢復的。巴拉刈對各器官或系統毒性影響如下所述。
1.皮膚:皮膚的暴露接觸,會造成紅疹,易脆的指甲和黏膜潰瘍導致鼻出血。2.眼睛:眼睛的暴露會造成結膜的潰瘍損傷。3.腸胃道系統:腸胃道主要急性症狀源自於巴拉刈的腐蝕性,會造成黏膜潰瘍受傷。口腔、舌頭、舌咽和胃部的黏膜受損,會在數天內發生,影響病人進食,嚴重的腸胃道潰瘍可能進一步造成穿孔和出血的風險。4.肺臟:為巴拉刈中毒主要影響的器官,毒性物質累積在肺臟,會損害肺臟細胞,降低氣體交換能力和影響呼吸功能。肺水腫在服用後2天內發生,緊接著肺部細胞腫脹、空泡化,且內質網和粒線體被破壞後,進展到充滿單核前纖維母細胞 (monounclear profibroblasts) 的增生期,最終導致不可逆的肺纖維化。此過程若進展快速,將在5星期後因至肺纖維化而死亡。5.腎臟:腎臟功能損傷雖然是可逆的,但近端腎小管功能損傷、近曲小管空泡化導致壞死、腎小球變性和腎小管上皮細胞壞死,亦可能導致在服用後2~6天內發生腎衰竭,且進一步抑制巴拉刈的排除。6.肝臟:服用後數小時到數天內,肝細胞也會因為內質網和粒線體的損傷,造成肝細胞腫脹壞死。臨床上可見黃疸、肝指數上升、肝腫大或急性胰臟炎。
肆、治療
巴拉刈中毒無專一性的解毒劑,有效的治療資料相當有限,所以治療除支持療法外,將會以減緩吸收、促進排出和降低對器官傷害為目標。
一、支持療法
每位經診斷中毒的患者,應給予標準支持療法包括:(一) 維持呼吸道暢通,受到黏膜毒性及嘔吐物影響,會造成呼吸道阻塞;(二) 血氧監測,動脈氣體分析及X光可輔助診斷,肺部損傷及代謝性酸中毒造成的低血氧。輕到中度的低血氧不建議常規供給氧,可能會增加氧化壓力導致死亡率上升,但應保持在 PaO2 大於50 mmHg 或 SaO2大於80%;(三) 血壓維持,低容積造成的低血壓可經輸液灌注及血管加壓劑獲得改善,但若腎功能惡化需密切監測體液的平衡1。
二、減緩吸收
若有皮膚接觸,應除去被汙染的衣物,進行身體清洗。在病人食入巴拉刈一小時內可使用吸附劑 (活性碳、矽藻土類或離子交換樹脂) 進行胃部灌洗1,但此方法的效用目前仍未被有效定義。若發現患者已有口腔或食道潰瘍,建議放置鼻胃管後再執行。
三、促進體內排出
使用利尿劑,促進巴拉刈由血中排除是無效的,因此不建議使用強效利尿劑。目標應該著重於維持正常腎功能,因當腎功能下降,會降低排除,進而增加在肺臟及其它深部器官的沉積2。身體外部移除 (extracorporeal removal) 可包含腹膜透析、血液透析、持續性血液過濾、血液灌注。腹膜透析,移除體內巴拉刈的量少不建議使用;血液透析,有成功案例,但於高濃度 (大於每小時10 mg) 時效果較好,低濃度移除效果不佳,效過劣於血液灌注,但急性腎衰竭患者可考慮使用1,2;持續性血液過濾,有少數案例使用,效果不確定;血液灌注,會使用活性碳做為吸附劑,低濃度仍有清除力,是目前較有效且臨床上常用的方法,若尿液中巴拉液濃度大於5 ppm (百萬分之一) 建議在24小時內開始第一個8小時療程 (越早使用效果越好),若超過24小時,已分佈到深層組織,清除效果不佳,在血液灌注後,會有再次分佈效應,血中濃度會反彈性升高,因此四小時後須再追蹤尿液巴拉刈濃度,評估是否需要再進行下一個療程。但亦有學者提出,開始透析的時間才是影響預後最重要的決定因子,其次才是透析方式1。
四、降低對器官的傷害
此部分治療理論為,減少氧化壓力造成肺部及其他器官損傷,可分為藥物和非藥物治療。
(一)藥物治療
1.免疫抑制劑:
免疫系統的調節在巴拉刈導致的肺纖維化中扮演重要角色,許多免疫抑制劑皆曾使用於巴拉刈中毒的治療,但目前僅有 cyclophosphamide 和類固醇 (methylprednisolon 或 dexamethasone) 的合併治療,在臨床上正面證據較多 (參閱表一,以關鍵字– steroids [Mesh]、cyclophosphamide 和 paraquat,並限制於人類和英文相關文獻檢索後共獲15篇,最後擷取有相互對照組下之參考文獻5篇),而其他藥物於巴拉刈中毒治療上皆無顯著角色。Cyclophosphamide 透過免疫調節,降低發炎反應,以延緩肺部的損傷,而類固醇則以抑制過氧化物的產生,增加 P-glycoprotein 反應,降低巴拉刈在肺部的累積。另外 cyclophosphamide 因可能導致白血球減少症,以致有助於延緩肺部纖維化發生。
在1986年 Addo 將此合併療法 (cyclophosphamide 和類固醇) 用於治療巴拉刈中毒患者5,發現有75%的存活率。雖然之後有研究發現,該合併療法對於死亡率改善效果不明顯6,引起大家對於合併療法治療效果的疑慮。但後續的研究皆顯示合併療法可以減少死亡率7-9,即使中毒後14天才給藥,也可能可改善預後10。
類固醇可抑制過氧化物產生發炎物質,因此有學者在完成合併療法治療後,給予維持劑量類固醇,並將 PaO2 保持在 80 mmHg 以上以改善預後11,或當 PaO2 小於 60 mmHg 時,再給予一次脈衝治療 (pulse therapy) 降低死亡率12。
在統合分析亦發現,於中重度中毒患者使用 cyclophosphamide 和類固醇的治療可以顯著降低死亡率 (相對風險比0.72,95%信賴區間為0.59-0.89)13。目前臨床上在傳統腸胃灌洗和血液灌注後,會給予 cyclophosphamide 每天1 g 連續2天和 methylprednisolon 每天1 g 連續3天,也和實證結果相符13。
2.抗氧化劑、螯合劑:
抗氧化劑,例如維他命C,維他命E和 acetylcyctine,用於治療巴拉刈中毒主要是依據體外試驗及動物模式,目前療效尚不確定1。
(二)非藥物治療
非藥物治療包含,放射線治療、一氧化氮、肺臟移植…等。使用低劑量放射線治療,原理為抑制纖維母細胞的增生,僅有少數成功個案,尚有爭議2。一氧化氮,有個案報告顯示,可短暫改善動脈的氧和能力,但在停止使用後,有大量肋膜滲液產生,且進一步惡化導致死亡,目前治療角色未被定論2。肺臟移植,並無成功案例,因巴拉刈造成肌肉損傷,導致患者依賴呼吸器,而死於肺炎。以上方法,皆因病例數有限,效果不確定,故目前臨床上鮮少使用2。
伍、結論
巴拉刈中毒會造成嚴重生理傷害,影響黏膜、腎、肝、肺臟等器官,最終導致多重器官衰竭而死亡,但大多數巴拉刈中毒皆為蓄意事件,因此應同時關懷病人身心狀況,避免不幸事件的重演,防治策略於此也有不可忽略的重要性。此外,醫療人員應具備相關急救知識和敏銳觀察力,在緊急狀況能採取適切的治療措施,於支持療法使用後,以活性碳進行胃灌洗避免過度吸收,進行含活性碳的血液灌注移除體內巴拉刈,並以免疫抑制劑以降低發炎物質攻擊肺部,延緩肺部的損傷和後遺症的產生。
表一 Cyclophosphamide 及 methylprednisolon 或 dexamethasone 注射劑治療巴拉刈中毒的臨床研究7-9,12,14,15
作者 |
文獻類型 |
人數 |
治療方式 |
死亡率 |
註釋 |
Lin 1996 |
- |
16 |
CP 1 g 每天一次,連續2 天 加上 MP 1 g 每天一次,連續3 天 |
25% |
.兩組死亡率有顯著差異 (P< 0.05) .副作用:Leucopenia (37.5% ),一星期後恢復,無需治療 |
17 |
未使用 CP 和 MP |
70.6% |
|||
Lin 1999 |
隨機分派 |
22 |
CP 每天一次每公斤15 mg,連續2 天 加上 MP 1 g 每天一次,連續3 天 |
18.2% |
.兩組死亡率有顯著差異 (P< 0.05) .副作用:Leucopenia (36.4% ),一星期後恢復,無需治療 |
28 |
未使用 CP 和 MP |
57.1% |
|||
Lin 2006 |
隨機分派 |
16 |
CP 1 g 每天一次,連續2天 加上 MP 1 g 每天一次,連續3天 之後 DX 5 mg 每六小時一次 如果 PaO2 <60 mmHg ,重複一次 pulse |
31.3% |
✽兩組死亡率有顯著差異 (P=0.0272) ✽PaO2 > 80 mmHg 才停止DX ✽如果 PaO2 <60 mmHg . MP 1 g 每天一次,連續3天 . 如果 WBC > 3000/ mm2,距第一次 CP 間隔2星期以上,每天一次每公斤15 mg 使用1天 |
7 |
DX 5 mg 每六小時一次 |
85.7% |
|||
Afzali 2008 |
隨機分派 |
9 |
CP 1 g 每天一次,連續2 天 加上 MP 1 g 每天一次,連續3天 Mesna 每天一次每公斤15 mg,連續4天 |
33.3% |
.兩組死亡率有顯著差異 (P < 0.05) |
7 |
未使用 CP,MP 和 Mesna |
81.8% |
|||
Lin 2011 |
回溯性 研究 |
59 |
CP 每天一次每公斤15 mg,連續2 天 加上 MP 1 g 每天一次,連續3 天 之後 DX 5 mg 每六小時一次 如果 PaO2 <60 mmHg ,重複一次pulse |
66% |
✽PaO2 > 80 mmHg才停止 DX ✽如果PaO2 <60 mmHg .MP 1 g 每天一次,連續3天 .如果 BC >5000/ mm2,距第一次 CP 間隔2星期以上,每天一次每公斤15 mg 使用1天 ✽重複 pulse 治療,可顯著降低整體死亡率 (P=0.004) 和因肺纖維化導致低血氧的死亡 (P<0.001) |
52 |
CP 口服每天一次每公斤2 mg,連續14 天 DX 5 mg 每六小時一次,連續14 天 |
92% |
註1:CP: cyclophosphamide;MP: methylprednisolon;DX:dexamethasone。
參考資料:
1. Gawarammana IB, Buckley NA. Medical management of paraquat ingestion. British Journal of Clinical Pharmacology 2011;72(5):745-57.
2. Winchester JF. Paraquat poisoning In: UpToDate, Traub,SJ(Ed),UpToDate 2011.
3. Hart TB, Nevitt A. A new statistical approach to the prognostic significance of plasma paraquat concentrations. Lancet 1984 2(8413):1222-3.
4. 陳妙禎. 巴拉刈中毒. 腎臟與透析 2004;16(3):145-9.
5. Addo E, Poon-King T. Leucocyte suppression in treatment of 72 patients with paraquat poisoning. The Lancet 1986;327(8490):1117-20.
6. Perriëns J, Benimadho S, Kiauw I, et al: High-dose cyclophosphamide and dexamethasone in paraquat poisoning: a prospective study. Human & Experimental Toxicology 1992;11(2):129-34.
7. Afzali S, Gholyaf M. The effectiveness of combined treatment with methylprednisolone and cyclophosphamide in oral paraquat poisoning. Archives of Iranian Medicine 2008;11(4):387-91.
8. Lin JL, Leu ML, Liu YC, et al: A Prospective Clinical Trial of Pulse Therapy with Glucocorticoid and Cyclophosphamide in Moderate to Severe Paraquat-poisoned Patients. American Journal of Respiratory and Critical Care Medicine 1999;159(2):357-60.
9. Lin JL, Wei MC, Liu YC. Pulse therapy with cyclophosphamide and methylprednisolone in patients with moderate to severe paraquat poisoning: a preliminary report. Thorax 1996;51(7):661-3.
10. Descatha A, Mégarbane B, Garcia V, et al: Delayed immunosuppressive treatment in life-threatening paraquat ingestion: a case report. Journal of Medical Toxicology 2009;5(2):76-9
11. Chen GH, Lin JL, Huang YK. Combined methylprednisolone and dexamethasone therapy for paraquat poisoning. Critical Care Medicine 2002;30(11):2584-7.
12. Lin JL, Lin-Tan DT, Chen KH, et al: Improved survival in severe paraquat poisoning with repeated pulse therapy of cyclophosphamide and steroids. Intensive Care Medicine 2011;37(6):1006-13.
13. Li LR, Sydenham E, Chaudhary B, et al: Glucocorticoid with cyclophosphamide for paraquat-induced lung fibrosis. Cochrane Database Syst Rev 2010;16(6):CD008084.
14. Lin JL, Lin-Tan DT, Chen KH, et al: Repeated pulse of methylprednisolone and cyclophosphamide with continuous dexamethasone therapy for patients with severe paraquat poisoning. Critical Care Medicine 2006;34(2):368-73.
15. Agarwal R, Srinivas R, Aggarwal AN, et al: Experience with paraquat poisoning in a respiratory intensive care unit in North India. Singapore Medical Journal 2006;47(12):1033-7.
Management for Paraquat Intoxication
Pei-Tzu Lin, Chan-Wei Chang, Ching-Ling Tai
Department of Pharmacy, Chiayi Chang Gung Memorial Hospital
Abstract
Paraquat is the most popular and virulent herbicide with low lethal dose and should avoid misdrinking. There is no specific antidote for paraquat poisoning. Besides supportive care, the current therapy strategies are preventing paraquat absorption, assisting paraquat removing from blood and alimenting the organ damage of paraqut. Cleaning the contaminated skin and using nasogastric lavage with activated charcoal are used to prevent paraquat absorption. Hemoperfusion is better than hemodialysis which is suitable for acute renal failure patient to remove paraquat from blood. Cyclophosphamide 1g for 2 days and methylprednisolone 1g for 3 days followed by dexamethasone is the best regiment to reduce organ damage. But other antioxidation agents have no significant efficacies.

