摘要
冠狀動脈疾病屬常見的心臟疾病。利用塗藥血管支架放置於周邊或冠狀動脈中,可擴張血管並且緩慢釋放藥物,目前為治療策略之一。塗藥血管支架包含三組成,支架平台,塗布其上的耐久或可降解的高分子聚合物,以及抑制增生藥物或抗癌藥物。本篇主軸將摘錄介紹目前塗藥支架之科技現況。
關鍵字:冠狀動脈疾病、塗藥血管支架、coronary artery disease、drug-eluting stent
壹、前言
隨著時代的進步,由於飲食習慣許多血管疾病也慢慢的浮現,罹患心臟病的人數也有逐年上升的情形。冠狀動脈心臟疾病 (coronary artery disease,CAD),是一個隱形殺手,在醫學檢查常有心衰竭或心律不整等病徵,由於心臟主要藉由心臟的冠狀動脈供應養分,在高糖、高脂、高鹽的飲食中使得冠狀動脈漸漸的堵塞,所能運送的養分也減少了許多。初期可能會造成胸悶頭暈等症狀,後期可能隨時會造成暈倒、休克的嚴重問題,甚至都有可能會危害到生命。現今的人們因有良好的飲食而遺忘需要多多運動,以避免產生血管阻塞等現象。
貳、冠狀動脈阻塞與血管支架
目前醫療處理冠狀動脈阻塞的方式分為兩種:一、做繞道手術 (coronary artery bypass),一般冠狀動脈阻塞時,會使得血流阻塞,通常會截取健康動脈或靜脈在血流量堵塞的分枝,做成繞道接枝到心臟形成另一通道,使得血液得以繞過堵塞處,以維持血液循環和心臟肌肉營養之供給。二為裝置冠狀動脈血管支架,簡稱為血管支架 (stent)1。血管支架是一條非常精細的金屬管狀物,依病灶發生之位置而放置血管病灶所使用之尺寸。方法之一是將氣球導管引導至狹窄之病灶,撐開動脈粥狀硬化之部位,將血管支架植入,可減少血管管壁回縮或血管剝離而維持血管血流暢通2。簡單的說就是將已經阻塞的血管壁內,植入一種金屬物質的支架,使已經阻塞之血管保持通透性,而降低中風、冠狀動脈阻塞的危險性,也可使血管內的氧氣運輸達到最佳之狀態。目前的血管支架製作技術層面,主要是利用精細的金屬合金網狀管狀物,將此支架壓縮附著於氣球導管上,經由引導線及導線運送到動脈病灶處,再藉由氣球擴張術使血管支架留在血管壁中,以保持血流通暢,此支架將置放在病人體內,通常1至3個月後血管內皮細胞會生長將其覆蓋,不再暴露於血管中3。
裝設血管支架仍會有潛在風險,若患者對金屬的支架材料產生過敏則會發生支架內再度狹窄等問題,到目前為止臨床上對於傳統的血管支架再次發生狹窄問題,仍就不斷出現,特別是糖尿病特定族群。目前醫學的發展是將傳統血管支架以藥物塗抹於金屬表面後,再植入病人的血管內,塗藥支架可以抑制平滑肌細胞產生之不當增生,亦可降低血管再次發生狹窄之問題,此種以藥物塗抹於金屬表面之支架稱為塗藥血管支架 (drug-eluting stent,DES)4。以下分別詳述支架,塗布材料,塗藥部分。
一、支架本身
一般血管支架大多為無機金屬材料,最早的血管支架材料是316L 不銹鋼。一般不鏽鋼 (又稱白鋼) 依據其含碳量與含鉻量的比例,可區分成許多不同等級,而其應用也不盡相同。如302為無磁性,一般常用於廚房用具的材料;304作為化學設備,不易氧化;403可作為置物櫃,但具有磁性,使用時間增加會生鏽;而316L 則是作為支架的材料,主要是其含碳量低,因此價格也較高,但其具有堅硬不變型、不褪色、可耐腐蝕,因此在體內生理環境下不會有變型的可能,此外316L 在人體內不會產生排斥,相容性好,因此有其他許多醫療用途,如人工關節、骨釘、脊椎矯正器等。目前陸續有鉭絲,鉑銥合金,鎳鈦合金,鈷銥合金等材質之使用,其中具有記憶性的材料為鎳鈦合金 (Ni-Ti alloy),是目前主流的支架材料商品。鎳鈦合金相變溫度範圍很大 (自-50-80℃),應用範圍很廣。此外在製作支架技術層面,目前多為雷射切割,但若作為腦血管或腎臟血管支架,其精細度則須更高。而支架本身也可利用一些表面處理的方式,來減少新生壞死組織發炎之產生或是產生血栓的機率,例如塗布上 heparin 或 TiO2;或是利用高分子材料塗布於表面,稱為覆膜型5。
二、塗布材料
塗布於支架的材料,目前仍以高分子聚合物材料為主要的塗布材料,但材料種類囊括耐久性的高分子聚合物 (durable polymer) 與生物可降解性的高分子聚合物 (biodegradable polymer) 以及非高分子聚合物 (non-polymer) 的材料,舉例說明如下6。
(一) 耐久性的高分子聚合物 (Durable polymer)
BioLinxTM 為目前新型態的耐久性高分子聚合物,其生物相容性高,材料本身混和三種聚合物,包含疏水性聚合物 (hydrophobic C10 polymer) 可協助藥物控制釋放,和親水性聚合物 (hydrophilic C19 polymer) 使得生物相容性更高,以及親水性聚乙烯吡咯烷酮 PVP (hydrophilic polyvinyl-pyrrolidinone) 可增加起始藥物快速釋出的速率。Endeavour ResoluteTM 即是利用 BioLinxTM 作為塗布材料,屬於第二代的塗藥支架,相較第一代 EndeavourTM 可降低癒合時間增加的風險並延緩血栓的形成。報告指出,所攜帶的藥物 zotarolimus 在一周內可釋出約50%,持續釋放可達31天7。
(二) 生物降解性的高分子聚合物 (Biodegradable polymer)
1. SupralimusTM:
SupralimusTM 所塗布之高分子聚合物分為兩層,基層混和聚乳酸 (poly-l-lactic acid;PLA) 與聚乳酸-甘醇酸 (poly-lactide-co-glycolide;PLGA),表面塗布水溶性之聚乙烯基吡咯烷酮 (polyvinyl-pyrrolidone;PVP)。PVP 表層於支架植入後2小時內即完全被降解,可控制藥物 sirolimus 於一週內釋放達50%,持續釋放至41天。
2. ExcelTM:
ExcelTM 是先將免疫抑制藥品 sirolimus 塗布為一薄層約10-15 µm,再塗布 PLA 作為可降解材料,此設計可達6-9個月的持續釋放。
3. NEVOTM:
NEVOTM 與 ExcelTM 設計模式類似,區別在於 NEVOTM 先將藥物與高分子聚合物先製成複合物型態。此設計以 PLGA 作為塗布材料,藉由調整乳酸 (lactide) 與甘醇酸 (glycolide) 可調控藥物釋出速率。PLGA 是完全可吸收的高分子聚合物,由於較少的 PLGA 材料即可負載高劑量的藥物,以此塗布於支架表面面積也可減少。
4. InfinniumTM:
InfinniumTM 塗布於支架上包含四種高分子聚合物,分別為 PLA、PLGA、PVP 及 poly-l-lactide-co-caprolactone,抗癌藥 paclitaxel 分別貯存於不同高分子聚合物間質中,因此每層中皆存在不同的釋放速率。
(三)Non-polymer
以 YUKONTM 最為常見。YUKONTM 相較於其他塗布高分子聚合物類型的支架,在支架本身做微孔洞 (microporous) 為貯藥空間,將藥物以噴霧方式塗布再逕行乾燥後,停留在表面,以此方式只需要藉由更少量的高分子聚合物作為調控釋放速率。一般藥物釋出完全後,高分子聚合物仍存在於體內,需要更久的時間才可降解完全消失於體內。因此使用更少量的高分子聚合物也是開發塗藥支架的方向之一。
三、塗藥部分
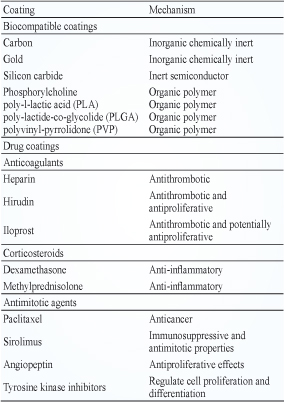
一般支架單獨使用具有支撐的功能,於表面塗布藥物則根據藥物作用性質區分為兩種,一為抑制血管細胞增生的藥物或免疫抑制劑或抗血栓藥物來保持支架本身的功能性與維持生體相容性,由於這些塗布的藥物會經過時間滲透至周圍的血管壁組織內,可達到抑制組織增生或發炎的現象,而降低動脈再次狹窄;一為治療型,大多為抗癌藥為主。由於支架的表面積有限,因此塗布其上的藥物效能 (potency) 必須夠高,才可在有限的面積上釋放足夠的治療濃度8。表一為目前支架上可塗布的基質材料與藥物。
表一 可塗布於支架上的基質及藥物
目前台灣在臨床上,假若病人合乎健保規定之適應症者,即可享有健保給付,以下簡介幾種不同類型之支架。
(一) 禧福釋放冠狀動脈支架 (Cypher. Sirolimus- eluting select. Coronary Stent)
Sirolimus 學名為 rapamycin,為巨環類抗生素,屬於一種免疫抑制藥,主要與紅血球結合,作用是抑制血管細胞的增生,而不會產生組織疤痕。關於 Cypher 之作用機轉,此藥物會在細胞內與 FKBP-129 (FK binding protein, immunophilin) 結合形成免疫抑制複合體 (complex),此複合體對 calcineurine 並無作用,而是與關鍵性調節激活酵素 Mtor (mammalian target of rapamycin) 結合,並抑制其活性,藉此阻斷由 cytokine 主導的T細胞分化週期由 G1 進入S階段,進而抑制其活化與增生,以達到免疫抑制效果9。
(二) 塔克斯紫杉醇冠狀動脈支架 (Taxus Liberte. Monorail. Paclitaxel-Eluting Stent)
Taxusvm 學名為 paclitaxel,為太平洋紫杉醇,屬於一種醫學常見的抗癌藥,此藥品之作用是殺死血管壁附近分裂的癌細胞,而防止血管壁再阻塞之情形發生。紫杉醇作用機轉為有絲分裂中的微管抑制劑,紫杉醇具有聚合和穩定細胞內微管的作用,導致使快速分裂的腫瘤細胞在有絲分裂階段被牢牢固定,而微管不再分開,可阻斷細胞於細胞周期之 G2 與M期,使癌細胞複製受阻斷而死亡。
參、結論
血管支架應用於治療冠狀動脈硬化症造成的血管狹窄成效顯著,並廣泛應用於人體其他的周邊血管,擁有相當雄厚的成長潛力。雖然塗藥血管支架之價格昂貴,需部份自費負擔,但近年來患者接受度愈來愈高。進步的生物醫療科技尚有諸多問題要克服,如何研發設計新一代塗藥血管支架,增進基材與血液的相容性,或可降解型態的支架,以降低血栓形成,提供心臟血管病人安全、療效明確且符合經濟效益的塗藥血管支架,是未來一項重要的課題。
參考資料:
1. Burt HM, Hunter WL: Drug-eluting stents: an innovative multidisciplinary drug delivery platforms. Adv Drug Deliv Rev 2006; 58: 345-346.
2. Hoffmann R, Mintz GS, Dussaillant GR, et al: Patterns and mechanisms of in-stent restenosis. A serial intravascular ultrasound study. Circulation. 1996; 94: 1247-1254.
3. Htay T, Liu MW: Drug-eluting stent: a review and update. Vasc Health Risk Manag 2005;1: 263-276.
4. Fattori R, Piva T: Drug-eluting stents in vascular intervention. Lancet 2003; 361: 247-249.
5. Kukreja N, Onuma Y, Daemen J, Serruys PW: The future of drug-eluting stents. Pharmacol Res 2008; 57: 171-180.
6. Capodanno D, Dipasqua F, Tamburino C: Novel drug-eluting stents in the treatment of de novo coronary lesions. Vasc Health Risk Manag 2011; 7: 103-18.
7. Udipi K, Melder RJ, Chen M, et al: The next generation Endeavor Resolute Stent: role of the BioLinx Polymer System. EuroIntervention 2007; 3: 137-139.
8. Puranik AS, Dawson ER, Peppas NA: Recent advances in drug eluting stents. Int J Pharm 2012 in press doi: 10.1016/j.ijpharm.2012.10.029.
9. Chieffo A, Aranzulla TC, Colombo A: Drug eluting stents: focus on Cypher sirolimus-eluting coronary stents in the treatment of patients with bifurcation lesions. Vasc Health Risk Manag 2007; 3: 441-451.
10. Sheiban I, Villata G, Bollati M, Sillano D, Lotrionte M, Biondi-Zoccai G: Next-generation drug-eluting stents in coronary artery disease: focus on everolimus-eluting stent (Xience V). Vasc Health Risk Manag 2008; 4: 31-38.
Drug-Eluting Stent
Yi-Ping Fang1, Pei-Yi Hsieh2, Ping-Yi Lee3
Department of Biotechnology, Yuanpei University1
Taipei City Hospital, Hepig Branch2
Department of Pharmacy, Kaohsiung Chang Gung Memorial Hospital3
Abstract
Coronary artery disease is the most common form of heart disease in the world. Utilizing a drug-eluting stent dilated the peripheral or coronary arteries and slowly releasing a drug to block cell proliferation is one of the treatment strategy. The drug-eluting stent composed of three elements including an antiproliferative drug, a durable polymer and the stent platform. Herein, the objective was summarized the current status and technical achievements of drug-eluting stent.

