摘要
本文為一乾癬病人使用 methotrexate 引起皮膚毒性反應的案例報告。Methotrexate可能引起罕見的皮膚毒性反應,大多發生於乾癬患者,其機轉可能為快速增生的患部細胞較易攝入 methotrexate,而較正常細胞易造成毒性。通常發生於開始治療後的3至7天內,症狀包括皮膚燒灼感、剝離壞死,有如蛇蛻皮一般。皮膚毒性反應可能為嚴重血液毒性的前哨兵,因此應盡早於24小時內給予解毒劑 calcium folinate。Methotrexate 引起皮膚毒性反應的危險因子包括老年人、較高或增加 methotrexate 劑量、感染、腎功能不全及併用危險藥品,如非類固醇消炎止痛藥 (nonsteroidal antiinflammatory drugs,NSAIDs) 及 trimethoprim-sulfamethoxazole (TMP-SMX) 等。對於高危險群患者,建議使用較低的 methotrexate 起始劑量,並依臨床治療需要緩慢增加劑量,同時小心監測患者是否發生相關的不良反應。
關鍵字: methotrexate、calcium folinate、乾癬、皮膚毒性反應
壹、前言
Methotrexate 為葉酸拮抗劑,可抑制 DNA 的合成及修復,具有抗發炎、抗增生及抗腫瘤作用,常用於風濕性關節炎、乾癬及癌症。長期使用 methotrexate 可能造成肝臟及肺臟的傷害,而急性症狀則多為口腔、胃腸道潰瘍或胃炎,以及血液毒性造成全血球低下,皮膚方面則可能有紅疹、燒灼感、脫皮及壞死。本文藉由一案例討論乾癬病人使用 methotrexate 引起皮膚毒性反應,並進一步探討其危險因子及其治療。
貳、病例
一、基本資料及入院經過
一位49歲男性病人,過去病史為精神分裂症,曾因自殺未遂導致截肢,沒有抽菸、喝酒及其他過敏史,患者因乾癬在某地區醫院風濕過敏科治療,並於2012/4/5開始服用 methotrexate,其藥歷如表一。
表一 Methotrexate 門診處方藥歷
2012/4/5 |
2012/4/19 |
2012/5/10 |
2012/5/24 |
|
Methotrexate 2.5 mg/tab |
1# QW |
2# QW |
3# QW |
4# QW |
於5/24門診後一段時間,患者開始出現皮膚毒性反應,紅疹首先出現於下肢,而後蔓延至下背及上臂,皮膚轉黑且開始出現水泡,患部呈燒傷狀且有疼痛感,且口腔黏膜亦出現潰瘍,因此患者於6/4被送至本院急診。患者本身無法清楚表達疾病過程,而根據主要照護者 (患者哥哥) 表示,皮膚症狀起始時間不明。
患者於急診時即給予預防性抗生素 ertapenem 及 vancomycin,並以 gentamicin 藥膏處理傷口,然而6/6出現白血球低下 (leucopenia) 及輕微發燒 (37.8度),絕對嗜中性白血球數量 (absolute neutrophil count,簡稱 ANC) 為510/μL,懷疑為 methotrexate 造成的毒性反應,因此會診皮膚科後給予 calcium folinate 錠劑 (15 mg/tab) 1# q6h,並抽血檢測 methotrexate 血中濃度,檢測結果為0.01 μmol/L,而後轉入皮膚科病房觀察,入院後經過、用藥紀錄及檢驗數值如表二至四。
表二 患者住院經過

表三 用藥紀錄
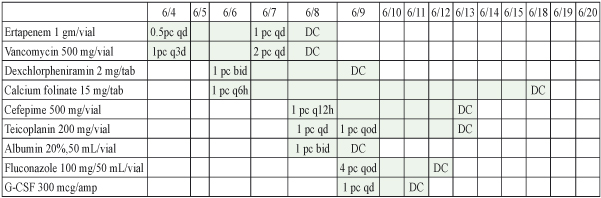
表四 檢驗數值
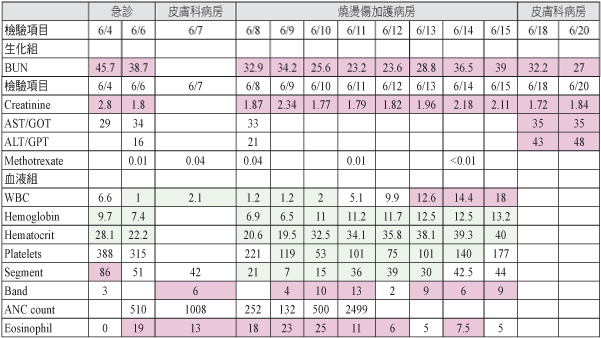
參、討論
Methotrexate 為葉酸拮抗劑,藉由不可逆地抑制二氫葉酸還原酶 (dihydrofolate reductase,簡稱 DHFR),來抑制 DNA 及 RNA 的生合成,主要用以治療癌症,如子宮絨毛膜上皮癌、急性淋巴性白血病及骨肉瘤等,且 methotrexate 有免疫調節作用,可用於治療類風濕性關節炎,然而實際作用機轉尚不明確。另外,methotrexate 可作用於皮膚表層快速分裂的細胞,因此可用於嚴重頑固性乾癬的治療1,如本案例患者的臨床用途。
Methotrexate 在胃腸道吸收佳,在血漿中約有50-70% 與白蛋白結合,可能被其他高蛋白結合率的藥物 (如 phenytoin、salicylates 及 sulfonamides) 取代結合位置,而提高游離態濃度。Methotrexate 的排除主要經由腎臟,少部分經由肝臟代謝。Methotrexate 可能造成肝、肺毒性及急性腎衰竭,對於快速增生的黏膜細胞,如胃腸道及口腔表皮等,容易造成潰瘍及壞死,methotrexate 也可能造成血液毒性,包括全血球低下,使患者容易發生嚴重感染而造成高死亡率。另外,methotrexate 也可能造成罕見的皮膚毒性反應,症狀包括燒灼感、皮膚剝離壞死,有如蛇蛻皮一般2。
根據文獻,methotrexate 引起的皮膚毒性反應大多發生於原本已有皮膚疾病的病人,特別是乾癬患者,可能在使用 methotrexate 不久後,在原本的患部區塊發生疼痛性的壞死,而被視為乾癬的惡化,因此增加 methotrexate 的劑量,使得毒性反應更加惡化。為何乾癬患者較易發生 methotrexate 的皮膚毒性反應呢?假設性的機轉為這些快速增生的患部細胞,較易攝入 methotrexate,因此較正常細胞易引起毒性3。
Methotrexate 引起的皮膚症狀,通常發生於開始使用後的3至7天內,而血液毒性則多發生於使用一週後,因此 methotrexate 引起的黏膜炎及壞死,被視為嚴重血液毒性的前哨兵,且可用來輔助診斷患者是否有急性中毒4。以本案例患者而言,因無法確認症狀起始時間,無法與文獻對照,然而患者在6/4急診抽血檢驗白血球仍有6600/μL,當時皮膚已成燒傷狀,兩天後的白血球即掉到1000/μL,觀察其症狀時序與文獻相符。發生 methotrexate 毒性的危險因子包括老年人、感染、腎功能不全及併用危險藥品,如非類固醇消炎止痛藥 (nonsteroidal antiinflammatory drugs,NSAIDs) 及 trimethoprim-sulfamethoxazole (TMP-SMX) 等,併用 sulfonamides 藥品可能妨礙 methotrexate 在腎臟的排除,且取代 methotrexate 與血漿中蛋白質的結合,而提高 methotrexate 的血中濃度4-6。此外,藥物劑量亦是重要的危險因子之一,雖然文獻中曾觀察到即使在治療劑量下,methotrexate 可能因慢性累積造成毒性,但多數的患者仍是使用高於治療劑量,或是增加劑量而發生相關的不良反應4,6,7。本案例患者為49歲男性,入院前有輕度腎功能不佳 (3/5血漿肌酸酐值為1.95 mgdL),且於近一個半月內調高 methotrexate 的劑量,由一周2.5 mg 增加為10 mg,可能為引起皮膚及血液毒性的原因。
除了鑑別臨床症狀外,皮膚病理切片及檢測患者血中 methotrexate 濃度,亦能有助於診斷及治療。然而血中 methotrexate 濃度與是否發生毒性沒有絕對的相關性,僅能用於決定解毒劑的劑量,一但懷疑患者發生毒性時,不需等血中 methotrexate 濃度結果,即應立即停藥並給予解毒劑 calcium folinate4。Calcium folinate 為活性葉酸,不需經 DHFR 代謝即可拮抗 methotrexate 的作用,且若能在最後一次 methotrexate 投與後12至24小時內給予,治療效果最佳,通常可在治療後約兩周恢復,然而若延誤治療時機,療效將大幅降低,甚至可能無法反轉毒性。Calcium folinate 劑量為每3-6小時給予100 mg/m2,靜脈輸注15-30分鐘,速率不可超過160 mg/min,治療應持續數天直到臨床症狀改善,且 methotrexate 濃度小於0.01 μmol/L。對於嚴重白血球低下的患者,可考慮給予白血球生長激素 G-CSF,另外對於貧血及血小板低下患者,則可以考慮輸血補充紅血球及血小板。其他支持性治療包括給予含 bicarbonate 的輸液,以鹼化尿液來降低腎臟毒性8。
本案例患者因追蹤 methotrexate 濃度均不高 (0.01-0.04 μmol/L),故口服 calcium folinate 15 mg/tab pc q6h,使用時間為6/6-6/18。血液毒性方面,6/6開始出現白血球低下 (ANC 為510/μL),因6/9 ANC更降至132/μL,此時給予 G-CSF 300 mcg/amp 1pc qd,之後6/11因 ANC 上升至2499/μL,於是停用 G-CSF,其白血球低下持續時間約五天,較文獻中血球恢復的時間為短。
肆、結論
Methotrexate 可能引起罕見的皮膚毒性反應,且患者多有皮膚相關的疾病 (如乾癬),因此不易被察覺而可能延誤治療時機。根據文獻報告及本案例均可發現,皮膚的毒性反應可能預告了嚴重血液毒性的發生,因此應盡早給予解毒劑 calcium folinate 及支持性療法 (如給予輸液),對於嚴重白血球低下的患者,可考慮給予 G-CSF,以免造成不可逆的血球低下。對於易發生 methotrexate 毒性的高危險群,如年紀大、腎功能不佳或併用 NSAID 的患者,應注意 methotrexate 的使用劑量,建議由低劑量開始治療,若因臨床症狀須調高劑量,則應緩慢調高劑量,根據2009年美國乾癬基金會 (National Psoriasis Foundation) 建議,當開始 methotrexate 治療或是每次調高劑量時,應於一周後追蹤患者的全血球數,之後的前幾個月應間隔2至4周追蹤9,同時小心監測患者是否發生其他相關的不良反應。
參考資料:
1. Olsen EA. The pharmacology of methotrexate. J Am Acad Dermatol 1993; 25: 300-318.
2. Roenigk HH Jr, Auerbach R, Maibach HI, et al: Methotrexate in psoriasis: consensus conference. J Am Acad Dermatol 1998; 38: 478-485.
3. Lawrence CM, Dahl MGC. Two patterns of skin ulceration induced by methotrexate in patients with psoriasis. J Am Acad Dermatol. 1984; 11(6): 1059-1064.
4. Fridlington JL, Tripple JW, Reichenberg JS, et al: Acute methotrexate toxicity seen as plaque psoriasis ulceration and necrosis: A diagnostic clue. Dermatol Online J. 2011 Nov 15; 17(11): 2.
5. Kazlow DW, Federgrun D, Kurtin S, Lebwohl MG. Cutaneous ulceration caused by methotrexate. J Am Acad Dermatol. 2003; 49(2)Suppl2: S197-198.
6. Tan KW, Tay YK. A case of acute methotrexate toxicity. Ann Acad Med Singapore. 2011 Feb; 40(2): 97-9.
7. Kaplan DL, Olsen EA. Erosion of psoriatic plaques after chronic methotrexate administration. Int J Dermatol. 1988; 27(1): 59-62.
8. Micromdex: Toxicology of methotrexate sodium. Available at http://www.thomsonhc.com/micromedex2/. Accessed on September, 2012.
9. Kalb RE, Strober B, Weinstein G, Lebwohl M. Methotrexate and psoriasis: 2009 National Psoriasis Foundation Consensus Conference. J Am Acad Dermatol. 2009 May; 60(5): 824-37.
Methotrexate-Induced Cutaneous Toxicity in A Psoriasis Patient
Chien-Yi Yang, Chi-Yuan Cheng, Chi-hua Chen
Department of Pharmacy, Chang-Gung Memorial Hospital Linkou
Abstract
We reported a patient with psoriasis who developed methotrexate-induced cutaneous toxicity. Methotrexate can cause rare cutaneous toxicity most commonly in patients with psoriasis. It has been hypothesized that these hyperproliferative epidermal cells of psoriatic plaques take up more of the methotrexate than normal cells and are thus more susceptible to its toxic effects. The symptoms include burning sensation and sloughing of the skin and usually appeared between 3 and 7 days after exposure. The cutaneous toxicity may serve as a herald for the impending development of life-threatening pancytopenia, hence, the antidote "calcium folinate" should be administered within 24 hours. Predisposing factors for methotrexate induced cutaneous toxicity include older age, higher or increased methotrexate dose, infection, renal dysfunction and concomitant use of nonsteroidal antiinflammatory drugs or trimethoprim-sulfamethoxazole. For these high risk patients, it is suggested to start with lower initial dose of methotrexate and adjust gradually according to clinical response. Meanwhile, we should carefully monitor whether the adverse drug reactions related to methotrexate was occurred.

