摘要
貧血是慢性腎臟病 (chronic kidney disease, CKD) 患者最常見的併發症,一般認為與腎臟無法產生足夠的紅血球生成素 (erythropoietin, EPO) 有關,其他像是慢性出血、發炎反應、營養不良或副甲狀腺功能亢進…等亦可能導致貧血的情形。紅血球生成刺激劑是治療腎性貧血最主要的藥品,目前市面上所使用的紅血球生成刺激劑有多種選擇,彼此間在血紅素的提升效果上差異不大,皆藉由直接或間接結合至紅血球生成素接受體之方式以刺激紅血球生成素分泌。腎性貧血若能適時評估與治療,可以有效改善患者的生活品質與預後。
關鍵字: 慢性腎臟病、貧血、紅血球生成刺激劑、chronic kidney disease、anemia、erythropoiesis stimulating agents
壹、前言
貧血是慢性腎病 (chronic kidney disease, CKD) 患者最常見的併發症之一,慢性出血、發炎反應、營養不良或副甲狀腺功能亢進…等都可能導致腎性貧血,若能適時評估與治療 CKD 患者的貧血,可以改善患者的生活品質與預後,甚至可能延緩腎臟疾病的惡化。
貳、貧血的發生原因
貧血是體內紅血球數量降低的一種表現,通常可藉由血紅素 (hemoglobin, Hb) 的降低而得知,當紅血球數量不足時組織即會產生缺氧的現象,出現蒼白、頭暈、疲倦及呼吸急促…等症狀,長期下來亦可能造成代償性的心輸出量增加、左心室肥大、心衰竭…等心血管問題1。造成貧血的原因非常多元,通常由許多種因素所共同造成,約有5成的貧血是由鐵離子缺乏所導致,但隨著地域及種族的不同,發生貧血的原因也會有所差異,另外像是血液流失過多、寄生蟲感染、急慢性感染或微量元素…等的缺乏,也會增加貧血發生的風險2。
參、慢性腎臟病與貧血之關連性
人體內紅血球的數量,主要是由位於腎臟皮質上對組織氧合極為敏感的特殊間質細胞所控制,當有貧血或其他原因造成組織氧合量下降時,會透過缺氧誘發因子 (hypoxia inducible factor, HIF) 等訊息之調控而促使紅血球生成素 (erythropoietin, EPO) 分泌,最後 EPO 會結合至骨髓內紅血球的前驅細胞 erythroid colony-forming units (CFU-Es) 上,以預防 CFU-Es 的細胞凋亡及促進其分化的方式來增加紅血球的數量 (圖一)。在有腎臟疾病的患者上,前述 EPO 的產生能力會降低,造成 EPO 不足及紅血球生成過程的早期凋亡而導致貧血3。
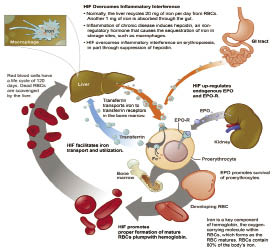
圖一 紅血球生成的調控機轉15
CKD 患者伴隨有貧血的情形極為常見,曾有研究發現,對於未進行透析的患者而言,貧血的盛行率隨著腎功能的下降而提高,當 eGFR 下降至15 mL/min/1.73 m2時,約有33%的男性及67%的女性有貧血之情形;而若是已經接受血液透析的腎臟病人者,發生貧血的比例甚至高達90%4。腎性貧血發生的原因通常是由多種因素所造成,像是慢性出血、發炎反應、營養不良,副甲狀腺功能亢進或體內尿毒素蓄積…等都會降低紅血球生成,但一般多認為腎臟無法產生足夠的 EPO 是造成腎性貧血的主因。若能適時治療腎病人者的貧血,除可以改善患者的生活品質與疾病的預後外,甚至可以延緩腎臟疾病的惡化5。
肆、腎性貧血的評估與治療目標
美國國家腎臟基金會 (NKF/KDOQI) 於1997年時,公佈了 CKD 貧血標準與血色素目標的治療指引,並分別於2000、2006及2007年進行改版與更新。在2006年的指引中提到,分辨貧血與否是評估 CKD 患者貧血癒後、診斷與治療效果最首要的步驟,不論患者的腎病期別與成因為何,每年皆至少進行一次血紅素濃度之檢測;而當男性 Hb < 13.5 g/dL、女性 Hb < 12.0g/dL 時則應診斷為貧血並需進一步評估與治療。
一、貧血的評估
由於 CKD 患者的貧血不一定全然由 EPO 缺乏所造成,可利用數項指標來判斷導致貧血或造成藥物治療效益不佳之原因,其指標包括了全血球計數 (CBC)、白血球分類及血小板計數、網狀紅血球計數 (absolute reticulocyte count),以及血清鐵蛋白 (ferritin)、血中運鐵蛋白飽和度 (serum transferring saturation, TSAT) 與網狀紅血球血色素含量 (reticulocyte hemoglobin content, CHr)。血清鐵及 TSAT 代表可以立即提供紅血球生成的鐵含量,而 ferritin 則代表體內鐵的總儲存量;對非透析的患者而言,當男性的 ferritin < 25 ng/mL、女性 < 12 ng/mL 時即代表鐵儲存量的極度不足,而若 TSAT < 16%時,體內即無足夠的鐵可提供用以驅動紅血球生成,即出現所謂缺鐵性貧血的情況3。
二、Hb 的治療目標
由於在多個研究的結果皆發現,將 Hb 提高至 > 11 g/dL 時,可以有意義改善患者的預後,包括可以增加生活品質、降低死亡率及住院率,以及降低嚴重左心室肥大的發生率;至於對於將 Hb 提高至 ≥ 13 g/dL 的患者,在存活率、住院率或左心室肥大發生率方面並沒有明顯的好處,甚至有較高心血管副作用之傾向;因此 KDOQI 在2006年改版的指引中,建議 CKD 患者的 Hb 應維持在 > 11 g/dL 以上,同時認為對於使用紅血球生成刺激劑 (erythropoiesis stimulating agents, ESA) 治療的 CKD 患者,並沒有足夠證據建議應將 Hb 提高至 ≥ 13 g/dL3。
然而,KDQOI 在後續審閱數個研究的結果後,又在2007年將指引做了小幅更新,將使用 ESA 的未透析或已透析患者之 Hb 值,重新設定於11-12 g/dL 間;同時認為,使用 ESA 治療的 CKD 患者不論透析與否,其 Hb 皆不應該 > 13 g/dL6,並將該建議之證據等級提高。而最近在2011年6月由 FDA 對 CKD 患者使用 ESA 的聲明中更表示,若 CKD 患者的 Hb < 10 g/dL,即可開始 ESA 的治療,同時認為若 CKD 患者的 Hb ≥ 11 g/dL,除可能增加死亡、嚴重心血管副作用及中風之風險外,亦沒有臨床上額外之效益,因此更進一步將 CKD 已透析患者的 Hb 目標限縮在 ≤ 11 g/dL 內7 (表一)。因而在臨床許可的情況下,若能將 Hb 嚴格控制在10-11 g/dL 間似乎是更為理想之選擇。
表一 KDOQI 與 FDA 之指引比較

伍、腎性貧血的藥物治療選擇
ESA 及鐵劑是治療腎性貧血最重要也最廣泛使用的藥品,目前市面上 ESA 達到並維持 Hb 目標的效果皆差不多,最大的差異僅在於藥效長短之不同。需注意的是,若 CKD 患者使用 ESA 一段時間後仍無法達到 Hb 目標,即有可能產生了 ESA 抗性。ESA 抗性最常見的原因是鐵缺乏,每當腎性貧血的患者無法以 ESA 達到目標 Hb 時,即應評估是否有造成對 ESA 的反應不佳的其他特定原因 (表二)。另外若患者以 ESA 治療超過4週,而 Hb 以每週0.5-1.0 g/dL 的速度下降,或每週須要輸血1-2次,但血小板及白血球都正常且網狀紅血球計數低於10000/uL 時,即應懷疑可能產生 ESA 抗體,此抗體會中和 ESA 及內生性的 EPO,產生抗體導致的純紅血球生成不良 (antibody-mediated pure red cell aplasia, PRCA),造成嚴重的貧血甚至可能致命3。
表二 2006 年 KDOQI 對腎性貧血的治療建議3

一、Epoetin
Epoetin 中的 Epoetin-α 及 Epoetin-β 是目前最廣泛使用的基因重組人類紅血球生成素,兩者皆由中國倉鼠卵巢細胞所製造而來,惟在胺基酸側鏈結構上有些差別。Epoetin-α 及 Epoetin-β 的半衰期長短與給藥途徑有關 (靜脈約4-11小時,皮下約19-25小時),兩者在各指引的使用建議上並沒有太大差異,可以每週2-3次的頻率以皮下或靜脈的途徑給予,同時兩者在改善腎性貧血的效果亦相當。Epoetin 在皮下的生體可用率只有靜脈途徑的1/3,多數的指引仍建議以皮下的方式投與,同時皮下較靜脈的途徑可以減少約15-50%的每週劑量,可能與皮下的藥物吸收速度較慢有關8。
二、Darbepoetin-α
Darbepoetin-α 是2001年 FDA 所核准的另一個 ESA,Darbepoetin-α 與 Epoetin 一樣是由中國倉鼠卵巢細胞所製造而來,但其在胺基酸序位之調整,使半衰期較 Epoetin 延長了近3倍之多9。常見的起始劑量為0.45 mcg/kg,以靜脈或皮下之方式每週投予1次,再依 Hb 的值調整劑量,但調整頻率不應大於每月1次。每1 mcg 的 Darbepoetin-α 大約相當於200 IU 的 Epoetin10,對於先前使用 Epoetin 每週2-3次的患者,Darbepoetin 應每週給藥1次,若先前使用 Epoetin 每週1次,則 Darbepoetin-α 則每2週給藥1次11。
三、Continuous Erythropoiesis Receptor Activator (CERA)
CERA 是 FDA 於2007年11月所核准的另一個 ESA,其主要是在 Epoetin-β 的分子接上一個 polyethylene glycol (PEG) 側鏈,半衰期因而延長至130小時左右,給藥頻率得以再為拉長12。初次使用的劑量為0.6 mcg/kg,以靜脈或皮下之方式每2週投予一次,若 Hb 可以維持至目標值,給藥頻率可調整為每月1次,每次2倍之劑量。另需注意的是,由於在使用 CERA 治療的患者中,曾有因產生 EPO 抗體而發生 PRCA 之案例,同時這些抗體對所有 ESA 有交叉反應亦已被證實,因此懷疑或確認患者含有 EPO 抗體者,不應再將 ESA 轉換為 CERA11。
四、Peginesatide
國內並未上市的 Peginesatide 是 FDA 在2012年3月所核准的最新一種 ESA,它是與內生性或重組 EPO 結構完全不同的聚乙烯二醇化雙聚胜肽化合物 (pegylated dimeric peptide),其雙聚胜肽的結構可以結合至 EPO 接受體,除了刺激紅血球的生成外亦將半衰期大幅延長10。此藥除了有每月給藥1次的便利性外,由於其與 EPO 的結構不同,理論上並不會與 EPO 抗體產生交叉反應,其臨床效益應並不會被 EPO 抗體所中和,是在患者產生 PRCA 後或許仍能使用的 ESA13。不過可惜的是,Peginesatide 因上市後的過敏反應問題而於2013年2月底進行全球的自願性回收14。
陸、結論
貧血是 CKD 患者最常見的併發症之一,若未積極加以矯正,患者除了可能出現相關的併發症外,更會影響預後、生活品質與心臟…等功能。目前在 CKD 患者的貧血治療藥物仍以鐵劑及 ESA 為首要,由於各 ESA 的臨床效益差異不大,可依患者需求選擇合適給藥頻率之藥物。然而,畢竟每次的藥物注射對患者的生理及心理都是壓力與負擔,若未來能有更長效與安全的製劑可供選擇,相信對患者而言應是一大福音。
參考資料:
1. 李文欽、張舜智、黃忠餘等:慢性腎臟病與貧血。腎臟與透析2007; 19: 81-88。
2. Iron deficiency anaemia: assessment, prevention, and control. A guide for programme managers. Geneva, World Health Organization, 2001(WHO/NHD/01.3).
3. KDOQI: KDOQI Clinical Practice Guidelines and Clinical Practice Recommendations for Anemia in Chronic Kidney Disease. Am J Kidney Dis 2006;47(Suppl 3):S11-145.
4. 黃俊德、吳明儒、徐國雄:血液透析病人之貧血。腎臟與透析2012; 24: 195-200。
5. Tarng DC: Cardiorenal anemia syndrome in chronic kidney disease. J Chin Med Assoc 2007; 70(10):424-9.
6. KDOQI: KDOQI Clinical Practice Guideline and Clinical Practice Recommendations for anemia in chronic kidney disease: 2007 update of hemoglobin target. Am J Kidney Dis 2007;50(3):471-530.
7. FDA Drug Safety Communication: Modified dosing recommendations to improve the safe use of Erythropoiesis-Stimulating Agents (ESAs) in chronic kidney disease. Available at: http://www.fda.gov/drugs/drugsafety/ucm259639.htm
8. Deicher R, Hörl WH: Differentiating factors between erythropoiesis-stimulating agents: a guide to selection for anaemia of chronic kidney disease. Drugs 2004;64(5):499-509.
9. Locatelli F, Del Vecchio L: Optimizing the management of renal anemia: challenges and new opportunities. Kidney Int Suppl 2008;111:S33-7.
10. Hörl WH: Differentiating factors between erythropoiesis-stimulating agents: an update to selection for anaemia of chronic kidney disease. Drugs 2013;73(2):117-30.
11. NESP®、MIRCERA®藥品中文仿單。
12. Fishbane S: Anemia in chronic kidney disease: status of new therapies. Curr Opin Nephrol Hypertens 2009;18(2):112-5.
13. Macdougall IC, Rossert J, Casadevall N, et al: A peptide-based erythropoietin-receptor agonist for pure red-cell aplasia. N Engl J Med 2009;361(19):1848-55.
14. Affymax and Takeda Announce a Nationwide Voluntary Recall of All Lots of OMONTYS® (peginesatide) Injection, Available at:http://www.fda.gov/Safety/Recalls/ucm340893.htm
15. HIF-Erythropoiesis, Available at:http://www.fibrogen.com/erythropoiesis
Evaluation and Management for Anemia in Chronic Kidney Disease
Yu-Wei Hsu, Pei-Fen Tsai, Hui-Chuan Lin
Department of Pharmacy, Ditmanson Medical Foundation Chia-Yi Christian Hospital
Abstract
Anemia is a undesirable complication that develops in most patients with Chronic Kidney Disease (CKD), several factors including chronic bleeding, inflammation, nutritional deficiencies or hyperparathyroidism are associated with anemia in CKD patients. Insufficient erythropoietin production by the kidney is generally considered as a major cause of renal anemia. Erythropoiesis stimulating agents (ESAs) increase the production of erythropoietin through direct or indirect action on the erythropoietin receptor. Currently available ESAs showed a similar efficacy on hemoglobin level achievement and played the prominent role on anemia management in CKD. For CKD patients, early assessment and management for anemia improves not only the quality of life but prognosis of patients.

