摘要
鉛中毒常會被延誤診斷或誤診為急性腹痛。此案例為50歲女士,過去病史有高血壓、及慢性腎衰竭使用腹膜透析治療,入院前一週病人即有腹痛、噁心和便秘等情形。入院後病人除腹痛外合併有四肢無力等情形,住院期間曾因血氧偏低緊急插管。此案例懷疑因長期服用中藥而導致鉛中毒;在檢驗部分病人呈現貧血 (Hb = 9.3 g/dL) 和血鉛濃度過高 (Pb = 145.2 μg/dL)。經由 CaEDTA 治療後,血鉛濃度由145.2→98.6→42.3→25.7 ug/dL。四肢無力及胃腸道不適等症狀皆已改善。
關鍵字: 鉛中毒、CaEDTA、lead poisoning
壹、前言
多數鉛中毒是因為長期曝露於含鉛的環境中。臨床上鉛中毒的病人症狀多變,且無專一性,在診斷上較為困難。臨床上若懷疑病人是鉛中毒時,需觀察病人是否有肚子痛 (鉛絞痛)、便秘、高血壓、貧血、牙齒是否有出現『鉛線』,有些病人會合併有神經系統的障礙,像是失眠、焦慮、手腳酸麻、全身無力倦怠,甚至在末期會出現手足下垂症,嚴重者會出現腦水腫,合併腦壓增高的症狀。鉛中毒的治療,主要是以 CaEDTA 治療;以 CaEDTA 治療可提高鉛的排除20-50倍;若能早期發現鉛中毒,則中毒現象為可逆。
貳、案例報告
本案例為一位50歲女士,過去病史有高血壓、心肌梗塞、末期腎衰竭,已使用腹膜透析治療5年;入院前7天曾出現噁心、嘔吐、腹痛,並曾求診於胃腸科被診斷為胃潰瘍;此次仍因胃腸不適入院,病人主訴為便秘、腹脹。本次住院主要診斷為腸阻塞及胃潰瘍。
病人於4/21入院治療,但4/24於病房出現嗜睡、意識改變、全身無力,且無法自行翻身,至4/25除上述症狀未改善外,病人對疼痛刺激無反應,且氧氣使用下血氧仍偏低,故緊急插管治療送至加護病房。病人入加護病房插管後意識恢復,但仍持續四肢無力,且非常焦慮;由一系列的檢查 (表一) 可知無非典型肺炎、腹水培養有一套 coagulase-negative staphylococcus, CONS,在腦部電腦斷層掃描、核磁共振及腦波,並沒有出血或癲癇等異常情形。在生化檢驗值 (表二) 顯示病人肝功能、血氨、凝血功能、及心肌酵素皆正常,也沒有電解值異常情形。而有異常的部份為白血球 (WBC = 10.9 103/uL) 有偏高的趨勢,懷疑與腹腔感染有關,因此在藥物上是選用 piperacillin3g q12h 治療;而血紅素偏低 (Hb = 8.5 g/dL),懷疑是與病人末期腎衰竭有關。
表一 細菌培養及腦部檢查

表二 生化檢驗值
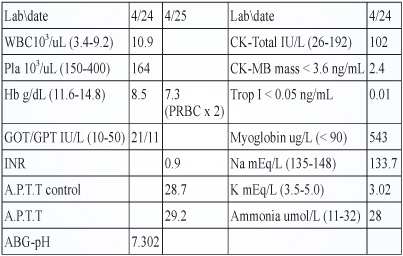
由於病人血氨值正常 (ammonia = 28 umol/L),腦部檢查也無異常情形;無法解釋為何病人會四肢無力;因此於4/25會診神內醫師,神內醫師診斷為格林-巴里症綜合症 (Guillan-Barre syndrome, GBS),建議以血漿置換術治療。於4/29-5/8進行血漿置換術,治療療程結束後病人焦慮、腹脹,四肢動度皆未改善;此時家屬想以中藥進行治療,並透露病人在家中有長期服用中藥;為避免有重金屬中毒的疑慮,醫師將病人血液送檢,測得血鉛濃度為145.2 ug/dL (< 30 ug/dL) 已超過正常值 (表三)。另外在其它重金屬的部份,例如鎘、砷、汞、鋁皆於正常值內 (表三)。
表三 中金屬檢測值
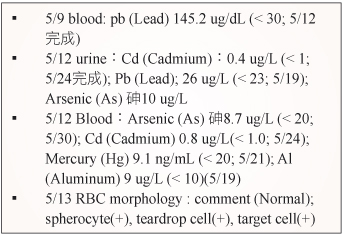
當確定診斷為鉛中毒後,立即使用 CaEDTA 治療,CaEDTA 治療療程一次為5天,此病人於5/12-5/16施行第一個療程,劑量為500 mg qd,經治療後血鉛濃度由145.2→98.6 ug/dL (表四),因血鉛濃度已有明顯降低,評估應續用 CaEDTA 治療;經由三個療程治療後,血鉛濃度由145.2→98.6→42.3→25.7 ug/dL (表四),肌肉無力情形明顯改善,且腎功能也有改善,scr 由5.81→4.24→3.85→3.83 mg/dL (表五)。
表四 鉛濃度與肌力
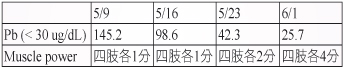
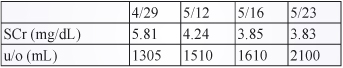
表五 腎功能檢驗值及尿量
參、討論
鉛中毒的特徵包含有肚子痛 (鉛絞痛)、便秘、焦慮、記憶力降低、高血壓、貧血、紅血球會出現嗜鹼性斑點、牙齒出現『鉛線』、手腳酸麻、全身無力倦怠,有的病人甚至會出現手足下垂症1,2。本案例在上述症狀中,除紅血球無出現嗜鹼性斑點、牙齒無出現『鉛線』外,其它症狀皆曾表現。
成年人鉛中毒的常見原因為,大多由呼吸道吸入所造成,約占40%3,而從腸胃道吸收鉛約佔10-15%,常見原因為禁食之患者,因飲食中缺乏鈣、鐵、磷、或鋅。鉛一旦被吸收會分布到血液中、軟組織、和骨骼肌;血液中的鉛有99%會與紅血球結合,而另外1%的游離鉛會分布至軟組織中,例如:腎臟、腦、肝臟、骨髓。在血液中的鉛可經由腎臟排除,若腎臟功能是正常的平均排除半衰期約為30天4。但若鉛存在骨骼肌裡,則排除半衰期會長達十年,且代表體內約95%以上含有鉛4。
鉛是屬於有毒金屬易導致人體器官衰竭1,3。若早期發現鉛中毒,則中毒現象為可逆性的。但若長期曝露於高濃度的鉛,則可能會造成不可逆的中樞神經、周邊神經系統及腎功能的損害。
本案例有末期腎病的病史,由文獻得知,鉛所造成的腎毒性又分為急性及慢性;在急性鉛中毒的定義為血鉛濃度大於100 ug/dL,易造成近端腎小管損壞5。而慢性鉛中毒,多數是因為長期 (5-30年) 曝露於鉛濃度 > 60 ug/dL 的環境所致。臨床特徵為慢性間質性腎炎,包含非特異性的腎小管萎縮、間質性纖維化,及少量的發炎細胞和動脈肥厚的現象;次要的特徵為:腎絲球的疤痕組織 (glomerular scarring),進而使得腎絲球硬化,導致腎絲球過濾率不可逆的減低。病人若為鉛中毒所引起的腎病變,常有血清肌酸酐上升的情形;但這些臨床特徵並不具有特異性,且易和慢性尿酸鹽腎病變、或高血壓腎病變混淆6,7。另外,由文獻得知血壓與鉛濃度有關,當血中鉛濃度上升為兩倍時,血壓約會上升1.0/0.6 mmHg2,7。本案例有高血壓、末期腎病等病史,因過去未察覺有鉛中毒的可能,猜測疾病可能也與鉛濃度過高有相關性。
本案例曾一度誤診為格林-巴里症綜合症,主要是因為格林-巴里症綜合症的表徵為:漸近式的運動困難、對稱性的肌肉無力、無反射或反射變慢、病人可以從輕度肌肉無力到四肢癱瘓、呼吸、眼球麻痹而危及生命。多數在2-4周開始恢復,但程度和快慢各病人差異較大8。上述表徵確實和病人入加護病房時的狀況非常相似,也和鉛中毒的特徵有相似處。當時以血漿置換術予以治療,治療10天後病情並無改善,經家屬透露想以中藥搭配治療,才發現鉛中毒的可能,因而改變了治療方向。
在鉛中毒的治療首先會採取遠離含鉛的環境,但若是血鉛濃度已大於50 ug/dL 時或有症狀出現時,則會考慮使用螫合劑,最常使用的螫合劑是 CaEDTA。CaEDTA 在1950年代就已經被發展出來,它可以有效的捉住鉛後,再由尿液排出;使用螫合劑後所排出的鉛量,是人體自然排出的20-50倍。因 CaEDTA 經由尿液排出,因此在第一次使用 CaEDTA 時必需觀察病人是否有足夠的尿量,因此建議不使用於寡尿的病人。在血鉛濃度大於20 ug/dL,但小於70 ug/dL 時,常用的劑量是靜脈輸注1g/m2/day,每8-12小時給藥,一個療程為5天,在一個療程治療完應停藥2-4天,並監測血鉛濃度;若血鉛濃度大於70 ug/dL 時,可再加上dimercaprol (BAL)9,10。
本案例雖為末期腎病,但並非寡尿型末期腎病 (表五),使用 CaEDTA 治療期間,每天尿量約為1050-2580 mL。因病人使用腹膜透析,因此劑量以 CaEDTA 500 mg qd 治療,當時因無法取得 dimercaprol (BAL) 故單用 CaEDTA 治療。在首次治療後,血鉛濃度由145.2→98.6 ug/dL,且 scr 由5.81→4.24 mg/dL,但四肢動度仍無明顯進步。但血鉛濃度已大幅下降,因此將再次以 CaEDTA 治療,經3個療程治療後,血鉛濃度由145.2→98.6→42.3→25.7 ug/dL (表四),肌肉無力情形明顯改善,且腎功能也有改善。
肆、結論
若能早期發現鉛中毒,則中毒現象為可逆的。但鉛中毒的表徵不具特異性,且血鉛濃度必需在較高濃度下才會有較明顯的表徵,例如血鉛濃度為80 ug/dL 時,才會出現較明顯的貧血和腸絞痛的情形,在大於60 ug/dL 時,神經系統、及腎功能的影響情形較為嚴重,因此在診斷上非常困難。必需藉由詳細詢問用藥史,及了解長期曝露環境,才能聯想到鉛中毒的可能。因此建議不服用來路不明的藥物,若必需長期曝露於有害的環境中,應定期追踪必要的相關檢查。
參考資料:
1. ATSDR. Toxicological Profile for Lead. US Department of Health & Human Services, Public Health Service, Agency for Toxic Substances and Disease Registry, Atlanta, GA 2007. Available at http:// www.atsdr.cdc.gov/toxprofiles/tp.asp?id=96&tid=22 (Accessed on July 20, 2011).
2. Navas-Acien A, Guallar E, Silbergeld EK, Rothenberg SJ. Lead exposure and cardiovascular disease--a systematic review. Environ Health Perspect 2007; 115: 472.
3. Rabinowitz MB. Toxicokinetics of bone lead. Environ Health Perspect 1991; 91: 33.
4. Goyer RA, Rhyne BC. Pathological effects of lead. Int Rev Exp Pathol 1973; 12: 1.
5. Nawrot TS, Thijs L, Den Hond EM, et al: An epidemiological re-appraisal of the association between blood pressure and blood lead: a meta-analysis. J Hum Hypertens 2002; 16: 123.
6. Staessen JA, Lauwerys RR, Buchet JP, et al:. Impairment of renal function with increasing blood lead concentrations in the general population. The Cadmibel Study Group. N Engl J Med 1992; 327: 151.
7. Flora G, Gupta D, Tiwari A. Toxicity of lead: A review with recent updates. Interdiscip Toxicol. 2012 Jun; 5: 47-58.
8. Yuki N, Hartung HP. Guillan-Barre syndrome. N Engl J Med 2012; 366: 2294.
9. Micromedex®2.0 Edetate Calcium Disodium
10. Shiri R, Ansari M, Ranta M. Lead poisoning and recurrent abdominal pain. Ind Health. 2007 Jun;45: 494-6.
Case Report — Lead Poisoning Developing Muscle Weakness
Jung-Fang Chen, Hue-yu Wang
Department of Pharmacy, Chi-Mei Medical Center
Abstract
The diagnosis of lead toxicity is often delayed and abdominal pain is mistaken for acute abdomen. We describe the poisoning of 50-year old female as a result of the use of traditional Chinese medicine. The patient had history of chronic kidney disease on continuous ambulatory peritoneal dialysis for five years and hypertension for seven years. She presented with one week of abdominal pain, as well as nausea, and constipation. The patient was taken to hospital and developed progressive generalized weakness and difficultly respiratory. Microcytic microchromic anemia (hemoglobin 9.3 g/dL) and high blood lead level (145.2 μg/dL) were found. A diagnosis of lead poisoning was made and course of chelating treatment started with intravenous calcium disodium ethylenedia minetetraacetate (CaEDTA). We preformed CaEDTA chelation therapy twentyl times. The blood lead level was 145.2, 98.6, 42.3, and 25.7 μg/dL, respectively. Motor neuropathy, and gastrointestinal symptoms disappeared.

