摘要
嚴重皮膚過敏反應,如史帝文生-強生症候群 (Stevens-Johnson syndrome, SJS),毒性表皮溶解症 (toxic epidermal necrolysis, TEN) 及藥物疹合併嗜伊紅血症及全身症狀 (drug reaction with eosinophilia and systemic symptoms, DRESS),皆屬於延遲反應型藥物過敏反應,常發生在不同的藥物中,其中包括一些常用的抗癲癇藥;抗癲癇藥引致的嚴重皮膚過敏反應致死率為6.49%。在台灣,芳香族抗癲癇藥是導致 SJS 及 TEN 的主因,並且為產生 DRESS 的次要原因。而抗癲癇藥中 carbamazepine 被報導為台灣最常引起 SJS/TEN 的藥物,而 phenytoin 則常導致 DRESS。因此,病人及臨床工作者除了瞭解治療前所需完成的檢查外,更須衛教病人注意相關症狀及密切監測用藥後的相關副作用,以適時的給予治療避免重大不良反應發生。
關鍵字: 嚴重皮膚過敏反應、抗癲癇藥、毒性表皮溶解症、史帝文生-強生症候群、HLA-B*1502
壹、前言
依據2014年3月台灣藥害救濟基金會中全國藥物不良反應通報中心公告不良反應之症狀排名,皮膚系統症狀仍居前五名之列;如以通報成分排名,抗癲癇藥品亦列於前二十大藥物中。抗癲癇藥所造成的不良反應皮膚黏膜所引起的反應最常見,嚴重者卻可能造成危及病人性命的情形,其中臨床上常見皮膚症狀的嚴重不良反應的即是史帝文生-強生症候群 (Stevens-Johnson syndrome) 或毒性表皮溶解症 (toxic epidermal necrolysis)。台灣長庚醫療團隊於2011年所發表的研究指出,抗癲癇藥引發嚴重皮膚過敏的個案中,發現第一線含苯環的癲癇藥 carbamazepine、phenytoin 及 lamotrigine 是最常引發嚴重皮膚過敏的藥品1。而本文將探討抗癲癇藥所引致的嚴重皮膚過敏反應其相關治療及預防。
貳、嚴重皮膚過敏反應之分類
嚴重皮膚過敏反應 (severe cutaneous adverse drug reactions, SCARs) 是一種由藥物所引起致命性的且罕見的疾病,包括(1) 毒性表皮溶解症 (toxic epidermal necrolysis, TEN);(2) 史帝文生-強生症候群 (Stevens-Johnson syndrome, SJS);(3) 藥物疹合併嗜伊紅血症及全身症狀 (drug reaction with eosinophilia and systemic symptoms, DRESS)。
一、 毒性表皮溶解症 (toxic epidermal necrolysis, TEN) 和史帝文生-強生症候群 (Stevens-Johnson syndrome, SJS)
TEN 和 SJS 雖然罕見,但是一旦發生往往會危及生命。高達70%的 TEN 和 SJS 是因藥物所造成。根據2005年 Letko E 等人回顧文獻統計,SJS 於密西根等洲及西德的發生率大約是每年每百萬人1-7.1例;TEN 於西歐及美國等區域則約為每年每百萬人0.4-1.22。
臨床症狀會發現患者皮膚起水泡、黏膜潰爛,嚴重時全身皮膚黏膜脫落,SJS 死亡率約10%,TEN 的死亡率高達30%3;即使病人存活了下來,也經常會有眼角膜沾黏受損或其他器官受損的後遺症。
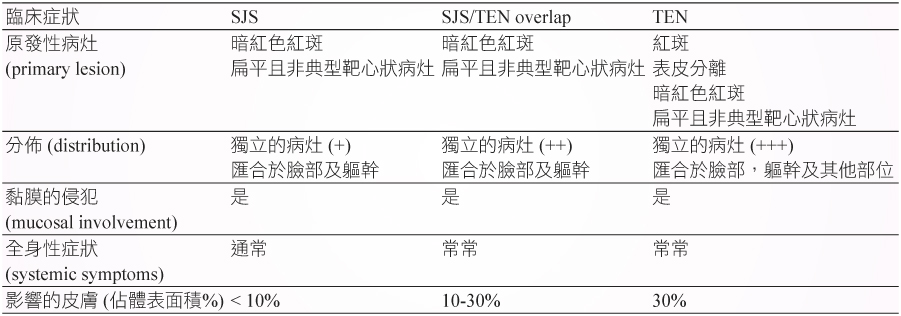
SJS 和 TEN 屬於嚴重的皮膚黏膜反應,目前認為 TEN 和 SJS 主要是激發免疫反應所造成。若受影響的皮膚體表面積在10%以下,稱之為 SJS;超過30%稱為 TEN;若介於10%-30%之間,則稱為 SJS/TEN overlap syndrome (表一)。當疾病進展到 TEN 時,造成病人死亡最常見的原因為敗血症或多重器官衰竭。
表一 SJS, SJS/TEN overlap syndrome, TEN 之臨床表徵
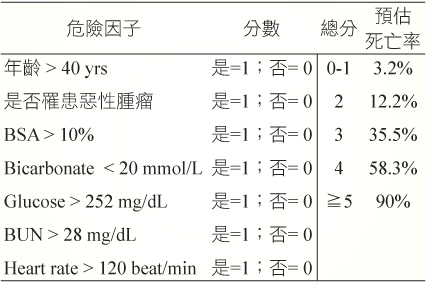
2000年 Bastuji-Garin 等人提出一套在住院24小時內以年齡、心率、惡性腫瘤病史、受影響的體表面積 (BSA, %)、血中尿素氮 (BUN)、血糖 (glucose) 與血中重碳酸根離子濃度 (bicarbonate) 等七項指標來評估病情的嚴重程度與預測死亡率 (A Severity-of-Illness Score for Toxic Epidermal Necrolysis, SCORTEN) (表二)4。若病人同時有超過五項以上的危險因子時,預估死亡率超過百分之九十。此套預測方式已被普遍認為可以準確評估 TEN 病人的病情。
表二 SCORTEN 評分
二、 藥物疹合併嗜伊紅血症及全身症狀 (drug reaction with eosinophilia and systemic symptoms, DRESS)
使用抗癲癇藥的病人發生 DRESS 的發生率約1/1,000到1/10,0002;根據研究,抗癲癇藥中如 carbamazepine、phenytoin 最常造成 DRESS 症候群。
發生此症候群的患者會出現廣泛性皮膚疹,同時常常合併有發燒、淋巴結腫大、血液異常 (包括嗜伊紅性白血球增加、非典型淋巴球增生)、內臟器官受影響 (包括肝炎、心肌炎、間質性腎炎、間質性肺炎) 等現象的藥物過敏反應的危險。紅疹和發燒通常是最常見的初始症狀,紅疹會先出現於臉部、軀幹上半部和四肢,有時甚至會造成臉部水腫。約50%的病人會出現嗜伊性白血球增加、轉氨酶 (aminotransferase)、鹼性磷酸酶 (alkaline phosphatase) 和膽紅素 (bilirubin) 數值上昇,嚴重肝炎常是造成死亡的原因。DRESS 通常出現在服藥後的1-6個星期,死亡率約10%3。
截至目前為止,醫界對於造成 DRESS 症候群的原因還不十分清楚,但是有許多證據顯示,此症是一種藥物引起的過敏反應,且牽涉到具藥物特異性的T細胞。
參、藥物基因檢測
近年來,有許多研究報告指出基因和藥物過敏反應有強烈的相關性。2004年由台灣研究首度發現抗癲癇藥 (carbamazepine) 引起的 SJS/TEN 與華人之人類白血球抗原基因型 HLA-B*1502有強烈關聯性,自此揭開抗癲癇藥不良反應基因體研究的重要里程碑。2007年 Man CB 等人研究漢民族使用抗癲癇藥引起嚴重皮膚不良反應與 HLA-B*1502基因三者之間的關係,結果發現使用抗癲癇藥發生嚴重皮膚不良反應的病人有 HLA-B*1502基因的機率明顯比控制組高。此研究中使用抗癲癇藥引起 SJS/TEN 的病人100%都帶有 HLA-B*1502基因5。同年,美國 FDA 及台灣衛生福利部也正式公告具 HLA-B*1502基因型的病人,尤其在亞洲族群,使用 carbamazepine 時容易引發危險反應的醫療警訊。
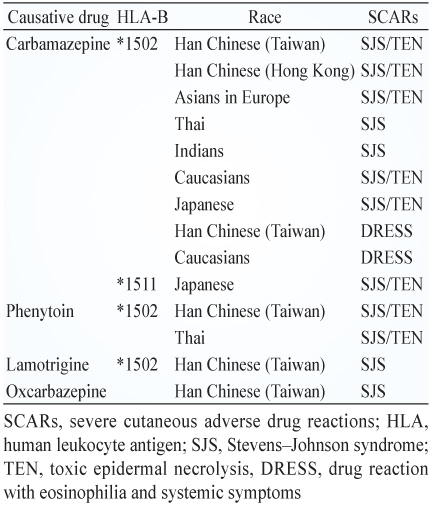
此外,針對具有苯環的芳香抗癲癇藥還包括 oxcarbazepine、phenytoin 及 lamotrigine 等也常會引起藥物過敏反應。其在華人和東南亞國家中的研究發現和 HAL-B*1502有很弱的相關 (表三),但其臨床應用價值須要再評估。
表三 HLA-B 與抗癲癇藥引發的 SCARs 之關聯性6
肆、抗癲癇藥與皮膚過敏之現況
近年來,臨床研究初步了解 HAL-B*1502
基因型為導致抗癲癇藥不良反應的元兇,故學者將更進一步致力於了解抗癲癇藥與嚴重藥物不良反應間的神祕關係。
用藥情形部分,目前台灣衛生福利部核准 Carbamazepine 或 Phenytoin 成分製劑之藥品仿單中均以載明該藥品可能導致致命之 SJS 或 TEN,通常在服藥初期的7-21天出現皮膚疹,而服藥後60天內可能誘發 DRESS,儘早停藥後可以緩解。
2013年由 Kim JY 等人針對韓國老人使用抗癲癇藥產生嚴重皮膚不良反應的風險評估研究,結果顯示使用抗癲癇藥病人產生的風險是控制組的三倍,且使用 carbamazepine 具有較高的風險存在7。在台灣,2008年 Gau SS 等人探討雙極性患者使用 valproate 及 carbamazepine 與嚴重皮膚不良反應的分析研究中指出,valproate 與 carbamazepine 可顯著預測嚴重皮膚不良反應的發生,且沒有年齡或性別的影響8。
在目前的臨床報告中,新一代抗癲癇藥中 lamotrigine 近來有愈趨增加引起嚴重皮膚過敏反應的報導。Joseph R. Calabrese 等人的研究中指出 lamotrigine 產生嚴重皮膚過敏反應易發生在治療後的8週內。此與起始劑量及增加劑量的速度是相關9。Lamotrigine 與 oxcarbazepine 也出現交叉反應現象。2011年美國 FDA 提醒臨床工作者使用 gabapentin 產生 DRESS7。
一般來說,使用藥物到發病大約有從數日到3週不等的潛伏期 (incubation time),平均潛伏期為2週10。以使用藥物時間與事件發生的關連性層面來看,2011年 Yang CY 等人針對亞洲人的研究中指出,carbamazepine 的潛伏期約12.32 ± 5.07天,而其他抗癲癇藥 (lamotrigine, oxcarbazepine, phenobarbital,及 phenytoin) 則 ≦ 27天。整體而言,在服用抗癲癇藥平均約20天易引發 SJS/TEN 或 DRESS,故服藥後仍需請病人觀察其皮膚反應,以避免重大不良反應發生1。
伍、處置、治療
目前對於治療共識是停止可能的致病藥物、在疾病的過程中給予適當的支持療法與積極的停止或減緩疾病進展三大方向。
首先,詳細回顧病人的藥物史是一很重要的步驟,且應立即停掉可疑的致過敏藥物;針對半衰期較長的藥物,停用的效果可能有限,故可再運用透析 (dialysis) 或其他體外血液淨化技術 (extracorporeal blood purification techniques)。除了立刻停用致病藥物之外,還必須禁用與致病藥物可能有交叉反應的藥物。
如同急重症與外傷的病人一樣,必須補充足夠的水份與維持體內體液與離子的平衡,並仔細監測是否有休克與器官衰竭的徵兆,在早期便可以給予適當的處置。
關於積極藥物治療方面,corticosteroids 是治療的主要方式之一,然而目前對於用在 SJS/TEN 病人之臨床價值仍有爭議。相關文獻提出使用固醇類可減緩發炎反應,減輕臨床症狀,但另一方面也可能造成癒合遲緩,增加感染機率,胃腸道出血和死亡率等因素11。另一份研究指出使用 corticosteroids 雖不會增加死亡率卻會延長病程12,故尚需進一步的研究來證實。目前,臨床上對於 corticosteroids 的療程大同小異,其中 Wolf 及 Verma 等人提出治療 TEN/SJS 病人短期連續給予3天 dexamethasone (1.5-2 mg/kg/daily) 的高劑量脈衝療法11,13。其它藥品如 cyclophosphamide、cyclosporin、IVIG 等也被報告可成功地降低 SJS 和 TEN 之死亡率11。在 DRESS 的治療部分,建議給予長期連續2-3個月口服投與 prednisolone 1-2 mg/kg 作為治療首選13。
陸、結論
同屬芳香族的 carbamazepine、phenytoin 與 phenobarbital 被報告有交叉反應,當病人因其中一種藥品引起不良反應症狀時,在抗癲癇藥的使用也必須避開另外兩類,應選擇 benzodiazepine 類或非芳香族的抗癲癇藥如:valproate、lamotrigine 或 felbamate 較為恰當。
目前諸多研究者已證實,HLA-B*1502與 carbamazepine 的強烈相關性。自100年6月起,針對初次處方 carbamazepine 者 HLAB*1502的基因檢測,希望藉由基因檢測在使用前能先篩選出高危險群,進而避免嚴重藥物不良反應的發生。而藥師對於病人初次接受抗癲癇藥治療時,也應進一步衛教病人注意皮膚方面症狀,當有不舒服情況時,應進一步諮詢醫師或藥師,以避免更重大的傷害發生。
Antiepileptic Drugs Related Severe Cutaneous Adverse Reactions
Ching-Hui Yen1, Wang-Chun Chen1, Yan-Tang Wang2, Mei-Fang Lin1
Department of Pharmacy1, Department of Neurology, E-Da Hospital2
Abstract
Severe cutaneous adverse drug reactions (SCARs), such as Stevens-Johnson syndrome (SJS), toxic epidermal necrosis (TEN), and drug rash with eosinophilia and systemic symptoms (DRESS) are delayed-type drug hypersensitivity reactions. They occured in associated with different medications, including some commonly used antiepileptic drugs (AEDs). The mortality rate of AED-SCARs were 6.49%. In Taiwan, it seems that aromatic AEDs is the main cause for SJS and TEN, and is a secondary reason for DRESS occurred. Among those AEDs, carbamazepine is the most common drug to cause SJS/TEN, and DERSS usually caused by phenytoin.
In order to provide proper medical care and avoid severe adverse drug reactions, the patients should not only know to carry out some laboratory test before taking these agents, but also need to know these ADEs related symptoms and close monitor these drugs related side effects after taking these anti-epileptic agents.
參考資料:
1.Yang CY, Dao RL, Lee TJ et al: Severe cutaneous adverse reactions to antiepileptic drugs in Asians. Neurology. 2011; 77(23): 2025-33.
2. Smith, JD: Drug-induced skin disorders. US Pharm. 2012; 37(4): HS11-HS18.
3. Yang MS, Kang MG, Jung JW et al: Clinical features and prognostic factors in severe cutaneous drug reactions. Int Arch Allergy Immunol. 2013; 162(4): 346-54.
4. Bastuji-Garin S, Fouchard N, Bertocchi M et al: SCORTEN: A severity-of-illness score for toxic epidermal necrolysis. J Invest Dermatol 2000; 115: 149-53.
5. Hazin R, Ibrahimi OA, Hazin MI et al: Stevens-Johnson syndrome: pathogenesis, diagnosis, and management. Ann Med. 2008;40:129-38.
6. Aihara M. Pharmacogenetics of cutaneous adverse drug reactions. J Dermatol. 2011; 38(3):246-54.
7. Kim JY, Lee J, Ko YJ et al: Multi-indication carbamazepine and the risk of severe cutaneous adverse drug reactions in Korean elderly patients: a Korean health insurance data-based study. PLoS One. 2013; 8(12): e83849.
8. Gau SS, Chao PF, Lin YJ et al: The association between carbamazepine and valproate and adverse cutaneous drug reactions in patients with bipolar disorder: a nested matched case-control study. J Clin Psychopharmacol. 2008; 28(5): 509-17.
9. Buzan RD, Dubovsky SL. Recurrence of lamotrigine-associated rash with rechallenge (letter). J Clin Psychiatry 1998; 59: 87.
10. Roujeau JC, Stern RS. Severe adverse cutaneous reations to drugs. N Engl Med 1994; 331: 1272-85.
11. Wolf R, Davidovici B. Severe cutaneous adverse drug reactions: who should treat, where and how?: Facts and controversies. Clin Dermatol. 2010; 28(3): 344-8.
12. Lee HY, Dunant A, Sekula P et al: The role of prior corticosteroid use on the clinical course of Stevens-Johnson syndrome and toxic epidermal necrolysis: a case-control analysis of patients selected from the multinational EuroSCAR and RegiSCAR studies. Br J Dermatol. 2012; 167(3): 555-62.
13. Verma R, Vasudevan B, Pragasam V. Severe cutaneous adverse drug reactions. Med J Armed Forces India. 2013; 69(4): 375-383.

