摘要
晚期前列腺癌的第一線治療選擇為荷爾蒙療法。由於前列腺癌的惡化除了受到睪固酮的影響之外,還會受到腎上腺所分泌之雄激素的影響,因此才有了合併雄激素阻斷法 (combined androgen blockade) 的出現,然而合併雄激素阻斷法的效果在1990年代仍未被確立。近年來一些大型統合分析則顯示,相較於單一療法,使用非固醇類的抗雄激素受體阻斷劑 (non-steroidal androgen receptor antagonist) 的合併療法,在存活率上有著微小但具統計上差異的成效。然而,在長期使用上,須考量合併雄激素阻斷法可能帶來更多的副作用。本文章即是回溯過去的研究,探討此療法在晚期前列腺癌上的成效。
關鍵字: 晚期前列腺癌、雄激素剝奪療法、去勢作用、促性腺激素釋放荷爾蒙致效劑、抗雄激素藥物、合併雄激素阻斷法
壹、前言
前列腺癌 (攝護腺癌) 是最常發生於男性的非皮膚惡性腫瘤,是一種前列腺細胞不正常增生的疾病。根據衛生福利部的統計資料顯示1,前列腺癌為十大癌症死因的第七名,占率為2.7%。與西方國家相比,雖然亞洲男性前列腺癌的發生率與死亡率都低很多,但隨著飲食習慣的改變和人口的老化,前列腺癌的發生率也有逐步上升的趨勢2。由於晚期前列腺癌多半具有轉移的情形,無法以手術或是定點放射線治療根除,因此荷爾蒙療法便成為最主要之治療方式。自1980年代以來,由於發現使用手術或是藥物達成去勢 (castration) 的效果後,前列腺仍會受到腎上腺所分泌之雄激素的影響,因此才有了合併療法的出現。然而對於合併療法在晚期前列腺癌的治療地位仍沒有定論。
貳、治療
前列腺癌的治療目標共有三個取向,除了防止疾病進一步惡化 (提早死亡和失能) 之外、也須控制症狀,並提高病人的生活品質達最大限度。至於如何選擇治療方式則取決於病人的年齡、預期壽命、健康狀況、是否適合進行手術、腫瘤分期、是否具有轉移性、疾病的預後以及病人的偏好。而前列腺癌細胞對於雄性激素的依賴關係,使得雄激素剝奪療法 (androgen deprivation therapy, ADT) 成為前列腺癌治療的最主要方式,可藉由手術或是藥物治療來達成。
由於藥物在投與的方便性,以及病人對於手術的接受度仍有所考量,因此藥物在晚期前列腺癌的雄激素剝奪療法當中,佔有相當重要的地位。目前的藥物治療以促性腺激素釋放荷爾蒙致效劑 (gonadotropin-releasing hormone agonist, GnRH agonist),又稱作促黃體素釋放荷爾蒙致效劑 (luteinizing hormone-releasing hormone agonist, LHRH agonist),以及抗雄激素藥物 (antiandrogen) 所領導的荷爾蒙療法為主 (圖一)。
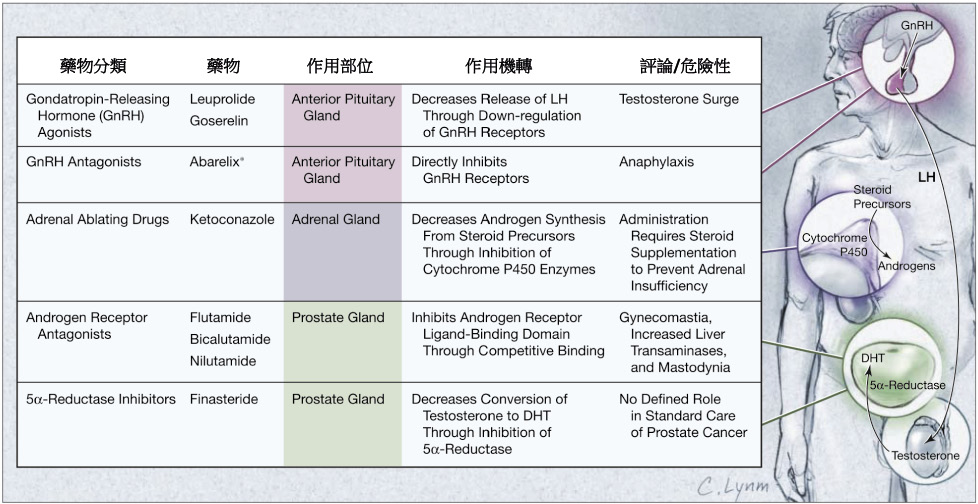
圖一 前列腺癌荷爾蒙治療藥物簡介3
參、荷爾蒙療法
大約在70年前,Huggins 等人首次報告了荷爾蒙療法對轉移性前列腺癌的影響4。過去的研究發現前列腺癌是雄激素依賴性,95%的雄激素是來自於睾丸的睪固酮 (testosterone)。睪固酮是維持正常、健康的前列腺上皮細胞所必需的物質,但它同時也是一個發展成前列腺癌的先決條件。雄激素被認為能夠藉由結合在前列腺癌細胞的雄激素受體,進而促進癌細胞的生長。藥物的作用便是根據這個原理,降低人體內血中睪固酮的濃度,而進一步抑制癌細胞的生長。
一、促性腺激素釋放荷爾蒙致效劑
此類的藥品有 leuprolide 和 goserelin,可作用在腦下垂體前葉向下調控 GnRH 受體,降低促黃體素 (luteinizing hormone, LH) 的釋放並減少睪固酮的生成。歐洲泌尿科協會指引指出5,GnRH 致效劑因為下列幾個理由目前已經成為應用在前列腺癌的標準療法:(一)具有潛在的可逆性而且能使用間歇性雄激素剝奪 (intermittent androgen deprivation, IAD) 的方式作為治療。(二)可以避免因為睾丸切除術 (orchiectomy) 所產生的生理和心理不適。(三)和 diethylstilbestrol 相比具有較低的心臟毒性風險。(四)具有相當的腫瘤治療效果。
然而 GnRH 致效劑在使用的初期會暫時性地導致睪固酮增加,此時可能加重轉移性前列腺癌的惡化,如骨頭疼痛和膀胱阻塞等。因此須仔細評估病人的情況是否適合使用,或是併用抗雄激素藥物 (antiandrogen) 來減輕此副作用6。
二、抗雄激素藥物
又稱做雄激素受體阻斷劑 (androgen receptor antagonist),藉由與前列腺細胞上的雄激素受體結合,達到阻斷雄激素的作用。依照其結構分為固醇類 (如 cyproterone) 及非固醇類 (如 flutamide, bicalutamide, nilutamide) 兩種。除了由睪丸所分泌的睪固酮之外,從腎上腺分泌的去氫皮質酮 (dehydroepiandrosterone, DHEA) 和雄烯二酮 (androstenedione) 也會刺激前列腺癌細胞的增生 (圖二)7。由於抗雄激素藥物不影響血中睪固酮的濃度,即無法達成去勢的效果,因此並不作為第一線療法使用。但其受體阻斷的作用可以預防 GnRH 致效劑的副作用及加強雄激素剝奪療法的效果。因此使用手術或是藥物的去勢療法,再利用抗雄激素藥物抑制源自腎上腺的雄激素與前列腺癌細胞的雄激素受體結合,也許可以更有效地阻斷前列腺癌的惡化。
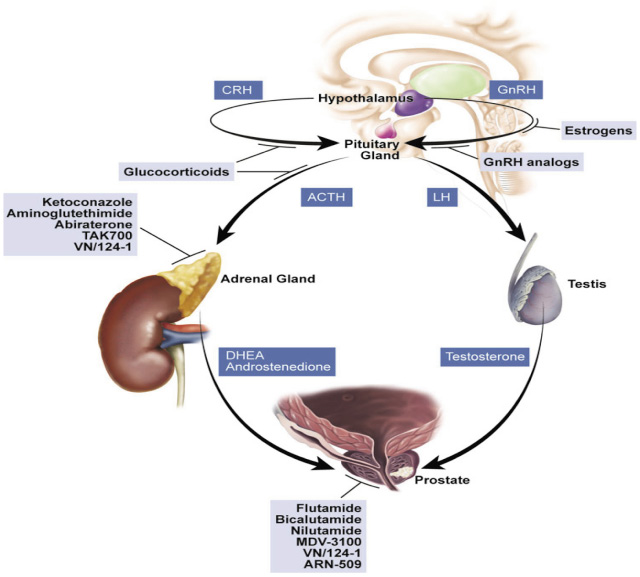
圖二 下視丘-腦垂腺-腎上腺軸7
三、合併雄激素阻斷法
自1970年代結束以後,合併雄激素阻斷法 (combined androgen blockade, CAB) 就以作為一種治療前列腺癌的方法而被研究。其方法為利用手術或藥物達到去勢的效果,再合併使用抗雄激素藥物。1990年代已有相當多隨機分派試驗和統合分析試著去評估其效益。然而它的治療地位一直未被確立,原因在於並非所有的研究都指出合併療法一定比單一療法較好8。近年來有幾個大型的隨機分派試驗及統合分析試著去證明這件事:(一)1998年受試者共30853人的 EORTC 隨機分派試驗指出9,goserelin 加上 flutamide 的合併療法與睪丸切除術相比,整體存活率顯著地偏向合併療法的使用 (34.4 vs. 7.1 months, p = 0.008)。(二)2000年 PCTCG 統和分析 (共收入27個隨機分派試驗,8275個病人) 指出10,合併療法和單一療法相比,兩組在整體的存活率並沒有差異。然而將7篇合併使用 cyproterone 的試驗排除後重新分析,結果顯示在五年存活率上,合併療法相較於單一療法是有統計上的顯著差異 (27.6% vs. 24.7%, p = 0.005)。(三)2001年有一篇系統性回顧 (共收入20個隨機分派試驗,6320個病人) 發現11,利用非固醇類的抗雄激素做合併療法和單一療法,結果數據雖小 (5%),但具統計上的顯著差異。(四)2002年另一篇統和分析 (收入21個隨機分派試驗,6871個病人) 卻顯示12,合併療法與單一療法相比,兩組在兩年存活率上並沒有統計上的顯著差異 (HR = 0.970, 95% CI = 0.866-1.087)。而作者在其中的10個試驗再次進行了統合分析,得到的結果是合併療法較單一療法在五年存活率上,有統計上的顯著差異 (HR = 0.871, 95% CI = 0.805-0.942)。
綜合以上結果,這些微小的統計上的顯著差異是否代表合併療法一定比單一療法較好,目前仍有爭議的空間,因為仍須考量合併療法較單一療法可能帶來更多的副作用。不過可以得知的是,似乎合併使用固醇類相較於非固醇類的抗雄激素藥物有著較差的存活率。
最近的研究顯示8,13,患有前列腺癌的日本男性使用 bicalutamide 80毫克作為合併療法,可以提高病人的存活率,卻沒有安全性及生活品質變差的疑慮。然而,使用 bicalutamide 作為合併治療的組別,較 flutamide 可以增加存活率。有一篇中國的回溯性研究結果亦同2。由於受試者族群的差異,1990年代的研究對象多為高加索人,bicalutamide 的研究對象多為亞洲人,這個結果似乎顯示「種族」的影響對於合併療法的效果可能也是一個主要原因8。美國臨床腫瘤協會 (American Society of Clinical Oncology, ASCO) 在2007年修正了治療指引14,將 bicalutamide 80毫克納入作為合併療法可以選擇之抗雄激素藥物。因此目前對於合併療法的研究報告傾向於併用非固醇類的抗雄激素藥物有著較好的療效。值得注意的是,雖然 bicalutamide 有著不錯的效果以及較少的副作用,但在台灣目前並沒有核准80毫克的劑型。再者 bicalutamide 尚缺乏大型的臨床試驗去證明其療效和安全性,仍待進一步的研究證實。
肆、副作用15
雄激素剝奪療法常見的副作用有體重減輕、疲勞、男性女乳症、熱潮紅及性慾低下。然而其所引起的性腺低下症,已被證實與骨密度的流失有關,使得骨折的風險成為使用此法須要考量的事情。骨密度的流失在開始治療的六到十二個月快速的發生,之後便慢慢減緩。一個回溯性,超過5000名前列腺癌受試者的研究分析指出,以雄激素剝奪療法治療的病人與未治療的病人相比,骨折的發生率,治療組較未治療組來的高 (19.4%:12.6%),骨折病人的死亡率則是未骨折的兩倍。其它的副作用包括:代謝症候群、胰島素阻抗性、糖尿病、肥胖、脂質代謝異常,都和性腺低下症相似。由於高血壓、高血糖及高血脂可能與心血管疾病風險有關,因此相關的議題也持續地被探討。根據美國食品藥物管理局針對目前已發表的文獻進行回顧,發現 GnRH 致效劑可能增加糖尿病、心臟病、中風和猝死的風險。相反地,多數的研究顯示睪丸切除術並不會增加心血管疾病的發生率。至於使用雄激素剝奪療法或合併療法是否必然會增加心血管疾病風險,目前仍不明確。但已有文獻指出合併療法在長期使用下對於性功能、認知功能以及體溫調節方面可能有著更差的生活品質5。
伍、結論
總結來說,在1990年代合併療法對於單一療法,尚無法看出其臨床效益。然而,造成這個結果的原因可能與試驗所選擇的藥物以及受試者有關。原因在於當時可用的藥品選擇不多,再者並沒有前列腺特異性抗原 (PSA) 的測試可用於篩選攝護腺癌的嚴重度。近年已經有一些研究顯示,合併療法對於轉移性前列腺癌有其臨床上的效益存在,尤其是在併用非固醇類抗雄激素藥物的情況下。在副作用方面,雄激素剝奪療法與心血管疾病的風險之間的關係目前無法確立,然而與性腺低下有關的代謝症候群仍可能發生。因此對於本身已有心血管疾病的病人來說,在使用荷爾蒙療法的期間宜定期回診進行追蹤。此外,可以預期的是合併療法比單一療法在長期使用的情況下,可能會產生更多的副作用,使用前應仔細評估。
Combined Androgen Blockade for Advanced Prostate Cancer
Chang-Ming Chen
Department of Pharmacy, Taipei City Wanfang Hospital
Abstract
Hormone therapy is the first-line treatment for advanced prostate cancer. Due to the deterioration of prostate cancer affected by testosterone and androgens secreted by adrenal glands, the treatment called combined androgen blockade (CAB) appeared. In the 1990s, the efficacy of CAB has not been confirmed. In recent years, comparing to the monotherapy of surgical or medical castration, some large meta-analysis found statistically significant but small difference in survival that favored combined androgen blockade with non-steroidal androgen receptor antagonist. On the other hand, CAB may lead to more side effects in the long-term use. This article focused on the efficacy of CAB for advanced prostate cancer.
參考資料:
1.行政院衛生福利部:民國101年國人主要死因統計結果。臺北:衛生福利部,2013。
2. Chen XQ, Huang Y, Li X, et al: Efficacy of maximal androgen blockade versus castration alone in the treatment of advanced prostate cancer: a retrospective clinical experience from a Chinese medical centre. Asian J Androl 2010;12:718-27.
3. Sharifi N, Gulley JL, Dahut WL: Androgen deprivation therapy for prostate cancer. JAMA 2005;294:238-44.
4. Huggins C, Hodges CV: Studies on prostatic cancer: I. The effect of castration, of estrogen and of androgen injection on serum phosphatases in metastatic carcinoma of the prostate. Cancer Res 1941;1:293-7.
5. Heidenreich A, Bastian PJ, Bellmunt J, et al: EAU guidelines on prostate cancer. Part II: Treatment of advanced, relapsing, and castration-resistant prostate cancer. Eur Urol 2014;65:467-79.
6. Loblaw DA, Mendelson DS, Talcott JA, et al: American Society of Clinical Oncology recommendations for the initial hormonal management of androgen-sensitive metastatic, recurrent, or progressive prostate cancer. J Clin Oncol 2004;22:2927-41.
7. Alva A, Hussain M: Optimal pharmacotherapeutic management of hormone-sensitive metastatic prostate cancer. Drugs 2013;73:1517-24.
8. Akaza H: Combined androgen blockade for prostate cancer: review of efficacy, safety and cost-effectiveness. Cancer Sci 2011;102:51-6.
9. Denis LJ, Keuppens F, Smith PH, et al: Maximal androgen blockade: final analysis of EORTC phase III trial 30853. EORTC Genito-Urinary Tract Cancer Cooperative Group and the EORTC Data Center. Eur Urol 1998;33:144-51.
10. Prostate Cancer Trialists' Collaborative Group: Maximum androgen blockade in advanced prostate cancer: an overview of the randomised trials. Lancet 2000;355:1491-8.
11. Schmitt B, Wilt TJ, Schellhammer PF, et al: Combined androgen blockade with nonsteroidal antiandrogens for advanced prostate cancer: a systematic review. Urology 2001;57:727-32.
12. Samson DJ, Seidenfeld J, Schmitt B, et al: Systematic review and meta-analysis of monotherapy compared with combined androgen blockade for patients with advanced prostate carcinoma. Cancer 2002;95:361-76.
13. Akaza H, Hinotsu S, Usami M, et al: Combined androgen blockade with bicalutamide for advanced prostate cancer: long-term follow-up of a phase 3, double-blind, randomized study for survival. Cancer 2009;115:3437-45.
14. Loblaw DA, Virgo KS, Nam R, et al: Initial hormonal management of androgen-sensitive metastatic, recurrent, or progressive prostate cancer: 2006 update of an American Society of Clinical Oncology practice guideline. J Clin Oncol 2007;25:1596-605.
15. Chi KN, Nguyen PL, Higano CS: Androgen deprivation for prostate cancer: when and how, the good and the bad. Am Soc Clin Oncol Educ Book 2013.

