摘要
蛋白質流失腸病變 (protein-losing enteropathy, PLE) 的特色為血清中蛋白質經由腸道過度流失,臨床表現為出現低蛋白血症 (hypoproteinemia)、低白蛋白血症 (hypoalbuminemia)、水腫、吸收不良、體重減輕、電解質失衡,甚至可能出現腹水 (ascites)、肋膜積液 (pleural effusion) 或心包膜積液 (pericardial effusion) 等症狀。有許多原因可能引起 PLE,大多不引起臨床嚴重症狀,但當中以原發性小腸淋巴管擴張症 (primary intestinal lymphangiectasia)、自體免疫疾病、先天性心臟病術後等原因所導致的 PLE,常伴隨極高的死亡率。近年來雖然 PLE 的治療有進一步的改善,但仍是臨床很難治療的疾病,盼透過臨床治療成功的案例提供予 PLE 處置參考,以幫助改善病人預後。
關鍵字: 蛋白質流失腸病變、低白蛋白血症、水腫、protein-losing enteropathy (PLE)、hypoalbuminemia、edema
壹、前言
蛋白質流失腸病變是一種複雜的疾病,有許多原因可能引起 PLE,通常大多不引起臨床嚴重症狀,但當中以原發性小腸淋巴管擴張症 (primary intestinal lymphangiectasia)、先天性心臟病術後、自體免疫疾病 (如:紅斑性狼瘡)、右心衰竭等原因所導致的 PLE,常伴隨極高的死亡率。PLE 主要表現特色為血清中蛋白質經由腸道過度流失1。PLE 臨床表徵為出現低蛋白血症 (hypoproteinemia)、低白蛋白血症 (hypoalbuminemia)、水腫、腹瀉、體重減輕、電解質失衡,甚至可能出現腹水 (ascites)、肋膜積液 (pleural effusion) 或心包膜積液 (pericardial effusion) 等症狀。其臨床檢驗主要發現於血清中白蛋白 (albumin)、免疫球蛋白 (IgA, IgG, IgM)、fibrinogen、transferrin、ceruloplasmin 濃度會下降,但無蛋白尿 (proteinuria) 的症狀。低白蛋白血症會造成下肢末梢水腫。小腸原發性疾病所致的低蛋白血症可能也與脂肪、碳水化合物吸收不良、脂溶性維生素缺乏有關2。若因心臟疾病所致之繼發性 PLE,最常見的原因跟系統或/及中央靜脈壓上升有關1。
貳、致病因2
人體胃腸道並不顯著提供血漿蛋白質的分解作用,正常情況下 albumin 與免疫球蛋白在胃腸道大約只有10%的流通量,一旦血漿蛋白質通過胃腸道便會快速降解成胺基酸並進入肝門循環再吸收。PLE 就是因血漿中蛋白質經胃腸道滲出增加所引起的疾病。導致 PLE 的致病因可概分為三類:
一、發炎性滲出
因黏膜遭受侵蝕或潰瘍所致的發炎性滲出,如:克隆氏症 (Crohn's disease)、潰瘍性結腸炎 (ulcerative colitis)、長期使用 nonsteroidal anti-inflammatory drug (NSAID) 藥物、胃腸道惡性腫瘤、侵蝕性胃炎或多發性胃潰瘍等疾病所致。
二、無侵蝕或潰瘍表現之黏膜性疾病
由於黏膜性疾病導致胃腸道通透性增加,但並無侵蝕或潰瘍存在,如:胃粘膜巨大肥厚症 (menetrier's disease)、紅斑性狼瘡 (systemic lupus erythematosus)、風濕性關節炎 (rheumatoid arthritis)、感染等因素所致。
三、淋巴管阻塞
因淋巴管阻塞致使淋巴液經腸道流失、腸道淋巴管的壓力增加,如:原發性小腸淋巴管擴張症 (primary intestinal lymphangiectasia)、右心衰竭、先天性心臟病、fontan operation (針對單一心室循環患者的心臟手術) 術後、腸系膜靜脈血栓 (mesenteric venous thrombosis) 等因素所致。其中臨床上有許多 fontan operation 術後發生 PLE 的相關研究,fontan operation 術後幾年發生 PLE 約有5-15%的比率,而診斷 PLE 後報告指出5年內死亡率約達50%。
參、診斷流程與臨床評估2
當懷疑患者可能有 PLE 時,可透過以下診斷流程來判定致病原因 (圖一)。
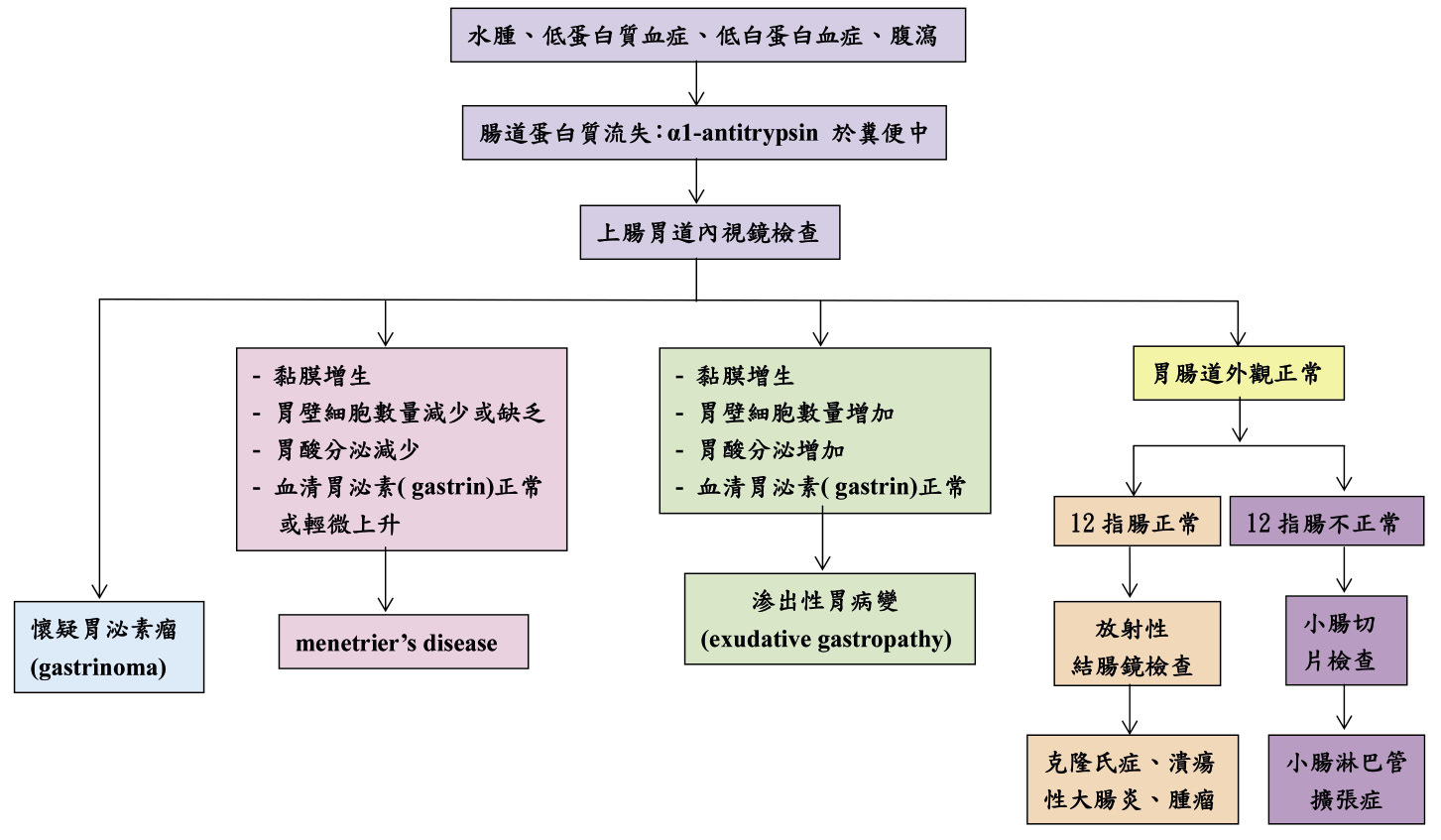
圖一 蛋白質流失腸病變 ( protein-losing enteropathy, PLE) 的描述與評估2
不同原因造成的 PLE 在實驗室檢查值皆類似,同樣會出現血清檢驗值 albumin、IgA, IgG, IgM、fibrinogen、transferrin、ceruloplasmin 濃度下降的情況。要確認 PLE 診斷前應先排除營養不良、嚴重蛋白尿或歸因於肝疾病所致之蛋白質合成不良等原因。原發性小腸淋巴管擴張症 (primary intestinal lymphangiectasia) 可透過臨床表徵、實驗室檢查值與病理發現來確認診斷。實驗室檢查值除上述血清檢驗值會降低外,也經常發生凝血因子減低及淋巴細胞經腸道流失導致淋巴細胞減少症 (lymphocytopenia) 的情況。病人若出現脂肪痢 (steatorrhea) 可能會造成脂溶性維生素缺乏。一般而言,胃腸道黏膜有/無遭受侵蝕或潰瘍所致的蛋白質流失,通常不會對病人造成嚴重的影響,但在淋巴管阻塞型 (lymphatic obstruction) 病人,尤其是先天性淋巴管擴張症 (congenital lymphangiectasia),其淋巴細胞經腸道流失顯著造成淋巴細胞減少 (lymphocytopenia) 可能影響到細胞免疫能力而惡化病人預後。
肆、PLE 治療
一、飲食治療
PLE 患者主要飲食治療建議在於需提供低脂肪、高蛋白 (大於2 g/kg/天)、中鏈三酸甘油脂 (medium-chain triglyceride) 的補充飲食,目的在減少腸道蛋白質損耗和改善營養狀況。有些患者可能尚須鈣鹽、水溶性與脂溶性維他命的額外補充1。
二、潛在疾病治療
絕大部分的患者可能都須透過手術來處理局部性腸道疾病或縮窄性心包炎 (constrictive pericarditis) 以緩解蛋白質的流失,而各種因應個別病人主要潛在疾病的治療也是關係到病人預後的重要處置2。
三、輔助性藥物治療
(一)Albumin
Albumin 的補充用以校正低白蛋白血症,唯即使補充 albumin 若仍不足以讓患者 albumin 的血清數值恢復正常,首要除潛在疾病的治療外,必要時也可能需合併使用下述輔助用藥以期使改善 PLE 症狀3。
(二)Heparin
Heparin 是葡萄糖胺多醣體 (glycosaminoglycan) 之混合物,藥物作用是藉著與抗凝血酶 III (antithrombin III) 結合而引發快速的抗凝血反應。Heparin 用於治療 PLE 的經驗顯示,其緩解臨床徵兆所需的作用時間會較延遲,改善 PLE 的機轉不明,相關案例報告研究建議 heparin 用於 fontan operation 術後 PLE 有改善臨床徵狀及蛋白質流失的效果4,5。然而長期或間歇性給予 heparin,可能導致 antithrombin III 活性降低而增加栓塞風險,建議以低劑量之 heparin 作治療以防止此現象發生。在一案例研究報告中發現,於3位行 fontan operation 數年後發生 PLE 的兒科患者,經飲食、類固醇等治療無效後嘗試以 heparin 治療,於發現 heparin 開始治療幾個星期後 (約3星期) 患者症狀都有顯著改善,諸如:albumin 值上升、α1-antitrypsin 值回復正常、逆轉腸道蛋白質的流失、解除水腫等作用,研究發現高劑量的 heparin 有造成背痛、骨質缺乏 (osteopenia)、骨折的副作用,因此建議使用 heparin 5,000 units/m2的初始劑量,再計畫性的逐步調降至個別病人之最低有效劑量。研究結論認為 heparin 對於 PLE 治療應該扮演著重要的角色4。在另一案例報告中,患者接受包括:飲食、albumin 輸注、利尿劑 (furosemide)、類固醇給予等治療無效後,開始 heparin 5,000 units/day 治療一個月後,其周邊水腫、腹水、慢性肺浸潤皆有顯著改善,生化檢驗值如:albumin、α1-antitrypsin 值皆逐漸恢復正常,是另一成功治療 PLE 的案例5。
(三)Corticosteroid
發炎反應被認為也是導致 PLE 的原因之一,所以給予皮質類固醇 (corticosteroid) 治療可能會有益處。研究也證實給予 prednisone 1-2 mg/kg/天對改善 PLE 症狀是有幫助的,但長期使用全身性作用的類固醇,可能造成顯著副作用,包括:體重增加、高血壓、高血糖、骨質疏鬆、感染等併發症。口服 budesonide 是選擇性作用於腸道黏膜的類固醇,通常較無全身性副作用,口服 budesonide 建議劑量為6-9 mg/kg/天,研究發現 budesonide 確實對提高血清 albumin 值有良好的效果,雖然對所有研究的病人其臨床徵狀都有改善,但是一旦停止使用,其 PLE 症狀又會再度回復,所以研究建議可能需長期低劑量給予來維持其療效6。目前口服劑型 budesonide 台灣並未進口,若長期使用 budesonide 需監測可能造成肝毒性、高血糖、高血壓等副作用。
(四)Octreotide
Octreotide 屬於 somastatin analogue,臨床上有案例報告使用 octreotide (200μg,一天兩次) 成功減低腸道蛋白質流失並改善臨床症狀。在一篇收納3名 fontan operation 術後 PLE 案例報告中指出,以 octreotide 給予此3名患者;案例1同時給予口服 budesonide 與 octreotide (Sandostatin LAR DEPOT) 20 mg/月,因 budesonide 引發庫欣氏症候群 (Cushing's syndrome) 及腎上腺機能不足 (adrenal insufficiency) 副作用而停止,而 octreotide 仍持續給予。案例2在 fontan operation 術後 PLE 以飲食治療及 heparin 治療控制效果成效良好,於3年後復發才給予 octreotide (Sandostatin LAR DEPOT) 10 mg/月治療。案例3則是在症狀惡化後給予 octreotide (Sandostatin 50 μg)/一天三次。3名患者在 octreotide 開始治療後,腹瀉及體液滯留的症狀都有改善,研究投予時間為14-28個月,而血清 albumin 值於治療前2.3-2.5 g/dL顯著進步至2.9- 3.3 g/dL。唯案例3因膽結石症狀持續進展而中斷治療,並於停止治療後7個月因敗血症死亡,研究結論認為 octreotide 對於 fontan operation 術後 PLE 的患者可能是有療效的治療7。Octreotide 也被使用於原發性小腸淋巴管擴張症的 PLE 患者治療,但研究證據仍相當有限8。對於 octreotide 減低腸道蛋白質流失的作用機轉並不清楚,被認為可能與減少內臟、淋巴管血流而減低了淋巴管壓力有關。Octreotide 用於 PLE 理想治療劑量並未確立,且研究認為 octreotide 不應當成起始治療,只可當成輔助療法。Octreotide 的使用亦須注意有可能會增加膽結石形成 (22-33 %)3。
(五)Sildenafil
臨床上 PLE 治療需盡可能降低高中心靜脈壓 (central venous pressure, CVP),即使患者狀態看似穩定亦然,尤其是 CVP ≥ 12 mmHg,在 PLE 研究報告中建議若患者持續高肺血管阻力,則治療策略可能須包括肺血管擴張劑,如:sildenafil (注射或口服0.5-2 mg/kg/dose/6h)。唯相關研究證據仍很薄弱,研究也顯示其在消除 PLE 症狀的附加利益也很有限,因此其角色主要仍著重在降低肺血管阻力之作用9。
(六)其它
有很多疾病可能會引起 PLE 的症狀,所以其治療藥物也很多變,在 PLE 的藥物處置介紹中常包括:利尿劑、高蛋白質-低脂飲食、albumin 輸液、類固醇等藥物的使用,但單靠這些藥物即可治療成功的仍在少數,或只是暫時緩解臨床症狀。除前述少數研究報告指出有成功治療 PLE 案例的藥物外,下述輔助用藥因應患者需要可能也扮演潛在改善病人症狀的療效。如:1.鈣:fontan operation 術後引起 PLE 的患者給予鈣補充可減少蛋白質流失,幫助總蛋白質 (total protein) 及 albumin 值回復正常10。2. Cyclosporine:自體免疫疾病 (autoimmune disease),如:硬皮病 (scleroderma) 所引起的 PLE,研究指出給予長期低劑量 cyclosporine 有成功治癒的案例11。3.利尿劑:spironolactone 有研究指出用於治療 fontan operation 術後 PLE 患者有改善效果12。其被認為可能與其改善心臟功能跟利尿的特性有關,另外也認為跟改善內皮細胞功能及減低發炎反應有相關性13。Furosemide:建議劑量1 mg/kg一天兩次,視症狀需要增加劑量。
伍、結論
PLE 引起的臨床症狀可能由輕微至極嚴重,目前仍是臨床很難治療的疾病,尤其在先天性心臟病人者 fontan operation 術後所引發的 PLE,被確認診斷後有極高的死亡率,盼透過臨床治療成功的案例提供予 PLE 處置建議參考,以幫助改善病人預後。
The Introduction and Medication Management of Protein-losing Enteropathy
Ying-Tao Wu1, Ju-Chun Shiao1, Kai-Lun Sheu2,3, Chien-Ying Lee1,3
Department of Pharmacy, Chung Shan Medical University Hospital1
Department of Family and Community Medicine, Chung Shan Medical University Hospital2
School of Medicine, Chung Shan Medical University3
Abstract
The main clinical feature of protein-losing enteropathy (PLE) is primarily characterized by excessive leakage of serum proteins into the gastrointestinal tract, resulting in common clinical manifestations such as hypoproteinemia, hypoalbuminemia, edema, malabsorption, body weight loss and electrolyte imbalance. In some rare cases, symptoms such as ascites, pleural effusion or pericardial effusion may even appear. There are many factors those might cause PLE, but most patients do not show serious clinical signs. However, for persons having primary intestinal lymphangiectasia, autoimmune disease or post-operation congenital heart disease leading to PLE, high mortality rate is frequently observed. Although the treatment of PLE has advanced greatly in recent years, this disease is still difficult to treat. Several successful clinical cases from the past can help us provide better care in managing patients with PLE.
參考資料:
1.Johnson JN, Driscoll DJ, O'Leary PW: Protein-Losing Enteropathy and the Fontan Operation. Nutr Clin Pract 2012;27:375-84.
2. Milovic V, Grand RJ: Protein-losing gastroenteropathy. Retrieved from UpToDate clinical knowledge base, institutional edition. This literature review current through 2015 Jan.
3. John AS, Johnson JA, Khan M, et al: Clinical Outcomes and Improved Survival in Patients With Protein-Losing Enteropathy After the Fontan Operation. JACC 2014;64:54-62.
4. Donnelly JP, Rosenthal A, Castle VP, et al: Reversal of protein-losing enteropathy with heparin therapy in three patients with univentricular hearts and Fontan palliation. J Pediatr 1997;130:474-8.
5. Kelly AM, Feldt RH, Driscoll DJ, et al: Use of heparin in the treatment of protein-losing enteropathy after fontan operation for complex congenital heart disease. Mayo Clin Proc 1998;73:777-9.
6. Rychik J, Piccoli DA, Barber G: Usefulness of corticosteroid therapy for protein-losing enteropathy after the Fontan procedure. Am J Cardiol 1991; 68:819-21.
7. John AS, Phillips SD, Driscoll DJ, et al: The Use of Octreotide to Successfully Treat Protein-losing Enteropathy Following the Fontan Operation. Congenit Heart Dis 2011;6:653-6.
8. Thacker D, Patel A, Dodds K, et al: Use of oral budesonide in the management of protein-losing enteropathy after the Fontan operation. Ann Thorac Surg 2010;89: 837-42.
9. Ohuchi H, Yasuda K, Miyazaki A, et al: Haemodynamic characteristics before and after the onset of protein losing enteropathy in patients after the Fontan operation. European Journal of Cardio-Thoracic Surgery 2013; 43:49-57.
10. Kim SJ, Park IS, Song JY, et al: Reversal of protein-losing enteropathy with calcium replacement in a patient after Fontan operation. Ann Thorac Surg 2004;77:1456.
11. Thacker D, Patel A, Dodds K, et al: Use of oral budesonide in the management of protein-losing enteropathy after the Fontan operation. Ann Thorac Surg 2010; 89:837.
12. Ringel RE, Peddy SB: Effect of high-dose spironolactone on protein-losing enteropathy in patients with Fontan palliation of complex congenital heart disease. Am J Cardiol 2003;91:1031-2.
13. Elinoff JM, Rame JE, Forfia PR, et al: A pilot study of the effect of spironolactone therapy on exercise capacity and endothelial dysfunction in pulmonary arterial hypertension: study protocol for a randomized controlled trial. Trials 2013;14:91.

