摘要
高血壓的疾患占孕婦的5-10%,為孕婦死亡的前三大主因之一,而引發死亡的原因,通常是因為高血壓合併子癲前症或子癲症,其發生率占孕婦的3.9%。妊娠中的高血壓,指收縮壓大於140 mmHg 或舒張壓大於90 mmHg,或妊娠後期之收縮壓比早期高30 mmHg 或舒張壓升高15 mmHg。對於輕微的妊娠高血壓病人可在家中臥床休息,服用降血壓藥物控制血壓。降血壓的藥物包含 methyldopa、labetalol、nifedipine 及 hydralazine,一旦血壓持續上升或有嚴重子癲前症的症狀出現時,則需要住院觀察及治療。嚴重的子癲前症和子癲症的病人,可以使用靜脈輸注硫酸鎂 (MgSO4) 來預防或控制痙攣的發生。硫酸鎂的作用在於抗痙攣而非降低血壓。使用硫酸鎂時,應要特別注意病人的肌腱反射 (deep tendon reflexes, DTR)、呼吸速率以及尿量,並且時常監測血清中的鎂離子濃度,以避免中毒發生。
關鍵字:gestational hypertension、preeclampsia、eclampsia、HELLP syndrom
壹、前言1
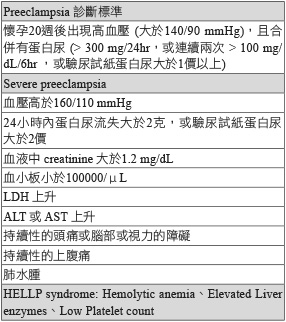
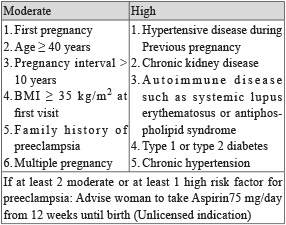
妊娠高血壓 (gestational hypertension),就是身體不能適應懷孕所引起的血液循環方面的變化而產生的疾病。妊娠高血壓是孕婦易患的疾病之中最可怕的一種,多發生於懷孕後期,約有5-6%的孕婦會罹患妊娠高血壓。依世界衛生組織的統計,在開發中的國家,有高達16%的孕婦死於高血壓所引發的疾病,是孕婦死亡率的第一位2。依 The Working Group classification of hypertensive disorders complicating pregnancy 的分類,妊娠高血壓可以分成四大類:1.妊娠高血壓;2.妊娠高血壓合併子癲前症 (preeclampsia) 或子癲症 (eclampsia);3.慢性高血壓;4.慢性高血壓合併子癲前症3。妊娠高血壓又稱為 pregnancy-induced hypertension,指懷孕20週後首次診斷出收縮壓大於140 mmHg 或舒張壓大於90 mmHg 的血壓狀況,但無合併蛋白尿。子癲前症的診斷標準 (表一)4,若有發生無法追究原因的痙攣就稱為子癲症,可能發生在產前、產中或產後,但在產後48小時後發生痙攣的機會約有10%。若產後12週後高血壓仍持續,則稱為慢性高血壓。造成子癲前症的危險因子有:孕婦為第一次懷孕、多胞胎懷孕、葡萄胎、原來就有腎臟或心臟疾患、家族遺傳因素等,都屬於子癲前症的好發族群 (表二)。
表一 子癲前症的診斷標準4
表二 子癲前症的危險因子1
貳、致病機轉及臨床表徵5,6
子癲前症是一系列病程的演變,在胚胎著床時就已經開始,造成臨床病程的機轉可能原因如下:一、血管痙攣:血管過度收縮造成血管阻力上升,並且讓血壓上升。二、血管上皮細胞的激化:受損或被激化的上皮細胞可能會使一氧化氮 (nitric oxide) 的分泌減少,或使促進凝血或血管收縮的物質增加,而引發臨床症狀。三、前列腺激素分泌改變:在子癲前症的患者,血管內膜分泌的 prostacyclin (PGI2) 會減少,但血小板分泌的 thromboxane A2 會增加,因此造成對 angiotension II 的敏感度增加,而引發血管收縮。四、一氧化氮活性減少。五、Endothelins 的血中濃度過高。六、Aantiangiogenic factors 表現增加,如:soluble Fms-like tyrosinekinase 1(sFlt-1) 及 soluble endoglin (sEng)。
參、低劑量 aspirin 用於預防的研究7
根據抽血超音波檢查進行判斷,包含血液中胎盤生長因子 (PIGF)、懷孕相關蛋白質A (PAPP-A) 以及超音波測量子宮動脈血流 (Uterine PI)、母親平均血壓 (MAP) 等,篩檢準確度高達八成。子癲前症對孕婦和胎兒潛在危險性極大,故及早診斷、控制與選擇適當時機產出胎兒與胎盤,是非常重要的。透過抽血以及超音波檢查,在懷孕第十二週找出95%罹患子癲前症高危險群之產婦,在醫師指示下及早服用低劑量 aspirin,可降低子癲前症的發生率。低劑量的 aspirin (0.5-2.0 mg/kg) 藉由降低 thromboxane 的合成及維持 prostacyclin 生成,而 prostacyclin 可以讓胎盤的內皮細胞放鬆達到預防子癲前症的效果。2013年針對42篇 RCTs 進行 meta-analysis,總共收錄超過 27,000名具有中至重度子癲前症危險因子的孕婦,研究發現及早 (≤ 16 weeks) 服用低劑量 aspirin 顯著降低子癲前症 (RR 0.47, 95% CI = 0.36-0.62; 7.6 versus 17.9%)、嚴重子癲前症 (RR 0.18, 95% CI = 0.08-0.41; 1.5 versus 12.3%)、胎兒生長遲滯 (RR 0.46, 95% CI = 0.33-0.64; 8.0 versus 17.6%) 及早產 (RR 0.35, 95% CI = 0.22-0.57; 4.8 versus 13.4%) 的發生率。進一步分析更發現,提早在12-16週就使用 aspirin,相較於16週後才使用的組別效果較好 (RR 0.41, 95% CI = 0.19-0.92 versus 0.93, 0.73-1.19)。
肆、治療藥物分類
選擇治療藥物時需考慮母親與胎兒的風險,最重要的考量因子為血壓的變化。許多研究建議嚴重高血壓 (BP ≥ 160 /110 mmHg) 需投與抗高血壓藥物,不僅對母親及胎兒有利且可以降低中風的風險。對於輕度到中度高血壓孕婦並不建議用藥,積極降壓治療 (血壓降低太快),可能造成胎兒窘迫、生長遲滯或使胎兒暴露於藥物潛在風險8。抗高血壓藥物有許多分類,所有藥物皆會通過胎盤,選擇藥物時根據病人血壓的 acuity 及 severity 來決定。以下分別來做介紹:
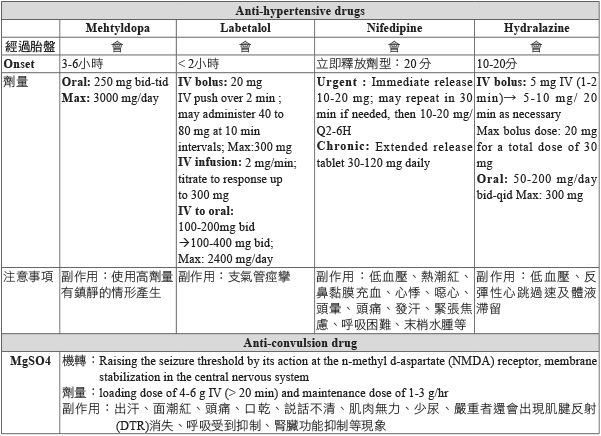
一、抗高血壓藥物 (表三)9
表三 抗高血壓藥物分類
(一)Methyldopa
廣泛用在孕婦上,長期對於嬰兒的安全性數據已建立。但其只具有 mild 的抗血壓能力且起始作用慢 (3-6小時),口服劑量為250 mg, bid-tid,最大劑量為3000 mg/day。
(二)β-blockers
2013年系統性文獻回顧 (收錄13個 population-based case-control 或 cohort studies) 比較在第一孕期服用 β-blockers 與產生先天性畸形 (major congenital malformations) 的風險。研究結果發現並無顯著增加先天性畸形的風險 (OR 0.90, 95% CI = 0.91-1.10)。但在 organ-specific malformations 發現:cardiovascular defects (OR 2.01;95% CI = 1.18-3.42),cleft lip/palate (OR 3.11; 95% CI = 1.79-5.43) 及 neural tube defects (OR 3.56; 95% CI = 1.19-10.67)。因此,這類藥物用於妊娠高血壓需要更進一步的研究。但是,labetalol 具有α及βadrenergic blocking activity,具有保護子宮動脈血流的能力,且作用快 (小於2小時),研究指出用於妊娠高血壓的療效及安全性較佳,臨床上有針劑及口服劑型可以選用。針劑起始劑量20 mg (輸注時間大於2分鐘),維持劑量20-80 mg (at 10 min intervals),總累積劑量300 mg。狀況穩定可改口服,起始劑量100 mg, bid,維持劑量100-400 mg, bid,最大劑量2400 mg/day。
(三)Calcium channel blockers (CCB)
研究指出使用長效型的 nifedipine (sustained release tablet) 並無主要的副作用產生。口服劑量為30-90 mg qd,最大劑量為120 mg/day。立即釋放型通常用於緊急處理,劑量為10-20 mg,若需要可每30分鐘重複給與,不會用於常規控制高血壓。
(四)Hydralazine
靜脈注射 hydralazine 通常用在緊急處理嚴重高血壓的病人。臨床上有靜脈注射及口服兩種劑型可供選擇,但常見的副作用包括低血壓、反彈性心跳過速及體液滯留,因此限制了此藥品在孕婦族群的使用。
(五)Others
像是 thiazide 類的利尿劑或是 clonidine,較少報導用在妊娠高血壓。利尿劑使用會使體液流失導致體內離子失衡,因此除了孕婦有合併肺水腫外,不會常規用於高血壓的治療。Clonidine 的機轉與 methyldopa 相似因此用於治療 mild 的高血壓,但其有反彈性高血壓的副作用,因此除非一般常用的抗高血壓劑不能使用的時候才會考慮使用 clonidine。
二、抗痙攣藥物10
硫酸鎂 (magnesium sulfate) 藉由作用在 n-methyl d-aspartate (NMDA) 受體進而使癲癇發作的閥值提高。另外,也有非專一性的鈣離子阻斷作用及抑制運動神經末梢釋放乙醯膽鹼,因此可以降低血壓,減少子宮收縮的強度和頻率。靜脈注射初始劑量為4-6 g (輸注時間大於20分鐘) 之後維持劑量為1-3 g/hr,治療濃度範圍建議在4.8-8.4 mg/dL (2.0-3.5 mmol/L),濃度太高可能會造成肌腱反射 (deep tendon reflexes, DTR) 消失嚴重甚至會產生呼吸抑制或心跳停止。鎂中毒的解毒劑為靜脈注射1 g calcium gluconate,可能的解毒機轉為體內鎂濃度上升時抑制了 parathyroid hormone (PTH),引起暫時性的血鈣濃度降低,透過鈣離子的補充來競爭細胞上的同一結合部位,拮抗鎂離子作用而解毒。
伍、結論
總結來說,妊娠高血壓如果合併子癲前症或子癲症,對於胎兒或孕婦都是危險的徵兆,要謹慎評估及治療,若出現子癲症、肺水腫、腎功能障礙、胎盤早期剝離、不正常胎兒監測結果、發生 HELLP 症候群及持續惡化的嚴重子癲症患者,應立即治療。為了防止合併症發生,這類患者在診斷早期儘早轉介到有成人及新生兒加護病房的醫院來治療,以避免不必要之風險發生。
Management of Hypertensive Disorders in Pregnancy
Hsiang-Ting Chen1, Chia-Yi Lin2
Department of Pharmacy, Sin-Lau Hospital1,2
Abstract
Hypertensive disorders are the most common medical complication of pregnancies, with an incidence of 5–10%, and a common cause of maternal mortality all over the world. Most cause of death is patients diagnosed with gestational hypertension will subsequently develop into pre-eclampsia, or severe features. In addition, these pregnancies may result in preterm delivery, fetal intrauterine growth restriction, and placental abruption.
Hypertension is defined as a systolic blood pressure (BP) ≥ 140 mmHg or a diastolic BP ≥ 90 mmHg or both. In the absence of strong evidence supporting the use of antihypertensive therapy for mild-to-moderate hypertension during pregnancy, initiation of pharmacological therapy is not recommend unless BP approaches severe hypertention range. The choice of antihypertensive agents include methyldopa、labetalol、nifedipine and hydralazine. Patients should receive an intravenous magnesium sulfate for eclamptic seizures or seizure prophylaxis. Because of the side effects, we recommend to monitor the serum magnesium concentration, DTR, respiration and urine output when using magnesium sulfate.
參考資料:
1.陳鴻昇:妊娠高血壓。高雄醫師會誌2012;20:9-14。
2. Dadelszen P, Magee LA: Fall in mean arterial pressure and fetal growth restriction in pregnancy hypertension: an updated metaregression analysis. J Obstet Gynaecol Can 2002;24:941.
3. Hutcheon JA, Lisonkova S, Joseph KS: Epidemiology of pre-eclampsia and the other hypertensive disorders of pregnancy. Best Pract Res Clin Obstet Gynaecol 2011;25:391.
4. Abalos E, Cuesta C, Grosso AL, et al: Global and regional estimates of preeclampsia and eclampsia: a systematic review. Eur J Obstet Gynecol Reprod Biol 2013;170:1.
5. Thangaratinam S, Koopmans CM, Iyengar S, et al: Accuracy of liver function tests for predicting adverse maternal and fetal outcomes in women with preeclampsia: a systematic review. Acta Obstet Gynecol Scand 2011;90:574-85.
6. Thangaratinam S, Koopmans CM, Iyengar S, et al: How accurate are maternal symptoms in predicting impending complications in women with preeclampsia? A systematic review and meta-analysis. Acta Obstet Gynecol Scand 2011;90:564-73.
7. Villa PM, Kajantie E, Räikkönen K, et al: Aspirin in the prevention of pre-eclampsia in high-risk women: a randomised placebo-controlled PREDO Trial and a meta-analysis of randomised trials. BJOG 2013;120:64-74.
8. Abalos E, Duley L, Steyn DW: Antihypertensive drug therapy for mild to moderate hypertension during pregnancy. Cochrane Database Syst Rev. 2014; 2:CD002252.
9. Moussa HN, Arian SE, Sibai BM: Management of hypertensive disorders in pregnancy. Womens Health (Lond Engl) 2014;10:385-404.
10. Visintin C, Mugglestone MA, Almerie MQ, et al: Management of hypertensive disorders during pregnancy: summary of NICE guidance. BMJ 2010; 341:c2207.

