摘要
目的:本研究探討藥師介入住院之癲癇病人,監測 phenytoin 治療成效。
方法:為回溯式世代研究法,研究時間為2011年1月1日至2012年7月31日,對象為本院使用 phenytoin 之住院病人。實驗組為有藥師主動介入監測 (2012年1月至7月);對照組為沒有藥師介入監測 (2011年1月至12月)。比較兩組間,監測血中濃度時間正確率、以血清白蛋白校正 phenytoin 濃度比率及 phenytoin 於治療濃度範圍內的比率。使用 Chi-square test 及 t-test 作為統計方法,以 P < 0.05視為統計學上有顯著之差異。
結果:共收入321位病人,排除適應症非癲癇的病人39位、使用 phenytoin 小於4天者共170位,剩餘112位病人,分別為實驗組30位,對照組82位。分析監測血中濃度時間正確率,兩組間無顯著差異 (實驗組90%、對照組80.4%,P = 0.393);以血清白蛋白校正 phenytoin 濃度比率,兩組間有顯著差異 (實驗組90%、對照組69.5%,P = 0.028);phenytoin 於治療濃度範圍比率,兩組間沒有顯著差異 (實驗組59.3%、對照組40.7%,P = 0.157)。
結論:藥師介入監測機制,提升了病人使用 phenytoin 時,以血清白蛋白校正濃度的比率,而提高濃度判讀與調整劑量的正確率。
關鍵字:藥師介入、癲癇、監測、phenytoin
壹、前言
Phenytoin 從1930年以來至今,廣泛使用在全身性及局部癲癇發作的藥品1,為治療濃度範圍狹窄的藥物,治療濃度範圍為10-20 mcg/mL2。根據全國藥物不良反應通報中心統計,歷年來 phenytoin 一直是位居第1、2名高通報率的不良反應可疑藥品3。Phenytoin 血中濃度大於25 mcg/mL 時可能會有眼球震顫、運動失調、複視情況發生;血中濃度大於30 mcg/mL 則會有嗜睡、昏睡等不良反應;血中濃度大於50 mcg/mL 則呈現昏迷狀態。如果 phenytoin 血中濃度持續高於治療濃度時,可能會導致譫妄、精神狀態的變化、腦病變或發展成不可逆的小腦功能障礙。
所以藥師在臨床藥事服務中,扮演著協助 phenytoin 監測的重要角色。一般 phenytoin 濃度監測需要有適當的抽血時間點,當達穩定狀態時,最高濃度監測值為靜脈注射給藥後2-4小時;達治療目標時,監測谷底濃度時間為給藥前抽血監測2-3。
Phenytoin 屬高蛋白結合率的藥品 (蛋白結合率約90%),臨床上仰賴具活性作用的游離態分子分佈於各組織間,分佈程度以中樞系統為最高,目前臨床監測仍以 phenytoin 總濃度 (白蛋白結合者與未結合者) 為主,須以白蛋白值校正,10-20 mcg/mL 為治療濃度參考標準2,4,5。其校正的公式一般為 C校正濃度= C監測濃度/(0.2 × 血中白蛋白) + 0.1;當腎清除率小於10 mL/min,其校正公式為C校正濃度= C監測濃度/(0.1 × 血中白蛋白) + 0.12,4- 6。
本研究藉由藥師介入使用 phenytoin 治療癲癇的住院病人,提供醫護人員 phenytoin 藥物濃度監測 (Therapeutic drug monitoring, TDM) 機制,期望達到抽血時間正確、校正濃度確實及血中濃度達有效及安全的治療範圍。
貳、方法
本研究為回溯式世代研究法 (Retrospective cohort study),研究時間為2011年1月1日至2012年7月31日,研究對象為以 phenytoin 治療癲癇的住院病人。對照組為2011年1月至12月,沒有藥師主動介入分析;實驗組為2012年1月至7月,藥師主動介入 phenytoin 監測分析。
病人收案標準:病人診斷為癲癇發作 (seizure),包括:全身性僵直陣攣型發作 (generalized tonic-clonic seizures) 或複雜型部分性發作 (complex partial seizures)。第一次使用 phenytoin 針劑 (Aleviatin Injection 250 mg/5 mL/amp) 的病人。排除條件: 病人診斷非癲癇發作。使用 phenytoin 小於4天,包括:停止使用、病人出院、更換口服劑型或其他抗癲癇藥物。
藥師主動介入標準:一、當醫師開立 phenytoin 針劑時,主動告知醫師監測 phenytoin 血中濃度日期。二、當監測 phenytoin 時,應提醒醫師監測血清白蛋白 (albumin) 以校正 phenytoin 血中濃度。三、當 phenytoin 濃度不在治療濃度範圍內 (10-20 mcg/mL),必須主動建議醫師調整 phenytoin 劑量。Phenytoin 於低血清白蛋白的病人濃度校正公式:(一)一般病人:C校正濃度= C監測濃度/(0.2 × Albumin) + 0.1。(二)洗腎或腎清除率小於10 mL/min 病人:C校正濃度=C監測濃度/(0.1 × Albumin) + 0.1。
本研究分析兩組主要結果:監測血中濃度時間正確率 (使用後4-5天監測,於給藥前30分鐘內抽血,並於達穩定濃度前每4-5天監測一次)。以血清白蛋白校正 phenytoin 濃度比率。 Phenytoin 治療期間時,濃度於10-20 mcg/mL 範圍的比率。次要結果:當 phenytoin 濃度不在治療濃度範圍內,調整 phenytoin 劑量的比率。 發現藥物不良反應的比率。 癲癇控制的成效 (以病例記載及腦波報告為主)。
Phenytoin 輸注給藥方式:稀釋液使用0.9 % normal saline,輸注濃度為 < 6.7 mg/mL,輸注速率為成人 ≦ 50 mg/min、65歲以上老年人及有心血管疾病的病人 ≦ 20 mg/min、12歲以下兒童為1-3 mg/kg/min,輸注管線材質為聚氯乙烯 (polyvinylchloride,PVC)。
統計分析:運用電腦 SPSS 12.0及 Minitab 14程式, 使用 Chi-square test 及 t-test 作為統計方法,並以 P < 0.05視為統計學上有顯著之差異。
參、結果
本研究共收入了321位病人,其中排除適應症非癲癇的病人39位、使用 phenytoin 小於4天 (病危出院、死亡、更換藥物或改為口服劑型) 170位,剩餘112位病人,分別為實驗組30位與對照組82位 (圖一)。
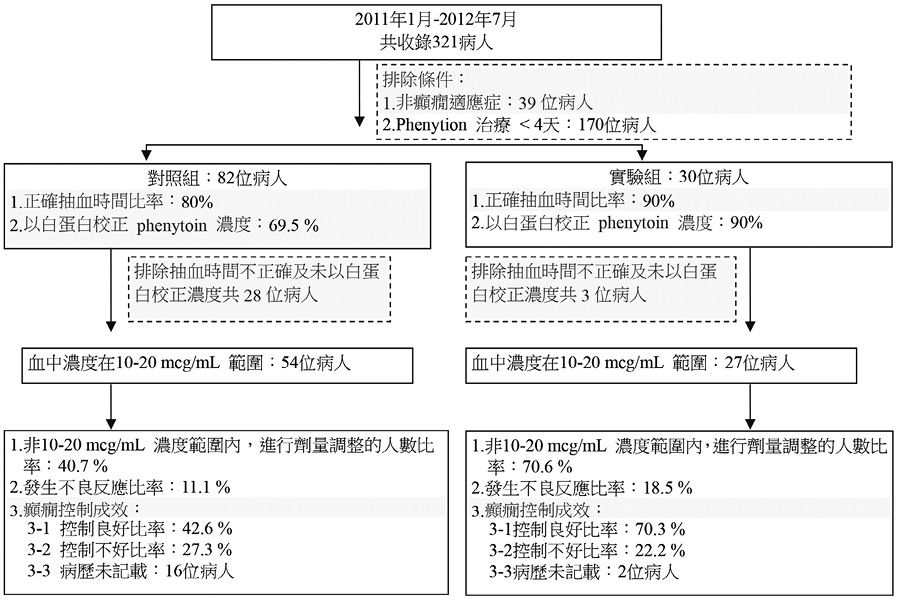
圖一 研究流程圖
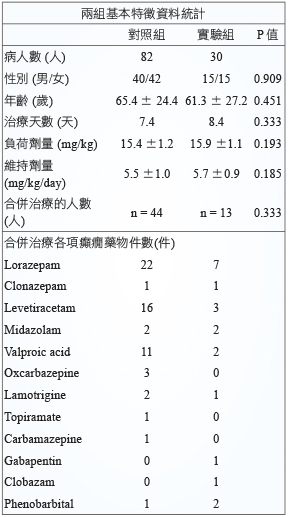
比較兩組之間病人基本特徵,包括:性別、年齡、phenytoin 治療天數、負荷劑量 (loading dose)、維持劑量 (maintenance dose) 及合併其他抗癲癇藥物治療,P值皆大於0.05,表示並無統計學上的差異 (表一)。
表一 實驗組及對照組基本特徵資料統計
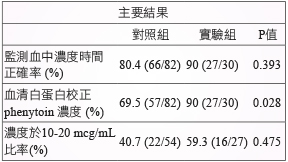
主要結果中發現:監測血中濃度時間正確率,實驗組90% (27/30)、對照組80.4% (66/82),兩組沒有顯著的差異 (P = 0.393)。以血清白蛋白校正 phenytoin 濃度方面,實驗組90% (27/30)、對照組69.5% (57/82), 實驗組有較高的比率,且有顯著的差異 (P = 0.028)。Phenytoin 治療期間時,因監測時間不正確,且沒有以血清白蛋白校正 phenytoin 濃度,故濃度於10-20 mcg/mL 範圍方面的評估,排除實驗組3人及對照組28人,排除後的結果分析為實驗組59.3% (16/27)、對照組40.7% (22/54),實驗組有較高的比率,但是沒有顯著的差異 (P = 0.157,表二)。
表二 實驗組與對照組主要結果比較
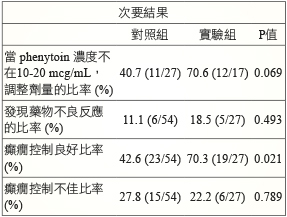
次要結果中發現:監測結果非在治療濃度範圍內 (10-20 mcg/mL),調整 phenytoin 劑量的比率,實驗組70.6%(12/17)、對照組40.7%(11/27),實驗組有較高的比率,但沒有顯著的差異 (P = 0.069)。 發現藥物不良反應的比率,實驗組18.5%(5/27)、對照組11.1%(6/54),兩組沒有顯著的差異 (P = 0.393)。 癲癇控制成效方面,控制良好 (減少發作次數及完全沒有發作) 的部份,實驗組70.3%(19/27) 與對照組42.6%(23/54),實驗組有較高的比率,且有顯著的差異 (P = 0.021);控制不佳的部份,實驗組22.2% (6/27) 與對照組27.8%(15/54),沒有顯著的差異 (P = 0.743,表三)。
表三 實驗組與對照組次要結果比較
肆、討論
近來藥師介入照護的研究資料有增加的趨勢,以 PubMed 關鍵字 “pharmacist intervention” 搜尋近5年共有883篇藥師介入的研究,佔資料庫總收入篇幅將近一半的數量 (1976-2012年,共1848篇)7,顯示藥師於醫療團隊的角色,愈來愈重要。而本篇研究模式參考 Wong 等人,在2011年新加坡 Tan Tock Seng 醫院發表的研究,主要以單一醫學中心的世代研究,比較藥師介入 warfarin 監測前後的成效;發現藥師介入後,凝血的國際標準化比值 (international normalized ratio, INR),均在理想內的時間達成8。由本研究數據得知藥師介入後,phenytoin 監測時間正確率、以白蛋白校正濃度比率、濃度於10-20 mcg/mL 比率、合理劑量調整、發現藥物不良反應的比率及癲癇控制的成效,皆較未有藥師介入之用藥較有成效之差異。
監測 phenytoin 血中濃度時,以公式校正 phenytoin 在身體內的濃度值是非常重要的。根據文獻報告,當人體血清白蛋白過低或腎功能不良時,易造成體內 phenytoin 游離態升高 (游離態治療範圍1-2.5 mcg/mL,一般佔總濃度的5-10%),此時若不校正 phenytoin 濃度,易導致臨床上 phenytoin 濃度誤判,造成藥物中毒9,10。
而在本研究族群中,實驗組血清白蛋白平均值標準差 (mean ± sd) 為2.83 ± 0.82 g/dL (正常值範圍3.5-5.0 g/dL),對照組則有偏低的趨勢 (為2.97 ± 0.79 g/dL);實驗組肌酐酸清除率的平均值標準差為61.8 ± 36.1 mL/min,對照組為54.8 ± 34.7 mL/min。本研究經由藥師介入後,發現實驗組30位病人中有27位監測血清白蛋白及腎功能;有12位病人經校正後濃度超過了20 mcg/mL,經即時調整劑量與持續追蹤,使治療濃度符合於正常治療範圍內。
文獻記載,phenytoin 治療濃度建議控制在10-20 mcg/mL 的範圍,且濃度在 > 15 mcg/mL 時,有86%的病人可以降低癲癇發作次數9。本研究經藥師介入後,濃度在10-20 mcg/mL,且控制良好的比率為75% (12/16人),有25% 的病人癲癇沒有改善。
Phenytoin 與濃度相關的不良反應,根據文獻資料庫記載,血中濃度大於25 mcg/mL 時可能會有眼球震顫、運動失調、複視情況發生;血中濃度大於30 mcg/mL 則會有嗜睡、昏睡等不良反應;血中濃度大於50 mcg/mL 則呈現昏迷狀態,大於100 mcg/mL 則會死亡3,9。本研究中,兩組中共有11位病人發生藥物不良反應,有6位發生皮膚疹,其中實驗組2人,對照組4人,有5位發生肝功能指數 (GOT、GPT) 上升,其中實驗組2人,對照組3人。此11位病人中,7位濃度小於20 mcg/mL (實驗組4人,對照組3人),4位濃度大於20 mcg/mL (實驗組2人,對照組2人),不良反應與濃度沒有直接相關性。
根據2006年 Takuya 等人的研究指出,在日本三重大學醫院,進行世代研究,共70位病人,將 phenytoin 游離態分成三組 (< 5%、5%-10%及 > 10%),研究結果發現游離態 > 10 %的組別中,年齡較大、肌酐酸清除率較低且血清白蛋白較低,有統計學上的差異 (P < 0.05);此研究結果建議,監測 phenytoin 游離態準確度較 phenytoin 總濃度高,而影響 phenytoin 蛋白結合的因子,最主要為年齡、肌酐酸清除率及血清白蛋白11。
故本研究未來方向,也許可以考慮引進 phenytoin 游離態的監測方法,來作為 phenytoin 的療效監測。
伍、檢討
一、本研究中,有幾項觀察的比較結果,兩組沒有統計學上的差異 (P > 0.05),包括:監測血中濃度時間正確率、phenytoin 治療濃度於10-20 mcg/mL 範圍、非治療濃度範圍內有調整劑量的比率。因兩組族群數差異大,也許可以持續增加實驗組的人數來進行分析。
二、在結果分析部份,實驗組有2位,對照組有16位,病例沒有記載後續癲癇相關的治療結果,導致癲癇治療成效的評估,沒有獲得完整的統計結果。
三、在結果分析部份,當 phenytoin 濃度不在治療濃度範圍內,藥師建議調整劑量,有一部份的醫師是選擇停藥或是更換藥品,因此可能會影響實驗組的統計結果。
四、本研究分析是以病例內容記載為主,藥師並未逐床觀察病人的臨床狀況,無法觀察到 phenytoin 與濃度相關的不良反應。
五、目前研究團隊的環境,未具備 phenytoin 游離態濃度的檢測方法,對於濃度在治療範圍內,但無法達到療效的病人,不能確實依游離態濃度,來提升治療效果。
陸、結論
本次研究,因藥師介入監測提升病人使用 phenytoin 時,以白蛋白校正濃度的比率及癲癇控制的成效;不良反應在研究中無法發現是否與濃度過高有相關性。
期待未來研究的方向:一、引進 phenytoin 游離態濃度的檢測方法,可以更進一步提升治療效果。二、改善資訊系統設定,當醫師開立 phenytoin 時,即套餐式帶出監測濃度檢驗的時間及血清白蛋白的檢驗單,以提升 phenytoin 臨床血中濃度監測的準確性及安全性。
Pharmacist Intervene Inpatients Effectiveness Analysis of Monitoring Phenytoin
Yu-Yi Chang, Hao-Hsien Li, Pei-Ling Tsai, Jin-Ru Juang, Ling-Chiau Liau
Department of Pharmacy, National Taiwan University Hospital Yun-Lin Branch
Abstract
Objectives: Pharmacist intervene epileptic inpatients effectiveness analysis of monitoring phenytoin in this study.
Methods: For retrospective cohort study of period is January 1, 2011 to July 31, 2012. Subjects included inpatients using phenytoin. The pharmacist intervention group in monitoring phenytoin during January to July 2012; The control group was no pharmacist intervention monitoring during January to December 2011. Comparison between the two groups, including the correct sampling time, adjusting phenytoin concentration by albumin and therapeutic concentration in 10-20 mcg/mL. Using the Chi-square test and t-test as a statistical method, P < 0.05 is regarded as statistically significant the difference.
Results: A total of 321 patients, excluding non-epilepsy indications of 39 patients and phenytoin using less than 4 days of 170 patients. There were 30 patients in the intervention group while 82 patients in the control group. Correct sampling time was no significant difference between the two groups (intervention group 90%, control group 80.4%, P = 0.393); Adjusting phenytoin concentration by albumin was significant difference between the two groups (intervention group 90%, the control group 69.5%, P = 0.028); Therapeutic concentrations in 10-20 mcg/mL was no significant difference between the two groups (intervention group 59.3%, control group 40.7%, P = 0.157).
Conclusions: The mechanism of pharmacist intervention monitoring enhanced ratios of adjusting phenytoin concentration by albumin when the epileptic inpatients use phenytoin.
參考資料:
1.UpToDate [database on the Internet]. Steven (MD): Pharmacology of antiepileptic drugs. [cited 2012 Oct 13]. Available from: http:// www.uptodate.com/contents/pharmacology.
2. Pharmacy Services University of Kentucky Chandler Hospital: Clinical Pharmacokinetics Service & Anticoagulation Guidelines July 2010. George: University of Kentucky College of Pharmacy 2010: 65-72.
3. 鄧艷屏、盧玲娟、謝右文等:ADR 通報之藥品分析-Phenytoin。 藥物安全簡訊2008 ; 22:19-27。
4. 楊淑珍、陳麗芳、葉聰志:洗腎病患疑似使用phenytoin過量造成癲癇之案例報告。 藥學雜誌電子報2012年10月14日,取自:http//www.taiwan-pharma.org.tw/JTP/101/0 25-029.html.
5. Micromedex 2.0 (Healthcare Series) [database on the Internet]. Greenwood Village (CO): Thomson Reuters (Healthcare). [cited 2012 Oct 14]. Available from:
http // www. thomsonhc.com/micromedex2/ librarian.
6. Larry AB: Applied Clinical Pharmacokinetics. 2nd ed. New York (USA): McGraw-Hill Medical, 2008:490.
7. PubMeD. gov [homepage on the Internet]. US National Library of Medicine National Institutes of Health [cited 2012 Oct 20 ].
Available from: http//www.ncbi.nlm.nih.gov/pubmed?term=pharmacist%20intervention.
8. Wong YM, Quek YN, Tay JC, et al: Efficacy and safety of a pharmacist-managed inpatient anticoagulation service for warfarin initiation and titration. Journal of Clinical Pharmacy and Therapeutics 2011; 36: 585-91.
9. Charles FL, Lora LA, Morton PG, et al: Drug Information Handbook 19th ed. Hudson Ohio (USA). Lexi-Comp, 2010-2011: 1316-9.
10. Sandrina LW, Isabel S, Ludo W: Therapeutic Drug Monitoring of Phenytoin in Critically Ill Patients. Pharmacotherapy 2008; 28: 1392-8.
11. Takuya I, Yoshiyuki K, Yutaka N, et al: Clinical Evaluation of Plasma Free Phenytoin Measurement and Factors Influencing its Protein Binding. Biopharm. Drug Dispos 2006; 27: 77-84.

