摘要
Tacrolimus 是一種巨環 (macrolide lactone) 類的神經鈣磷酸酶抑制劑 (calcineurin inhibitor),目前被廣泛用作心、肝、腎臟移植術後之免疫抑制劑1,2。Metronidazole 為咪唑 (imidazole) 衍生物,被用於具有感受性之厭氧菌感染症1。有多篇文獻指出,tacrolimus 併用 metronidazole 可能導致 tacrolimus 血中濃度升高,增加移植病人處於腎毒性、神經毒性之高風險1,3-5。
本案例報導一位65歲女性為心臟移植術後病人,因病情需要,服用抗排斥藥物 tacrolimus 及 prednisolone 長達5-6個月,復因感染困難梭狀芽孢桿菌 (Clostridium difficile) 發生嚴重腹瀉,故醫師開立 metronidazole 治療;病人腎功能在移植後數月原先都處於正常值,直至併用 metronidazole 開始,意外地,血清肌酸酐竟上升至1.9 mg/dL,且 tacrolimus 血中濃度也明顯上升 (由原來的7.3 ng/mL 增加至14.8 ng/mL),推測可能原因為:tacrolimus 併用 metronidazole 所造成;本文後續將討論此兩者藥物交互作用發生的可能原因及機轉,並進一步提醒臨床醫療人員對併用上開兩種藥物,有發生腎毒性之高風險。
關鍵字:tacrolimus、metronidazole、藥物交互作用
壹、前言
Tacrolimus (FK506) 是屬於巨環 (macrolide lactone) 類的免疫抑制劑,被用來作為心、肝、腎臟移植之第一線用藥或心、肝、腎臟移植 cyclosporin 無效之第二線用藥,在體內及體外研究皆為強效的抗排斥藥物。具有免疫調節的作用能夠阻斷第二介白質 (interleukin-2) 以及其他淋巴激素 (interferon-γ) 的產生。Tacrolimus 會與一種細胞內蛋白 FK-binding protein-12 (FKBP-12) 結合,形成 tacrolimus-FKPB 的複合物,具有抑制 calcineurin phosphatase 的活性,使其無法對活化的T型淋巴細胞核因子 (nuclear factor of activated T lymphocytes) 進行去磷酸化與易位 (translocation) 作用1,2。Tacrolimus 的口服生體可用率具有高度之變異性為4-89%1,2,主要與藥品經由肝、腸道藥物代謝酵素 CYP3A4進行代謝,以及作為腸道運輸蛋白 P-glycoprotein (P-gp) 受質有關,P-gp 在體內主要分布於肝、腎、空腸,負責將代謝物、毒素以及某些藥物排泄進入膽汁、尿液或腸胃道,另外 tacrolimus 的口服生體可用率亦受到其他多種因素之影響,包括食物、藥物交互作用、器官移植部位等1,2,4,6。由於有大於60%的藥物會經由 CYP3A4代謝酵素系統進行生物轉化,因此發生藥物交互作用的機會是相當高的1。有研究指出,在感染性腸炎的患者由於腸道細胞受到破壞以及腸道代謝的改變,導致 tacrolimus 的生體可用率被提高,進一步造成病人 tacrolimus 血中濃度上升,因此往往需要做劑量的調整,預防因濃度上升而造成急性腎毒性6,7。Metronidazole 為咪唑 (imidazole) 衍生物,被用來治療厭氧性細菌感染,也是困難梭狀芽孢桿菌 (Clostridium difficile) 感染的第一線用藥。在接受心臟移植之患者受到困難梭狀芽孢桿菌 (Clostridium difficile) 感染的發生率為8-15%,如果不及時治療則可能導致嚴重脫水、低血容量、低白蛋白血症、全身水腫和電解質失衡1,6,7。在體外研究及案例報告指出,metronidazole 是一種肝臟藥物代謝酵素 CYP3A4抑制劑,它能夠影響 tacrolimus 經由此酵素系統進行生物轉換1,3-5。目前,至少有兩篇以上的案例報告曾提到 tacrolimus 併用 metronidazole 導致 tacrolimus 血中濃度上升之藥物交互作用。因此本文將討論一位心臟移植術後病人,因為感染困難梭狀芽孢桿菌 (Clostridium difficile) 產生嚴重腹瀉,疑似併用 tacrolimus 和 metronidazole 所引起之藥物交互作用之案例。
貳、案例報告
一位65歲女性病人,身高150公分,體重45公斤,有嚴重心衰竭、冠心症等病史,對 Augmentin 有藥物不良反應的記錄。於103/6/25接受心臟移植,術後長期使用抗排斥藥物,目前服用 tacrolimus 1 mg/q12h、prednisolone 5 mg/qd 長達5-6個月,平時 tacrolimus 的血中濃度約維持在4.8-7.3 ng/mL (心臟移植術後 ≧ 4個月之病人,tacrolimus 的目標治療濃度為5-15 ng/mL),血清肌酸酐值約在0.5-0.7 mg/dL。病人從2/25開始出現腹瀉症狀,3/12發高燒38.7℃、抽血檢查顯示白血球20.44 *103/mm、CRP 2.4 mg/dL 皆異常升高,且經由糞便培養發現感染困難梭狀芽孢桿菌 (Clostridium difficile),腹瀉期間 tacrolimus 的血中濃度約維持在5.8-7.3 ng/mL。患者從3/16開始接受 metronidazole 500 mg/q8h IV、vancomycin 500 mg/q6h PO 治療,3/24糞便培養無細菌生長,在3/30停用 vancomycin 且因為腹瀉症狀逐漸獲得改善,於4/11停用 metronidazole,在藥物併用期間 tacrolimus 的血中濃度逐步上升由7.3 ng/mL增加至10.1 ng/mL。
於4/19病人又開始出現腹瀉症狀,4/20發高燒達38.4℃、抽血檢查報告顯示白血球為24.82*103/mm、CRP 2.64 mg/dL,醫師開立 doripenem 500 mg/q8h IVD、metronidazole 500 mg/q8h PO、loperamide 4 mg/ bid PO、acetaminophen 500 mg/stat 治療,經由糞便培養確認再次感染困難梭狀芽孢桿菌 (Clostridium difficile),且經醫師診斷為偽膜性大腸炎 (Pseudomembranous colitis),另外,在尿液培養中也發現感染克雷白氏肺炎桿菌 (Klebsiella pneumonia-ESBL, extend spectrum β-lactamase),5/1醫師改開立 fosfomycin 2000 mg/q8h IVD,4/30-5/5腹瀉次數明顯增加為平均8次/天,5/6醫師更換抗生素為 cefepime 2000 mg/q8h IVD,在藥物併用期間5/7抽測 tacrolimus 的血中濃度發現達到14.8 ng/mL 以及血清肌酸酐值上升至1.9 mg/dL,病人從5/10腹瀉症狀獲得控制,於5/12停用 metronidazole,因為4/26尿液培養無細菌生長,在5/11停用 cefepime,5/18再次抽測 tacrolimus 的血中濃度下降至6.9 ng/mL (圖一),血清肌酸酐值也下降至1 mg/dL。4/20 sputum chlamydia Ag :negative、P. jirovecii (PCR):negative、influenza A/B screen:negative、blood CMV (PCR):negative、mycoplasma P. Ab:negative、EBV -VCA IgM:negative、HSV IgM:negative (表一、表二)。
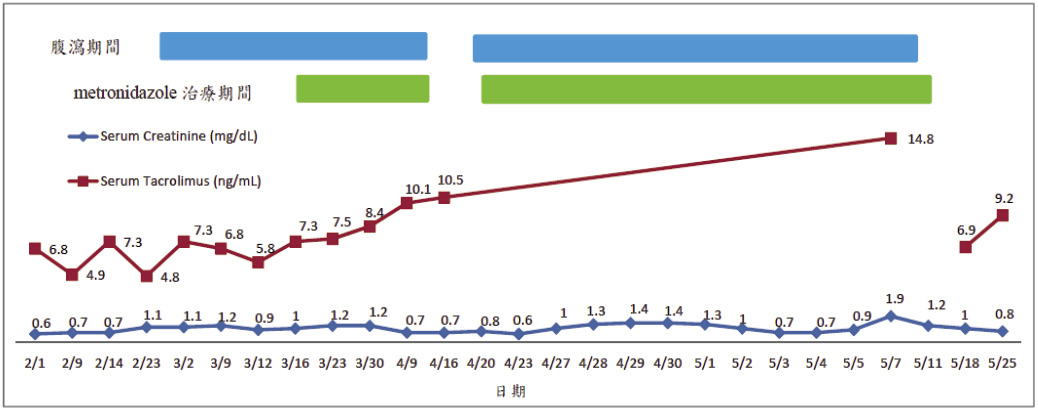
圖一 使用 metronidazole 前後 tacrolimus 血中濃度與血清肌酸酐值變化
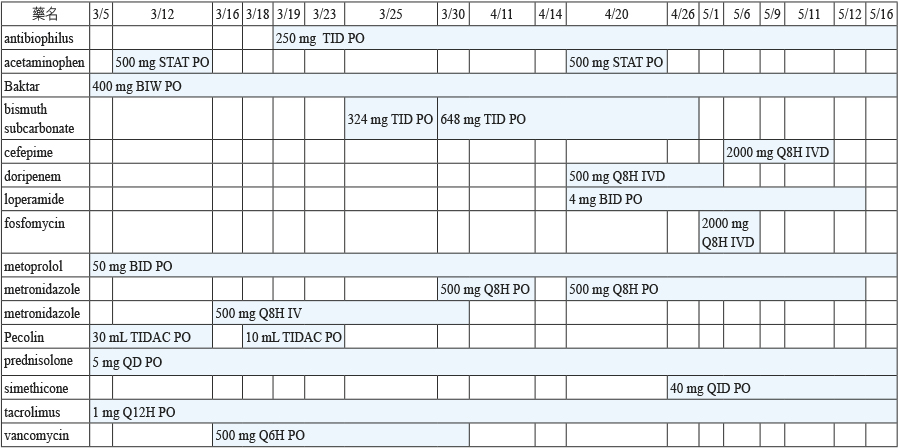
表一 病人用藥史
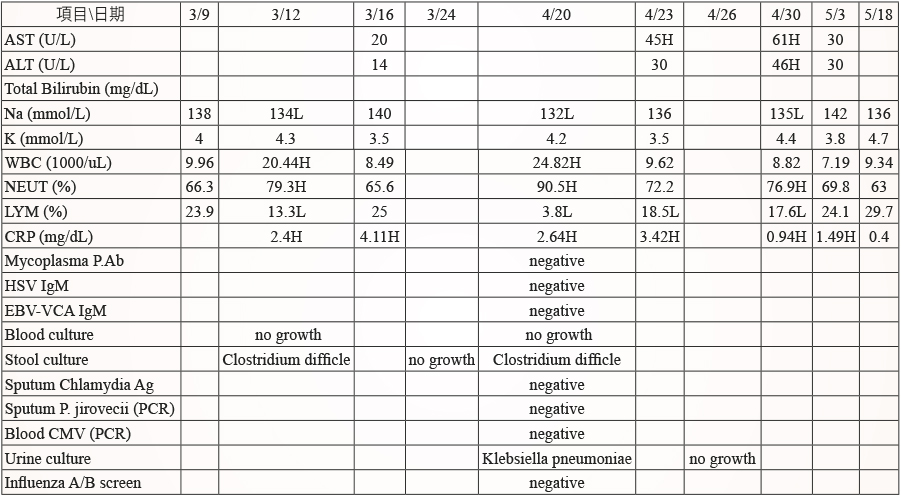
表二 檢驗報告
參、討論
一、 Tacrolimus 與 Metronidazole 交互作用之分析
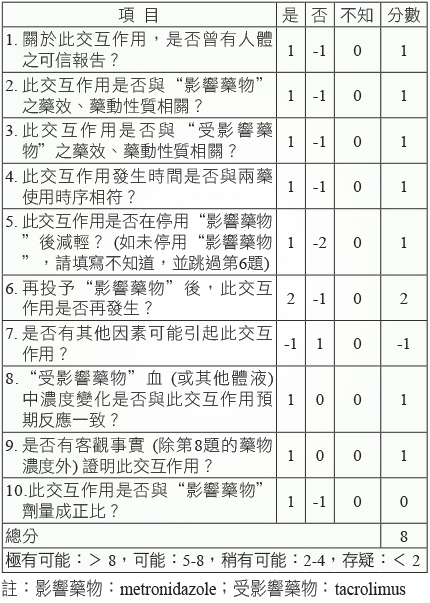
個案在第二次併用 metronidazole 第18天出現 tacrolimus 的血中濃度顯著增加至14.8 ng/mL,已超過原本濃度的2倍以上,而且血清肌酸酐值也上升至1.9 mg/dL。根據 Micromedex 查詢結果 tacrolimus 和 metronidazole 其交互作用嚴重程度為嚴重 (major),起始作用時間為延遲性 (delayed),文獻可信度為良好 (good)。另外,於 Drug Interaction Facts 顯示兩藥交互作用之臨床等級為第4級,嚴重程度為中度 (moderate),起始作用時間為延遲性 (delayed),文獻可信度為具可能性 (possible)5,由此可知併用這兩種藥品的確有可能造成交互作用的發生。過去有關於併用 tacrolimus 和 metronidazole 之案例報告顯示,tacrolimus 的血中濃度大約會在6-14天內增加2-3倍,而且此交互作用與腎毒性之風險具相關性1,3-5,8。通常評估藥物交互作用的可能性,需要考量多種因素,包含:病人本身的疾病因素、藥品動力學、藥效學、食物等。本研究亦使用 DIPS 來評估9,10,併用 tacrolimus 和 metronidazole 之藥物交互作用的潛在可能性,其結果顯示具有可能性 (得分為8分) (表三)。
表三 Drug Interaction Probability Scale of tacrolimus and metronidazole9,10
二、造成交互作用的原因及機轉
此藥品交互作用具有藥物動力學特性,是經由改變 tacrolimus 與 CYP3A4及 P-gp 體循環前代謝 (presystemic metabolism)有關4,6。在體外研究顯示 metronidazole 能夠抑制 CYP3A4和其他混合功能氧化酶 (mixed function oxidases) 的藥物代謝作用4。因為 tacrolimus 是 CYP3A4之受質藥物,所以,metronidazole 經由 CYP3A4抑制 tacrolimus 之代謝是可以被合理解釋的。目前並沒有證據顯示 metronidazole 是 P-gp 抑制劑或受質藥物,但是,根據過去文獻的報導 metronidazole 可能會干擾 tacrolimus 在體內的清除,如果 metronidazole 能夠抑制 P-gp 排出幫浦 (P-gp efflux pump),則可能造成 tacrolimus 的血中濃度增加1,4。有學者指出,感染困難梭狀芽孢桿菌 (Clostridium difficile) 後,因為細菌入侵破壞小腸上皮細胞和改變黏膜的通透性,干擾 P-gp 排出和/或 CYP3A4代謝,以及腹瀉會加快 tacrolimus 通過腸道的時間,而使其主要的吸收部位落在下腸道,而 CYP3A4主要分佈在腸道上半部細胞內,因而減少 tacrolimus 被酵素所代謝,進而造成 tacrolimus 的血中濃度上升,時間從腹瀉開始的1-2星期內都有可能發生1,4,6。雖然本案例因為腸道感染引發腹瀉可能是造成 tacrolimus 血中濃度上升的原因,但是回顧病人在使用 metronidazole 之前發生腹瀉期間 (約19天) tacrolimus 的血中濃度卻並未顯著提高,且經由 DIPS 的評估及文獻的佐證,本研究認為 tacrolimus 和 metronidazole 的交互作用為提高 tacrolimus 的血中濃度是很有可能發生的,另外,在藥物治療期間並未發現其他可疑之交互作用存在。
三、臨床處置
有多篇案例報告指出病人在停用 metronidazole、降低 tacrolimus 的給藥劑量後約2-6天 tacrolimus 的血中濃度、血清肌酸酐值會恢復到接近原來的數值,之後,仍然需要依目標血中濃度調整 tacrolimus 的劑量至適當狀態1,3-5。本案例在使用 metronidazole 期間並未停用或調整 tacrolimus 的劑量,在第二次併用 metronidazole 於第18天出現 tacrolimus 的濃度顯著增加至14.8 ng/mL,以及血清肌酸酐值上升至1.9 mg/dL,當停用 metronidazole 後,第6天 tacrolimus 的濃度恢復到6.9 ng/mL、血清肌酸酐值也下降至1 mg/dL,因此可以合理的懷疑 metronidazole 是造成病人 tacrolimus 的濃度及血清肌酸酐值升高之最主要原因。
肆、結論
因為感染併發症對於接受器官移植的病人是很常見的,所以使用免疫抑制劑處方之病人加入抗感染藥物治療的可能性是相當高。當病人在使用免疫抑制劑治療的期間,必須更仔細的監測每一種藥物之使用對病人的安全性。有多篇文獻指出,神經鈣磷酸酶抑制劑包括:cyclosporin、tacrolimus 等與抗感染藥物有許多交互作用存在。本案例報告指出 tacrolimus 和 metronidazole 併用的結果,將提高病人血中 tacrolimus 的濃度,也可能進一步導致腎毒性的發生。我們提醒臨床醫療人員,對於有在服用 tacrolimus 免疫抑制劑治療的病人,在剛接受或停止 metronidazole 治療時,應該更加密切地監測病人血中 tacrolimus 的濃度,特別是在治療的前2週與停止治療後。
Interaction between Tacrolimus and Metronidazole
Sheng-Ru Lin, Bai-Yin Tsao, Shih-Ning Hsu, Cheng-Chih Hsieh
Department of Pharmacy, Tri-Service General Hospital
Abstract
Tacrolimus is a macrolide calcineurin inhibitor that is frequently used in heart,liver,kidney transplant1,2. Metronidazole is an imidazole derivative used to treat anaerobic infections1.Multiple articles pointed out that coadministration of tacrolimus with metronidazole may result in elevated tacrolimus concentrations, possibly leading to nephrotoxicity, neurotoxicity1,3-5.
We described a 65 year-old woman post heart transplant who had been stabilized on tacrolimus and prednisolone for 5-6 months presented severe diarrhea. Stool cultures were positive for Clostridium difficile, and therapy with metronidazole was initiated. Administration metronidazole therapy, the patient's tacrolimus trough concentration and serum creatinine level increased to 14.8 ng/mL (baseline 7.3ng/mL) and 1.9 mg/dL, respectively. The possible reason may be related to tacrolimus with the addition of metronidazole. We will discuss the drug interactions occur causes and mechanism, and further remind clinical staff, concurrent administration of these two drugs, there is a high risk of occurrence of renal toxicity.
參考資料:
1.Page RL 2nd, Klem PM, Rogers C: Potential elevation of tacrolimus trough concentrations with concomitant metronidazole therapy. Ann Pharmacother 2005; 39: 1109-12.
2. Bauer LA: Applied clinical pharmacokinetics, 3rd ed. New York. McGraw-Hill, 2014: 713-8.
3. Herzig K,Johnson DW: Marked elevation of blood cyclosporine and tacrolimus levels due to concurrent metronidazole therapy(letter). Nephrol Dial Transplant 1999; 14: 521-3.
4. Djordjevic AC, Radovanovic RV, Stefanovic N, et al: Interactions between tacrolimus and metronidazole in a renal transplant patient 2012; 7: 587-590.
5. Tatro DS: Drug interaction facts 2015. Missouri. Wolters Kluwer Health, 2014: 2041.
6. Nakamura A, Amada N, Haga I, et al: Effects of elevated tacrolimus trough levels in association with infectious enteritis on graft function in renal transplant recipients, Transplantation Proceedings 2014; 46: 592-4.
7. Dubberke ER, Burdette SD: Clostridium difficile infections in solid organ transplantation. American Journal of Transplantation 2013; 13: 42-49.
8. Roedler R, Neuhauser MM, Penzak SR: Does metronidazole interact with CYP3A substrates by inhibiting their metabolism through this metabolic pathway? Or should other mechanisms be considered? Ann Pharmacother 2007; 41: 653-7.
9. Horn JR, Hansten PD, Chan LN: Proposal for a new tool to evaluate drug interaction cases. Ann Pharmacother 2007; 41: 674-80.
10. 鄭幸宜、陳宗賢、郭震群等:Valproate與Ertapenem交互作用。藥學雜誌2013; 29: 111-6。

