摘要
藥物引起的化學感受缺失,例如嗅覺缺乏、味覺障礙等,可能影響病人食慾使病人營養攝取不足,進而影響病情的恢復,症狀包括吃東西有金屬味、苦味或沒有味道,機轉涉及鋅的消耗及螯合、改變鈣離子通道活性、黏膜細胞的傷害等,因為化學感受能力的變化不易被察覺也不會造成立即危險,所以常被忽略,早期警告與介入治療,可以提高病人生活品質。
關鍵字:嗅覺缺乏、味覺障礙、口乾症、味覺減退、味覺缺乏、嗅覺遲鈍
壹、 前言
享受美食滿足人類的口腹之欲及避免腐敗食物與環境中的有害物質,味、嗅覺的功能在偵測這些氣味扮演重要的角色,病人發生味、嗅覺異常可能影響食慾造成營養缺乏,進而影響病情,需要釐清病因包括頭部外傷、藥物干擾、感染、環境中化學物質的暴露及可能疾病的影響,相較於其他疾病,此類問題因無立即生命危險,因此較少受到關注。
貳、 嗅覺及味覺病態生理
雖然嗅覺及味覺在功能上類似,但感覺神經輸入傳遞到不相關的皮質區域,嗅覺及味覺是由化學感覺神經 (chemosensory nerves) 所媒介1,而對刺激作用的化學物產生反應,刺激品嚐食物的欲望,是依據這些化學感覺區域的正常功能。
嗅覺依據空氣中的氣味分子傳導,經由通過鼻子及鼻竇到達嗅覺黏膜,嗅覺接受器位於嗅黏膜一平方公分的區域2,3,這些黏膜細胞含有微細絨毛,靠著連續產生黏液當作氣味傳遞媒介,黏液、揮發分子與嗅覺接受器結合,藉由嗅神經的神經路徑接著投射到嗅覺皮質。嗅覺異常可能與空氣污染、外傷、軸突傳遞的干擾、嗅覺接受器的干擾有關,因為嗅覺接受器直接暴露在外部環境,可能受到有害化學物質或感染而受到傷害,造成接受器細胞的凋亡。
人類的基本味覺有酸、甜、苦、鹹及鮮味4,味覺物質經由唾液的分泌及黏液圍繞著味蕾與味覺細胞產生交互作用,味覺物質是以水溶性被攜帶到達接受體,當唾液中的無機物成份改變,味覺會發生變化。研究顯示87%的味蕾功能位於離舌尖2公分之內5,味覺接受器細胞由傳入神經支配,主要由顏面神經、舌咽神經及迷走神經支配,另外三叉神經的分支也支配嘴巴及鼻腔內側,能感受來自辣椒引起辣的燒灼感。對於食物的喜好則結合味、嗅覺與食物溫度、機械感受器感受的口感等綜合因素。
參、 導致味、嗅覺發生異常的原因及異常形態
引起味、嗅覺改變的原因很多,例如疾病、頭部外傷及暴露於有毒物質環境中,在美國每年約有二百七十萬人發生嗅覺傷害,發生率隨著年齡增加而增加,估計每年20萬病人因為味、嗅覺等化學感受能力喪失而就醫3,其中超過22%病人無法歸因於疾病或外傷,而懷疑是藥物引起,藥物引起味,嗅覺疾病的盛行率 > 3%,味、嗅覺異常的形態可分為數種,其中的區別複雜也常造成診斷的錯誤 (表一、表二)3。
表一 疾病與影響味、嗅覺的相關因素
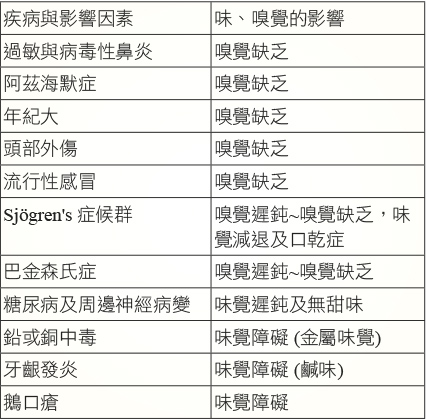
表二 有關味、嗅覺功能異常之描述

一、疾病與年齡的影響
病毒感染或頭部外傷常發生突然的嗅覺喪失,過敏性鼻炎、鼻息肉或癌症則會逐漸發生味覺改變6。嗅覺缺乏也發生在神經退化性疾病,其中90%發生於阿茲海默症、巴金森氏症及亨丁頓舞蹈症患者,常與嗅覺受損有關7。味覺減退及味覺缺乏在老年人是常見的問題,年齡增加會增加味覺的閾值,有研究比較所有種族同年齡的不同性別發生味覺減退的盛行率,發現女性高於男性,且年紀大者高於年輕族群,原因可能是老年女性比男性較常處方長期用藥。
二、環境與化學物質的暴露
抽煙能改變化學感受能力,研究發現抽煙者減少吃東西的愉悅感及脂肪食物的攝取,此可以解釋抽煙者平均體重較輕的原因,許多女性相信抽煙可以減重及壓抑食慾,在完整的戒煙療程之後,病人常經驗到體重突然增加,但抽煙對於味覺的影響仍然有爭議8。
味覺障礙常與化學物質暴露有關,例如水銀、銅、鋅、鉻、鉛等,可能導致味覺改變,例如甜的金屬味與鉛中毒有關,黃銅鑄造廠工人及鋼鐵焊接工人抱怨有金屬味覺,焊接金屬、礦石冶煉及在鹼性電池工廠中的工作者常暴露於鎘 (Cd) 的煙霧中,使嗅覺受到傷害都曾被報告,可能毒性機轉是鋅被鎘置換取代所致。另外殺蟲劑可能經由空氣水及食物,再由上皮吸收而接觸味覺接受器,可能引起神經傳導傷害,影響味覺資訊傳導到達腦部9。
三、 藥物影響味、嗅覺的異常形態與機轉
多種藥物有意義的影響味、嗅覺,這些藥物作用在不同程度及位置,例如周邊接受體、化學感覺神經路徑及腦部,可能的機轉包括藥物在口腔中味道不佳,抗膽鹼藥物及抗憂鬱藥物引起口乾症,產生不適當唾液量攜帶味覺分子而干擾味覺,藥物經由血液影響味覺接受細胞、抑制鈣離子通道的活性、干擾接受器的功能、傷害黏膜細胞影響味覺神經的衝動傳導等 (表三)3。
表三 藥物對味、嗅覺的影響
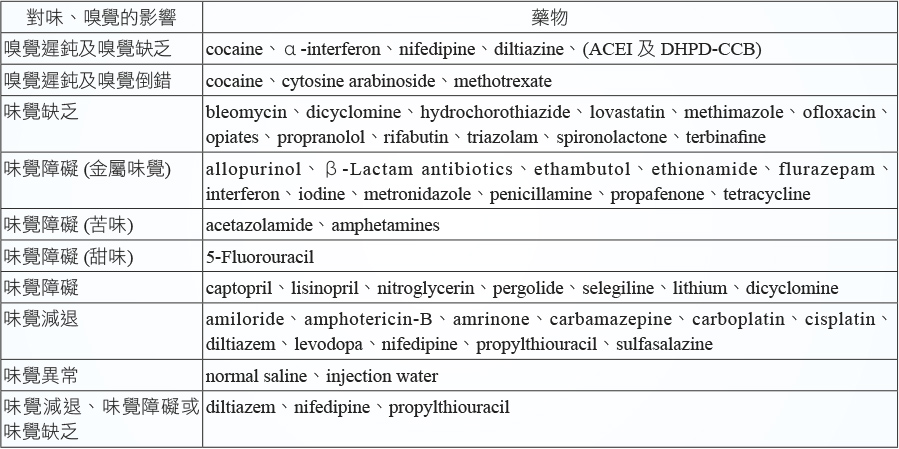
(一)嗅覺缺乏 (anosmia) 及嗅覺遲鈍 (hyposmia)3
毒性機轉可能與傷害嗅覺黏膜的再生、耗損微量元素或神經毒性有關,例如 cocaine、α-interferon、外用硝酸銀藥膏及抗癌藥,也有研究指出在治療劑量下的 nifedipine 及 diltiazem,傷害嗅神經元到嗅球的鈣離子所媒介的神經衝動傳導。
(二)嗅覺遲鈍 (hyposmia) 及嗅覺倒錯 (parosmia)
病人對正常氣味感覺厭惡的味道,機轉可能是因為對黏膜的直接毒性10,例如抗癌藥 cytosine arabinoside、methotrexate 及長期 cocaine 濫用。
(三)味覺障礙 (dysgeusia)
是一種常見但常被忽略的副作用,患者有過度的甜、苦、鹹味或吃東西有金屬味道,常被認為缺少正常味道因此與味覺缺乏混淆。味覺障礙是一種味蕾或神經元異常,涉及離子通道或二級訊息傳遞系統,研究指出常與鋅的缺乏傷害化學感知能力有關,發生機轉可能是鋅螯合增加局部 bradykinin 濃度或尚未確立的機轉,bradykinin 間接增加特定 prostaglandin 合成,最終在細胞內干擾訊息系統。
研究指出含有氫硫基 (sulfhydryl group, -SH) 結構的藥品有發生味覺障礙的疑慮,如 captopril、bisphosphonates、methemazole、etidronate、penicillamine、propylthiouracil11,會增加鋅和銅螯合及代謝作用,也有研究指出8.4%使用 ACEI 病人被報告發生味覺障礙,有些病人因此停藥,其中以 captopril 最常見,使用劑量大於50 mg,症狀包括腐臭味覺、持續鹹味及甜味、持續味覺減退,資料支持降低給藥頻率及使用非 sulfhydryl 結構的 ACEI 可以更快速解除症狀。
(四)口乾症 (Xerostomia)
是抗胆鹼藥物常見的副作用,例如 amitriptyline、brompheniramine 等,經由壓抑唾液的分泌使味覺減少及干擾食物適當的咀嚼,增加食物吞嚥困難及黏膜感染的危險,因此老年人及化學感受能力不足的病人應避免使用抗胆鹼藥物。
(五)味覺減退 (hypogeusia)
常見於重症病人,還有那些從長期疾病中復原的病人,病人一般不會抱怨,通常在討論食物的調味時被發現,例如老年病人常偏愛甜食,機轉可能與藥物增加鋅的清除或全身吸收的減少有關,此外癌症的化學治療增加微量元素損失、傷害黏膜細胞再生及味蕾的破壞而加重腫瘤誘導的味覺改變,引起味覺障礙及厭惡食物的味道也是化療期間營養攝取不良的主要理由,常使用硫酸鋅治療味覺障礙但療效存疑,研究發現鋅的治療對於化學感受能力缺損的好處並未大於安慰劑,僅有真正鋅缺乏病人對鋅治療有反應12,13。
(六)味覺缺乏 (ageusia)
與味覺障礙 (盛行率34%) 相比,味覺缺乏是較少見的 (盛行率 < 3%),病人可能增加食物調味料的用量來獲得某些食物的味覺,但調味料大都含高鹽份,使患有心臟病者可能加重高血壓、心衰竭及心絞痛症狀,可能的致病機轉是 dihydropyridine calcium channel blocker (DHPD-CCB) 鈣離子阻斷劑傷害味蕾神經傳遞物,減少神經元在樹突的反應或進一步傷害神經衝動傳遞到中樞神經,引起味覺缺乏。曾經被報導引起味覺缺乏的藥物包括 ACEI (angioten converting enzyme inhibitors)、diltiazem、nifedipine、nitrates、losartan、長期使用 NTG 貼片、短期使用 terbinafine 及口服抗黴菌藥。
肆、共病的影響
中風病人合併其他疾病可能會傷害化學感受能力,需要更小心監測。糖尿病病人可能有蛋白尿及腎小球病變,可能加重化學感受能力傷害,如果病人同時有抽煙會減少對於正常氣味食物的敏感度,再加上血糖控制不佳、周邊神經病變和腎衰竭,都是造成 ACEI 引起化學感受能力缺失的危險因子,這些病人應該比其他使用 ACEI 病人更嚴密監測。另外,蜘蛛膜下腔出血、中風續發動脈粥狀硬化、高血壓及阿茲海默症,使用 DHPD-CCB 治療可能產生不可逆味覺及嗅覺喪失,ACEI 及 DHPD-CCB 被證明有高盛行率嗅覺遲鈍及味覺減退14,長期使用這些藥物的病人要觀察飲食習慣,還有病人戒煙衛教,減少藥物劑量或使用替代藥物是可以考量的。
伍、味、嗅覺發生異常的治療3,15
研究指出治療的結果可能令人失望,因為即使早期停藥此不良反應有可能延長甚至變成不可逆。許多病例以維他命與微量元素治療無法顯示預期的好處15,應鼓勵病人自我飲食的調整。
治療通常依據病因,例如過敏性鼻炎、鼻竇炎,因為發炎使嗅覺接受器受到傷害,需要解除阻塞及伴隨的感染,給予類固醇 (glucocorticoid) 減少黏膜水腫,最佳使用短期2-3星期治療療程,但停止治療後症狀可能復發,研究支持長期治療使用鼻內類固醇噴劑,如果是細菌性鼻竇炎則選擇適當抗生素。某些過敏性鼻炎可使用抗組織胺,某些病例可能必須減敏,leukotriene 抑制劑可能減少鼻息肉大小,改善某些鼻息肉病人的嗅覺缺乏及嗅覺遲鈍。
使用硫酸鋅治療味覺障礙是普遍的但療效存疑,研究報告顯示有34%化學感受能力障礙的病人使用硫酸鋅治療,發現其中94%的病人對於治療並無好處,僅有真正鋅缺乏病人對鋅治療有反應13,在對照組的研究,鋅的治療對於化學感受能力缺損的好處並未大於安慰劑。
治療持續的味覺障礙 (dysgeusia) 包括遮蔽方法,例如使用吸入、無糖口香糖或口含錠薄荷產品,通常是短期使用,因為病人常會抱怨這些產品會掩蓋他們喜愛的口味,長期使用無法保證症狀解除。人工唾液產品,如含有 pilocarpine 10-15 mg 解決口乾症問題。有研究發現 theophylline (200-800 mg) 能改善受試者50%嗅覺喪失,但還須要進一步對照研究,其他的治療包括補充硒、鎂或氟,有成功治療案例,但療效還須進一步研究。
陸、總結
由於藥物引起的化學感受缺失不常被報告,有些引起味覺障礙藥物的報告沒有被發表,而掩蓋其真正的盛行率,但這些藥物仍然繼續被處方使用,醫療人員及照顧者應該注意觀察病人飲食狀況,藥師可提供相關資料,並且在治療早期給予患者警告,基於病人的反應早期介入,以維護病人生活品質,以預防不可逆的障礙發生。
Disscussion on Drug-Induced Smell and Taste Disturbance Including Its Treatment
Wen-Hwang Chen1, Yin-Yee Chu2, Ya-Lun Lee1, Pei-Liang Chen1
Pharmacy Department of Tungs’ Taichung MetroHarbor Hospital1
Internal Medicine Department of Tungs’ Taichung MetroHarbor Hospital2
Abstract
Drug-induced loss of chemosensation particularly on sense of smell and taste may affect one's appetite and therefore its nutritional intake. It can also affect or slow the recovery of a disease process. Taste disorders symptoms include metallic or bitter taste and some had no gustatory sensation…et al. It can cause alteration in zinc consumption and chelation, changing calcium ion channel activity and injury to mucosal cells...et al. Because loss or injury to chemosensory receptors is very difficult to detect and it does not cause immediate danger thus often ignored. Early warning and interventional therapy can improve the quality of life.
參考資料:
1.Estrem SA, Renner G. Disorders of smell and taste. Otolaryngol Clin North Am 1987;20:133-47.
2. Davidson TM, Murphy C, Jalowayski AA, Smell impairment. Can it be reversed? Postgrad Med 1995;98:107-9.
3. Ackerman BH, Kasberkar N. Disturbances of Traste and Smell Induced by Drugs drugs Pharmacotherapy. Pharmacotherapy. 1997 may-Jun;17(3)
4. Heckmann JG, Heckmann SM, Lang CJ, et al: Neurological aspects of taste disorders. Arch Neurol 2003; 60:667.
5. Moran DT, Rowley JC, Jafek BW, et al: The fine structure of the olfactory mucosa in man. J Neurocytol 1982; 11:721.
6. Apter AJ, Mott AE, Frank ME, et al: Allergic rhinitis and olfactory loss. Ann Allergy Asthma Immunol 1995; 75:311.
7. Hawkes CM. Diagnosis and treatment of Parkinson's disease: anosmia is a common finding. BMJ 1995;310(6977):447-52.
8. Mela DJ. Gustatory function and dietary habits in users and nonusers of smokeless tobacco. Am J Clin Nutr 1989;49:482-9.
9. Henkin RI. Drug-induced taste and smell disorders. Incidence, mechanisms and management related primarily to treatment of sensory receptor dysfunction. Drug Saf 1994; 11:318.
10. Mott AE, Grushka M, Sessle BJ. Diagnosis and management of taste disorders and burning mouth syndrome. Dent Clin North Am 1993;37:33-71.
11. lrvin JD, Viau JM. Safety profiles of the angiotensin converting enzyme inhibitors captopril and enalapril. Am J Med 1986;81(suppl4~):46-50.
12. Henkin RI, Scheichter BJ, Freidwald WT, et al. A doubleblind study of the effects of zinc sulfate on taste and smell function. Am J Med Sci 1976;272:285-99.
13. Alpers DH. Zinc and deficiencies of taste and smell JAMA 1994;272:1233-4
14. JM, Lambert AE. Long-term reduction of microalbuminuria after 3 years of angiotensin converting enzyme inhibition by peridopril in hypertensive insulin-treated diabetic patients. Am J Med 1992;92(4B):102%7
15. Zazgornik J, Kaiser W, Biesenbach G. Captopril-induced dysgeusia. Lancet 1993;341(8859):1542.

