摘要
糖尿病是引起慢性腎臟疾病的危險因子之一,約有20-30%的糖尿病人會進展為糖尿病腎臟病變。根據流行病學的統計資料,在台灣糖尿病、慢性腎病的盛行率逐年上升。且糖尿病合併慢性腎臟疾病的病人會增加心血管疾病的風險。糖尿病的血糖控制方法包括生活型態的改善、飲食控制、規律運動、口服藥物以及胰島素。然而糖尿病藥物治療時會因腎功能不良而增加低血糖的風險,須作藥物使用劑量的調整。
Metformin 是全球公認治療糖尿病的首選藥物,優點是少有低血糖的風險、體重不會增加。2015年4月衛生福利部公告修訂 metformin 在禁忌症的使用規範為:腎絲球體過濾率 (eGFR) 介於30-45 mL/min/1.73 m2應減量使用;腎絲球體過濾率 (eGFR) 小於30 mL/min/1.73 m2禁用。Pioglitazone 可用於慢性腎臟疾病,但對於併有心臟衰竭的病人須謹慎使用。而 sulfonylureas、glinides 及 insulin 類藥物會有低血糖的風險,從低劑量、緩慢增加劑量使用是重要的,並注意藥物的活性代謝產物會延長低血糖的時間。DPP-4 inhibitors 不會引起低血糖,多數藥物 (除 linagliptin) 調整劑量後可適用於慢性腎臟病人。適當的選擇降血糖藥物的合併適當的劑量調整對增進糖尿病合併慢性腎臟病人的用藥安全而言是重要的。
關鍵字:糖尿病、慢性腎臟疾病、低血糖、biguanide、sulfonylureas、DPP-4 inhibitors
壹、前言
根據流行病學的統計資料,在台灣糖尿病的盛行率逐年上升。從2000年到2008年糖尿病人口數增加了70 % (70.7萬人增加到120.5萬人),盛行率增加了48% (4.31%上升到6.38%)1。糖尿病是引起慢性腎臟疾病的危險因子之一。在全世界末期腎病的人口以7%年成長率增加,在2011年人口數達200萬人,慢性腎臟疾病的盛行率約在10-14%,是全球健康的重要課題。在台灣,末期腎病與透析病人逐年增加,慢性腎臟病的盛行率約為9.8%-11.9%,其中糖尿病人為主要族群之一2。
糖尿病未積極控制會增加大血管 (腦血管、心血管)、小血管 (視網膜、腎臟血管) 的病變。而有糖尿病合併慢性腎臟疾病的病人會增加心血管疾病的風險。過去研究指出,多數糖尿病合併有第三期以上腎病變者會引起嚴重的心血管事件,增加死亡率3。
藥物代謝的主要途徑包括肝臟及腎臟,糖尿病的用藥若經腎臟代謝,對於慢性腎臟疾病者可能延長代謝時間,增加低血糖發生的風險。對於合併有糖尿病、慢性腎臟疾病的病人如何選擇降血糖藥物,以穩定控制血糖、降低心血管疾病發生率、預防低血糖的發生,增加藥物治療的有效性及安全性是重要的課題。
貳、糖尿病治療目標
根據美國糖尿病學會 (American Diabetes Association;ADA) 公佈的治療指引,對於非妊娠的成年人的血糖控制建議糖化血色素 (Glycated hemoglobin;HbA1C) 控制在7%以下有助於降低小血管的併發症。然而有嚴重併發症的病人可接受控制 HbA1C 在7-8%之間,合併有慢性腎臟疾病者屬於這個部分3。
HbA1C 是廣泛用於評估長期糖尿病控制的方式。然而檢驗數值可能會受慢性腎臟疾病引起的併發症 (包括溶血、缺鐵性貧血) 所影響,再作校正評估。
根據台灣流行病學的研究顯示,糖尿病病人老化及共病症的比率逐年升高1。且糖尿病合併有慢性腎臟疾病者多為老年人,可能有其他併發症須要多種藥物治療,須考慮多種藥物併用引起的交互作用3。
參、 糖尿病合併慢性腎病之降血糖藥物治療個論
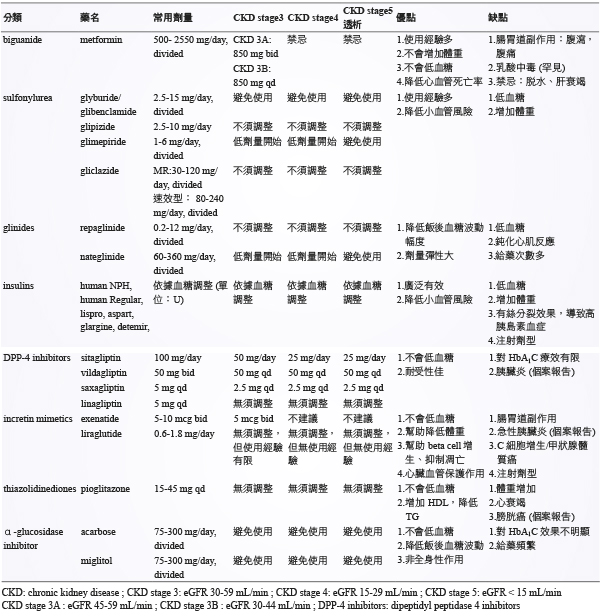
對於糖尿病合併慢性腎臟疾病者降血糖藥物的選擇、劑量的調整是重要課題,以下介紹降血糖各大類藥物的特性與對於糖尿病併發症的影響,藥物劑量調整與優缺點詳列於表一中。
表一 糖尿病併有慢性腎臟疾病的降血糖藥物治療4
一、Biguanide 類
臨床降血糖使用上第一線用藥,主要作用為減少肝臟糖質新生,增加組織對胰島素敏感性。口服身體可用率約50-60%,不與血液中蛋白質結合,經12-24小時由腎臟以原型排出,因此當腎絲球濾過率 (Glomerular filtration rate,簡稱 GFR) 下降時,metformin 會蓄積,可能導致乳酸中毒的危險 (非常罕見,每1000個人年約有0.03個案,但死亡率卻極高,約30-50%)5,因此腎臟功能不良者建議調整劑量4。2015年4月國內衛生福利部公告 metformin 在 eGFR 介於30-45 mL/min/1.73 m2應減量使用;eGFR 小於30 mL/min/1.73 m2禁用6。英國 UKPDS 的研究顯示,過胖的第二型糖尿病人,長期使用 biguanide 類藥物相較於飲食控制有助於降低血管疾病的發生率、總死亡率7。
二、Sulfonylureas 類
主要作用為刺激胰臟分泌胰島素,其第一代藥物 (包含 chlorpropamide、acetohexamide、tolbutamide、tolazamide) 大多由腎臟進行排除,因此在嚴重腎功能不良病人為使用禁忌,目前大多使用第二代藥物4。英國 UKPDS 的研究結果,使用 sulfonylureas 的藥物相較於飲食控制可有效降低小血管疾病的發生率,但對大血管病變沒有達到顯著差異7。
Glyburide,100%經由肝臟代謝4,雖然它的清除率與腎臟無關,但代謝產物具降血糖活性,增加低血糖的風險甚至會持續超過24小時3。根據 Simpson 等人的回溯性研究顯示,使用較高劑量的 glyburide 會增加死亡的風險 (hazard ratio:1.3,95% CI:1.2-1.4)7。Gliclazide,大部分經由肝臟代謝,代謝產物不具降血糖活性;且蛋白結合率高4,因此腎臟功能不良者不需調整劑量。然而中華民國糖尿病衛教學會的會訊中提到對於嚴重腎功能不良者,因為藥物動力學與藥效會受其影響,導致低血糖發生時間延長,建議避免使用5。
三、Nonsulfonylurea insulin secretagogues 類 (glinides)
包含 repaglinide 和 nateglinide,主要作用是藉關閉胰臟 beta-細胞膜上的 KATP 孔道,造成胰島素的釋放。作用時間短,低血糖風險比 sulfonylurea 類低4。目前沒有長期的臨床研究證實 glinides 類藥物是否會影響心血管事件的發生7。
四、Insulins
胰島素在腎小球過濾,近曲小管吸收,當腎功能惡化時,腎小管胰島素的再回收會增加以補償胰島素過濾的減少,目前並沒有根據 GFR 做出適合胰島素藥物調整的相關指引,因此需密集監測病人的血糖以適度調整胰島素劑量4。根據 Reilly 等人的研究結果,當 GFR 下降至10-50 mL/min 時,胰島素的劑量應該要減少25%,GFR 下降至10 mL/min 時,胰島素劑量應該減少50%3。英國 UKPDS 的研究結果顯示,長期使用 insulins 類藥物相較於飲食控制有助於降低心血管疾病的發生率,但也顯著增加低血糖的風險 (p < 0.0001)、增加體重 (p < 0.001)7。
五、 Dipeptidyl peptidase 4 (DPP-4) inhibitors 類
藉抑制 DPP-4活性來增加飯後腸泌素 (incretin) 濃度、胰島素分泌和減少昇糖素 (glucagon) 分泌,此類藥物多數可使用在腎功能異常病人身上,只是需要調整劑量。目前多個 DPP-4 inhibitors 長期使用對於糖尿病併發症影響的研究仍在進行中,包括 TECOS (Trial Evaluating Cardiovascular Outcomes with Sitagliptin) 研究、SAVOR-TIMI (Saxagliptin Assessment of Vascular Outcomes Recorded in Patients with Diabetes Mellitus–Thrombolysis in Myocardial Infarction) 研究等,仍須更多研究結果證實其效益7。
Sitagliptin,第一個口服 DPP-4 inhibitor,大部分在腎臟經由主動分泌及腎小球過濾以原型由尿液排泄。在有腎功能疾患的病人身上,可發現藥物排出減少,代謝半衰期延長,因此建議依據腎功能調整藥物劑量4。Vildagliptin 主要經由羧化 (carboxylation) 反應代謝,產生活性代謝產物3。藥物85%由尿液,15%由糞便排泄。在 CKD (chronic kidney disease) stage 3以上,因本身及活性代謝產物經腎臟排出減少,所以須調整劑量4。Saxagliptin,主要經肝臟的 CYP3A4/5代謝成活性代謝產物 (5-hydroxysaxagliptin)3,其具有藥物50%降血糖的功能。部分比例原型藥物及活性代謝產物經由腎臟排除 (佔75%),因此建議 CKD stage 3以上病人減少劑量使用4。Linagliptin,主要經由肝臟代謝成非活性產物,其中超過85%由膽汁排出,另5%由尿液排出,不須依腎功能調整劑量4。
六、Incretin mimetics 類
藉由結合胰臟 beta 細胞上的 GLP-1接受器來促進胰島素釋放,並減少昇糖素分泌及胃排空4。目前與 exenatide 相關的 EXSCEL 安全性研究仍在進行中,須待研究證實5。
Exenatide,經由腎臟進行蛋白質降解,尿液排除,在 CKD stage 4以上不建議使用。Liraglutide,完全經由體內內生性酵素-DPP4,及 NEP (neutral endopeptidase) 代謝,因此不需要依腎功能調整劑量3。然而缺乏 GFR < 60 mL/min 的臨床試驗支持,僅藥物動力學、藥效研究顯示 GFR 降低時 (GFR > 15 mL/min),並不影響藥物代謝或排泄。所以臨床使用時仍須注意相關不良反應4。
七、Thiazolidinediones 類
此類藥品活化轉錄因子 PPAR-γ,改善胰島素敏感性4。Pioglitazone,主要經由肝臟代謝成6種代謝產物,其中3種有活性,在腎功能不良時代謝產物不會蓄積,因此 GFR 下降時不需要調整劑量。然而須注意的是副作用:造成體液蓄積,特別是 CKD 的病人體液蓄積會造成病人水腫,增加慢性心臟衰竭的風險4。2007年 PROACTIVE 的研究結果,pioglitazone 用於心肌梗塞病史的病人,可以顯著降低28%心肌梗塞 (p = 0.045)、37%急性冠心症 (p = 0.035)、19%相關大血管併發症 (p = 0.033);但也顯著增加心衰竭的發生 (p = 0.003) 及因心衰竭住院的比例 (p = 0.022)7。臨床用藥選擇上須多方面評估選擇7。
八、α-glucosidase inhibitor 類
抑制小腸α-glucosidase 以延遲碳水化合物吸收,可降低飯後高血糖,單獨使用不會引起低血糖。Acarbose,幾乎全由腸胃道代謝,在腎功能不良的病人,血中藥物濃度可能增加數倍,因此不建議使用。其較大的副作用為肝指數上升、黃疸以及腸胃道症狀5。根據 UKPDS 對於 acarbose 的前瞻性研究顯示,對於罹病率與致死率無影響。然而2003年 STOP-NIDDM 的研究顯示使用 acarbose 相較於安慰劑可顯著降低49%的心血管風險 (p = 0.003)、其中主要降低心肌梗塞 (p = 0.03)7。
肆、結論
綜述以上藥物個論,依據腎功能分級,降血糖藥物的選擇列於圖一中3。臨床上藥物的選擇依腎絲球過濾率為依據,對於病情急遽變化的住院病人,仍以胰島素的治療為首選,同時須密切監測血糖變化。合併糖尿病與慢性腎臟疾病的病人的藥物選擇以藥物動力學不受腎功能影響的藥物為優先5,並注意藥物劑量的調整,因為腎功能降低影響藥物的代謝,增加藥物的累積,可能延長藥物的藥效,導致低血糖的風險。GFR < 30 mL/min 的病人建議轉診到腎臟專科醫師,以改善照護品質、降低醫療成本、提升病人用藥安全5。
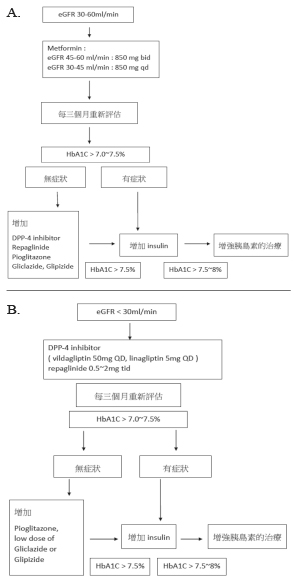
圖一 依據腎功能分級,降血糖藥物的選擇3
Drug Therapy in Diabetes Mellitus with Chronic Kidney Disease
Ai-Yu Yang1, Jheng-Jhong Cai2
Department of Pharmacy, Kaohsiung Medical University Chung-Ho Memorial Hospital1
Taipei Oxygen& Gases Co., Ltd.2
Abstract
Diabetes is one of the risk factors for chronic kidney disease (CKD). Approximately 20-30% of people with diabetes will progress to diabetic kidney disease. According to epidemiological statistics, the prevalence of diabetes and chronic kidney disease has been increasing year by year. Patients with diabetes mellitus and chronic kidney disease are in higher risk of cardiovascular disease. Glycemic control in diabetes patients includes improved lifestyle, diet control, regular exercise, oral medications and insulin injections. It will, however, require dosage adjustment regarding the increasing risk of hypoglycemia due to renal insufficiency.
Metformin is globally accepted as the first choice for diabetic subjects. In April 2015, the Ministry of Health and Welfare made an announcement that metformin dosage should be reduced once the estimated glomerular filtration rate (eGFR) falls between 30 to 45 mL/min per 1.73m2 and should stop use when it drops below 30 mL/min per 1.73 m2. Pioglitazone can be used in chronic kidney disease, however patients with heart failure should be cautious. The use of sulfonylureas, glinides and insulin can put these patients in danger of hypoglycemia, for this reason, lower doses and slow titration are important. DPP-4 inhibitors do not cause hypoglycemia and most of them (exclusive of linagliptin) require reduction in various stages of renal disease.It is important that appropriate select and dosage adjustment on hypoglycemic agents to improve drug safety in patients with diabetes mellitus and chronic kidney disease.
參考資料:
1.Jiang YD, Chang CH, Tai TY, et al: Incidence and prevalence rates of diabetes mellitus in Taiwan: analysis of the 2000-2009 Nationwide Health Insurance database. J Formosan Med Assoc 2012;111(11):599-604.
2. 衛生福利部國民健康署:慢性腎臟病防治手冊。台北:國民健康署,2000。
3. Ioannidis I: Diabetes treatment in patients with renal disease: Is the landscape clear enough? World journal of diabetes 2014;5(5):651-658.
4. Lalau JD, Arnouts P, Sharif A, et al: Metformin and other antidiabetic agents in renal failure patients. Kidney Int 2015; 87(2): 308-322.
5. 王舒儀:糖尿病腎臟病變降血糖藥物的使用原則。中華民國糖尿病衛教學會會訊2010;9。
6. 財團法人藥害救濟基金會,藥物安全訊息. http://www.tdrf.org.tw/ch/03_message/mes_02_main.asp?bull_id=5734.
7. 朱俊源、李文賢、許柏超等:以心臟科醫師的角度來看糖尿病藥物的使用。內科學誌2013; 24(1): 12-18。

