摘要
痛風與慢性腎疾病的盛行率皆逐年增加。痛風是世界上最常見的關節炎。國際準則明確規定治療目標為:保持病人無發作及保持低的血清尿酸值。治療包括了急性發作、降尿酸和預防發作。代謝徵候群、心血管疾病和腎臟疾病常是痛風之共病症。本文提供慢性腎病人痛風臨床處置。
關鍵字: 痛風、高尿酸血症、慢性腎疾病、HLA-B*5801、Gout、Hyperuricemia
壹、前言
痛風是一種極度疼痛的關節炎,門診或是住院病人皆常見之,為尿酸排泄減少或尿酸產生增加所造成的疾病。臨床表現上,痛風是血中尿酸濃度過高,引起尿酸鈉鹽結晶沉積於關節、軟骨、滑囊液、肌腱或軟組織中導致關節炎、軟組織沉積、腎結石以及尿酸鹽腎病之發炎性疾病。急性痛風突然發作時可見關節處紅、腫、熱、痛等現象,好發處為下肢的關節1-4。
慢性腎疾病 (chronic kidney disease, CKD) 的盛行率逐年增加,在美國約佔14%的人口,在全世界而言,約佔了16%。除了考量合併有痛風與慢性腎病人之外,慢性腎病是繼肥胖與高血壓,第三個痛風之獨立危險因子。此外,研究顯示,痛風和高尿酸血症可損害腎臟功能5。
本文章討論急、慢性痛風之臨床處理之外,也評估慢性腎病人之急、慢性痛風之處置。
貳、高尿酸血症的定義
依生理化學上的定義,血中每100 毫升血液中的尿酸濃度大於6.8-7.0 mg/dL 以上為高尿酸血症。人體內的血中尿酸濃度會受種族、遺傳基因、性別、年齡的影響4,6。
尿酸是嘌呤在人體代謝的最終產物,體內普林在肝臟代謝形成尿酸,最後由腎臟將尿酸隨尿液排出體外,如果體內產生過多或腎臟排泄尿酸不良,就會形成尿酸過高。在大部份的哺乳類動物有 urate oxidase (uricase) enzyme 可以把 uric acid 轉變成 allantoin,而降低血中 uric acid 的濃度;但人類此 uricase 已無功能,因此人類體內的尿酸約三分之二由腎臟經尿液排出,約三分之一由腸內細菌分解代謝隨大腸糞便排出,另有極少量由汗腺排泄。痛風的產生是經由改變 purine 的代謝所導致的高尿酸血症 (hyperuricemia) 所產生 (圖一)1,7。
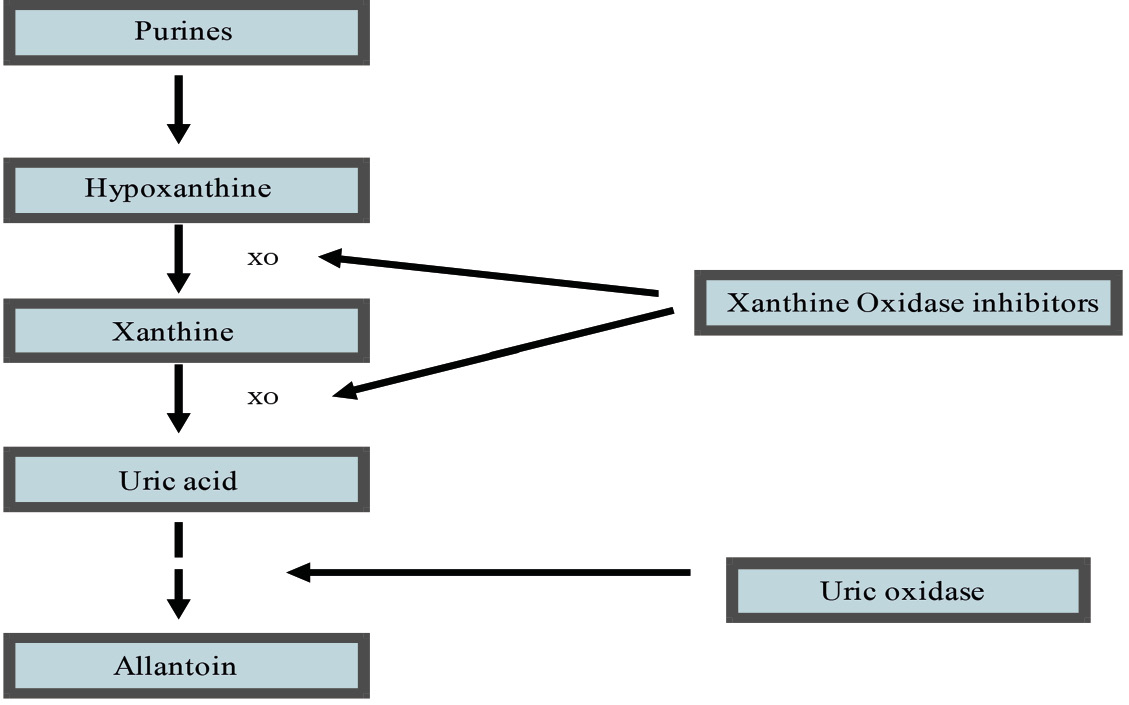
圖一 Purine 的代謝以及藥物作用之位置7
一般血中尿酸的飽合溶解度為6.8 mg/dL,當超過這個飽合點,尿酸結晶便會析出沉澱於軟組織,造成白血球浸潤及釋出細胞介質導致急性發炎反應5,7。
目前診斷痛風大多採用1977年美國風濕病學會 (American college of Rheumatology;ACR) 制訂的急性痛風診斷分類標準1,該標準以關節液和痛風石結節中找到尿酸鈉鹽結晶,作為確定的痛風診斷。但當抽取關節液困難或不便時,根據12 項臨床特徵中具備6項或6項以上,並排除其它疾病後,也能優先考慮痛風的診斷。這12項臨床特徵包含︰1.超過一次以上急性關節炎發作的病史;2.發炎徵狀在一天內達到高峰;3.急性單側關節炎發作;4.患部關節皮膚呈暗紅或紅色;5.第一腳趾關節疼痛或腫脹;6.單側第一腳趾關節炎發作;7.單側腳踝關節炎發作;8.有可疑的痛風石結節;9.高尿酸血症;10. x光片顯示不對稱關節腫脹;11. x光片檢查顯示不合併侵蝕的骨皮質下囊腫;12. 關節炎發作時抽取之關節液微生物培養呈無菌 (表一)1。
表一 American College of Rheumatology Prelimininary Criteria for Gout1

痛風的臨床表現分為四個階段:無症狀高尿酸血症 (asymptomatic hyperuricaemia);急性痛風性關節炎 (acute gouty arthritis);間歇期 (intercritical or interval gout);慢性痛風石關節炎 (chronic tophaceousgout)。
參、治療
一、無症狀高尿酸血症的治療
對於未曾有過關節發炎症狀的高尿酸血症,基本是採取較保守的態度,通常不會先以藥物降低血中尿酸。建議先找出及排除會造成高尿酸血症的疾病、藥物、肥胖、飲食習慣等,並加以調整及修正生活型態4,8。國家腎病學會整理出會增加血中尿酸值的藥物,可適時據以調整 (表二)5。
表二 會提升血中尿酸值之藥物10
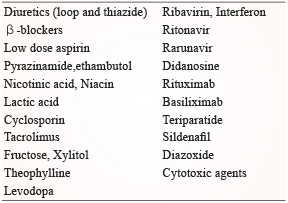
非藥物治療核心原則為:減肥,以達到健康的身體質量指數、均衡飲食、鍛煉強身健體、戒菸、保持適當之飲水5。
二、Acute gout 之處置
急性痛風發作時非常疼痛,但通常在一至兩週會自行緩解;再次復發的急性痛風通常發作期會延長,且需要治療才能緩解,提早使用消炎止痛藥物治療可以迅速緩解疼痛。
目前的2012美國風濕病學會治療指引建議急性痛風性關節炎的病人盡快在發作24小時內開始給與藥物緩解疼痛與發炎之情形。已經在使用降尿酸藥物的患者在急性痛風發作期間應該繼續療程不用中斷。而2016年歐洲抗風濕病聯盟 (EULAR) 則建議在痛風發作時盡快使用第一線的急性發作藥物如 coichicine (痛風發作12小時內)、非類固醇消炎止痛藥、類固醇11。
ACR 與 EULAR 並未建議那一個為首選,而是建議依照病人個別之共病症而選擇。而在嚴重或難治型發作則可以使用合併治療。
治療流程則依發作疼痛的嚴重度與受侵犯關節的數量與大小位置來決定 (圖二)6,9。
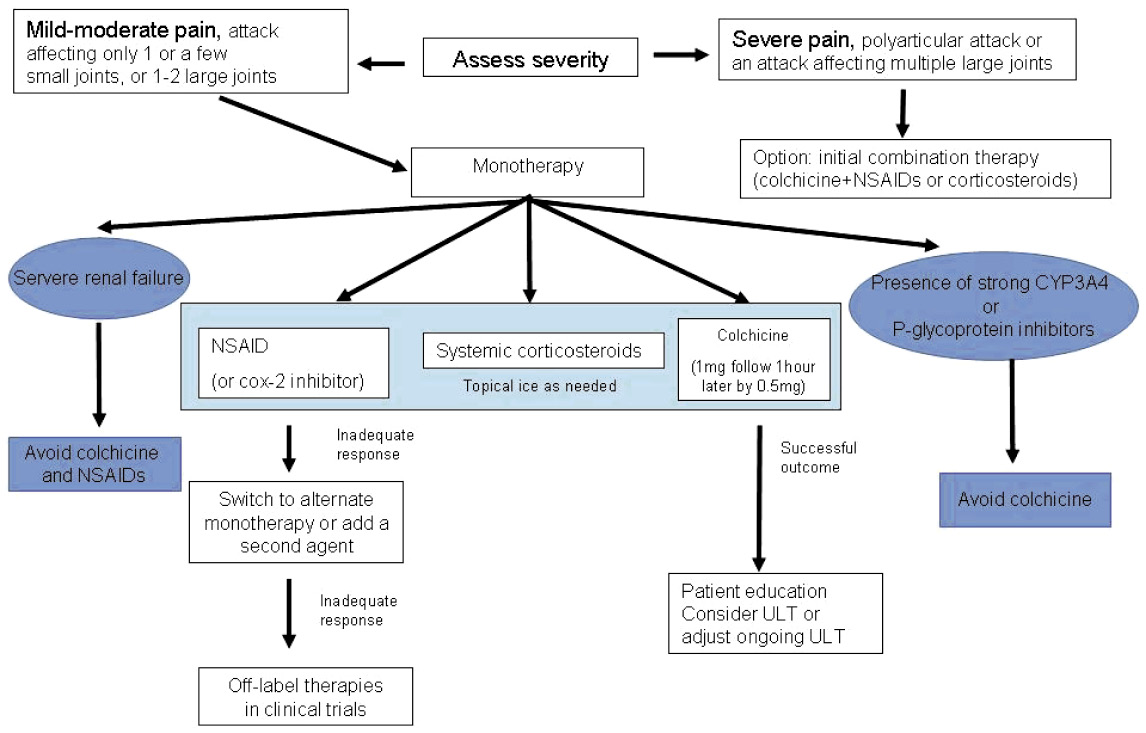
圖二 急性痛風的處置流程9,11
非類固醇消炎止痛藥方面,建議可使用至 Food and Drug Administration (FDA) 核准之抗發炎與止痛之全劑量。FDA 許可naproxen、indomethacin 與 sulindac 可用於急性痛風,目前在肌肉注射 ketorolac 與局部外用 NSAIDs 用來治療急性痛風是仍沒共識的9。此外目前美國腎臟基金會建議慢性腎病人避免使用 NSAIDs5,10。EULAR 亦建議嚴重腎損傷患者避免使用 NSAIDs11。
Colchicine 使用方面,以往治療模式為先給與1 mg 的 colchicine,之後每2-3小時給與0.5 mg,直至疼痛緩解或有噁心嘔吐或下痢之情形始停止使用;目前建議可先使用 colchicine loading dose 1 mg,接著在一小時後給與0.5 mg,然後可開始給與維持劑量0.5 mg,一天一次至一天三次直至痛風緩解,如此可以有效的緩解痛風又可以降低副作用的產生3,6,8,9。而慢性腎病人之 colchicine 清除率是大幅降低的,因此在嚴重慢性腎病 (CrCl < 30 mL/min),建議可依照急性治療之劑量,但兩週內不可超過2次療程;而在血液透析患者方面,建議給與單一劑量0.6 mg (0.5 mg),兩週最多給與2次5。EULAR 則建議使用強 P-glycoprotein 及/或 CYP3A4抑制劑者以及嚴重腎損傷患者避免使用 colchicine11。
類固醇方面,建議依發作關節的數量來選擇,如果是一至兩個小關節,建議使用口服之類固醇,若是一至兩個大關節發作,則建議關節內注射類固醇,且依照關節大小來決定劑量以及是否需要合併使用口服之非類固醇消炎止痛藥、類固醇或 colchicine6,9。
當關節內注射無法可用,如多關節侵犯,病人個人意願不高或患處施打受限,建議口服類固醇 prednisolone 從0.5 mg/kg/day 開始給與5至10天,然後停用。替代的藥物為肌肉注射單一劑量的 triamcinolone acetonide,然後接著口服 prednisolone9。
無法經口進食的住院病人,建議可以依受侵犯的部位與數量於關節內注射適當劑量之類固醇或者靜脈注射或肌肉注射 methylprednisolone9。
慢性腎病人方面,類固醇相對於 NSAIDs 及 colchicine,是比較有效且安全的藥物5。在合併藥物治療急性痛風方面,建議可以關節內注射類固醇合併 colchicine 與 NSAIDs,與口服類固醇。考量可能之胃腸道之毒性,目前並未討論到 NSAIDs 與全身性類固醇之合併使用9。
三、 不發作間歇期及慢性痛風石關節炎的治療
不發作間歇期是指兩次急性痛風關節炎中間的無症狀不痛期間。當長期沒有治療時,痛風病人的皮下及關節產生痛風石結節,有些會導致關節變形,嚴重時關節喪失活動能力。當病人經臨床檢查或影像學顯示有痛風石,或急性痛風性關節炎發作頻率一年大於或等於2次,或是 CKD Stage 2或更差的患者,或有尿路結石病史的患者,建議可開始給與藥物治療9。
降尿酸藥物 (urate-lowering therapy; ULT) 藥物有兩大類:抑制尿酸鹽產生 (uricostatic agents) 之 xanthine oxidase inhibitor (XOI) 類以及促進尿酸鹽排除 (uricosuric agents) 類。
首選第一線降尿酸治療藥物為 xanthine oxidase inhibitor (XOI)︰allopurinol 或febuxostat3,4。
一般 allopurinol 起始劑量建議不要超過100 mg/day。慢性腎疾病人 (CKD Stage 4或更差的患者) 建議可從50 mg/day 開始。一般認為如此可降低在開始使用降尿酸藥物導致之急性痛風發作之發生率,且可適時的處理可能發生的 allopurinol 嚴重過敏反應之情形。在降尿酸值的效果不佳時,建議縱使為腎損傷的病人,可在適當的衛教或常規監測可能的過敏反應或副作用 (騷癢、皮疹、肝功能異常) 之下,維持劑量可以大於300 mg/day 或更高2,5。
HLA-B*5801基因與 allopurinol 之高度過敏反應有高度之相關性,在 stage 3或更差之韓國血統慢性腎病,以及中國與泰國人身上,有高機率 HLA-B*5801基因存在,建議這些族群在開始使用 allopurinol 之前考慮監測有否 HLA-B*5801基因2,12。
Febuxostat 在輕至中度之慢性腎病人不需要調整劑量。一般建議起始劑量為40 mg/day,每日最大劑量為80 mg/day。當病人使用 allopurinol 無法達到理想目標或對 allopurinol 無法耐受則建議更改為 febuxostat11。在慢性腎病第四期或更差 (eGFR < 15 mL/min/1.73 m2) 缺乏足夠的安全性研究,不建議使用在此族群5。
而當病人非尿酸過度生產之情形,且對 allopurinol 產生抗藥性或耐受性,建議使用促進尿酸鹽排除類當慢性痛風治療之第二線藥物2。
一般促進尿酸鹽排除可選擇的藥物為 suphinpyrazone、benzbromarone 與 probenecid。但當 CCR < 50 mL/min 時,則不建議使用 probenecid。因此輕到中度腎功能不全的患者 (CCR 介於30-60 mL/min),建議使用 benzbromarone 每天50-200 mg。此外 fenofibrate 與 losartan 是目前尚未核准之 uricosuric agents2。
一般慢性痛風之處理流程為先單一使用 XOI (或者 uricosuric agents) 且至最大劑量,如未能達到治療目標則加入第二個藥物 uricosuric agents 合併使用至最大劑量。但是 CCR < 30 mL/min 時,EULAR 則不建議更改為 febuxostat 或加入 benzbromarone11。合併治療失敗之難處理痛風則給予注射之 pegylated uricase, pegloticase,目前在慢性腎病人因無足夠的研究,故不建議使用 (圖三)2,5,10。
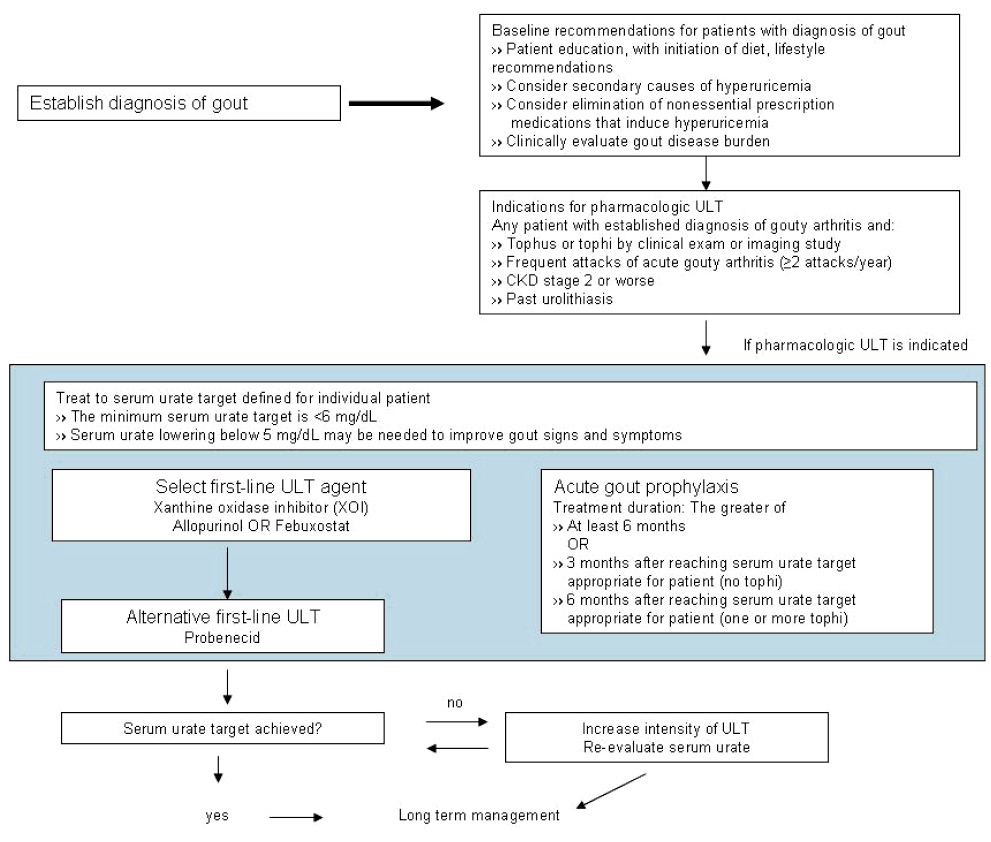
圖三 慢性痛風的處理流程10
四、 慢性痛風藥物治療時之抗發炎藥物選擇
初使用降尿酸藥物治療時,建議開始使用 colchicine 0.5 mg,一天兩次,最少六個月來預防急性發作產生11。慢性腎病者則應降低劑量,嚴重慢性腎病 (CCR < 3 0 mL/min) 者建議起始劑量為0.3 mg/day。血液透析患者起始劑量0.3 mg 一週兩次。美國腎臟基金會則建議慢性腎病人避免使用 NSAIDs。(GFR < 30 mL/min 者避免使用;GFR < 60 mL/min 者不建議常期使用)。低劑量之 prednisolone (< = 10 mg/day) 可作為二線考量2,5,6,11。
肆、痛風合併症的治療
當病人痛風發作在病人使用 loop 或 thiazide 利尿劑,建議替換之;如果降血壓則考量使用 losartan 或 calcium channel blockers;如果為高血脂則考量使用 statin 或 fenofibrate11。
在特別族群的考量上,藥物的選用還需考慮到可能發生的不良反應,例如潛在的中度和重度慢性腎病 (NSAIDs,COX-2抑製劑,colchicine),充血性心臟衰竭 (NSAIDs,COX-2抑製劑),消化性潰瘍病 (NSAIDs,COX-2抑製劑,皮質類固醇),抗凝或抗血小板聚集治療 (NSAIDS),糖尿病 (類固醇),持續感染或高風險感染 (類固醇),和肝臟疾病 (NSAIDs,COX-2抑製劑,秋水仙素)9。
伍、結論
高尿酸血症並不一定會發生痛風,對於無痛風發作的高尿酸血症通常不需要藥物治療;生活型態的調整與飲食控制是治療高尿酸的首要方式;避免食用大量的高普林類的食物以減低尿酸的生成,以及減少喝酒以避免影響了尿酸的排泄,且多喝水亦可避免泌尿道結石的情形;此外,經醫師仔細評估可能引起尿酸偏高的因素,而因素移除或控制後,通常尿酸值可能會回復到正常。急性痛風發作期越早給予藥物治療以緩解疼痛與發炎的情形可越快達到控制的效果;而慢性痛風只要經正確的處理與藥物劑量適度的調整加上耐心,通常都可以得到良好的控制。
Treatment of Gout for Patients with Chronic Kidney Disease
Chien-Tzu Liu, Yi-Ping Hsiang
Department of Pharmacy, E-DA Hospital
Abstract
Gout is the most frequent arthritis worldwide. International guidelines clearly specify treatment targets: keep the patient flare-free and maintain a low urate serum level. The treatment to target strategy includes therapy of flares, urate lowering treatment (ULT) and prophylaxis of flares. Comorbidities such as metabolic syndrome, cardiovascular and chronic kidney disease (CKD) are often found in gout patients. The objective of this article is to provide an update information on the management of acute and chronic gout in CKD.
參考資料:
1.Eggebeen, AT. Gout: an update. American Family Physician 2007; 76(6): 801-8.
2. Khanna D et al: 2012 American College of Rheumatology guidelines for management of gout. Part 1: systematic nonpharmacologic and pharmacologic therapeutic approaches to hyperuricemia. Arthritis Care Res (Hoboken) 2012 Oct; 64(10): 1431-46.
3. Zhang W. Doherty M. Pascual E, et al: EULAR evidence based recommendations for gout. Part I: Diagnosis. Report of a task force of the Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT). Annals of the Rheumatic Diseases 2006; 65(10): 1301-11.
4. 社團法人中華民國風濕病醫學會:台灣痛風與高尿酸血症診療指引。風濕病醫學會,2016。
5. National kidney Foundation.: A clinical update on gout: Optimizing care for patients with chronic kidney disease. National kidney Foundation 2014.
6. Jordan KM, Cameron JS, Snaith M, et al: British Society for Rheumatology and British Health Professionals in Rheumatology Guideline for the Management of Gout. Rheumatology 2007; 46(8): 1372-4.
7. Teng GG, Nair R, Saag KG. Pathophysiology, Clinical Presentation and Treatment of Gout. Drug 2006; 66 (12): 1547-1563.
8. Zhang W. Doherty M. Bardin T,et al: EULAR evidence based recommendations for gout. Part II: Management. Report of a task force of the EULAR Standing Committee for International Clinical Studies Including Therapeutics (ESCISIT). Annals of the Rheumatic Diseases 2006; 65(10): 1312-24.
9. Khanna D et al: 2012 American College of Rheumatology guidelines for management of gout. Part 2: therapy and antiinflammatory prophylaxis of acute gouty arthritis. Arthritis Care Res (Hoboken) 2012; 64(10): 1447-61.
10. Inker LA, Astor BC, Fox CH, et al: KDOQI US commentary on the 2012 KDIGO clinical practice guideline for the evaluation and management of CKD. Am J Kidney Dis 2014 May; 63(5): 713-35.
11. Richette P, Doherty M, Pascual E, et al: 2016 updated EULAR evidence-based recommendations for the management of gout. Ann Rheum Dis. 2016; 0:1-14.
12. Robinson PC, Stamp LK. Stamp LK.The management of gout: Much has changed. Aust Fam Physician 2016 May; 45(5): 299-302.

