摘要
許多研究發現,慢性骨髓性白血病及胃腸道基質瘤病人服用固定劑量的 imatinib 於穩定期波谷血中濃度的變異性很大。此外,陸續有研究發現慢性骨髓性白血病及進階型胃腸道基質瘤的病人,若 imatinib 波谷血中濃度較高,則病人有較佳的療效反應。由於 imatinib 除病人間的藥物動力學變異大,且其療程所費不貲,又考量到病人的服藥配合度可能不如預期且需長時間服用,是否能藉由血中濃度監測使病人達最佳治療成效,值得探討。
關鍵字: Imatinib、Glivec、therapeutic drug monitoring、chronic myeloid leukemia、gastrointestinal stromal tumor、tyrosine kinase inhibitors
壹、酪氨酸激酶抑制劑於病人的個體差異
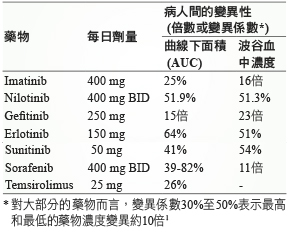
2012年 Gao 等人於《臨床腫瘤學雜誌》,發表了癌症標靶治療藥物血中濃度監測 (therapeutic drug monitoring,TDM) 的綜論,實際上不論給藥策略為何,標靶藥物有明顯而大幅的藥動學變異性。酪氨酸激酶抑制劑 (tyrosine kinase inhibitors,TKI) 的病人個體差異亦是如此 (表一),投予 imatinib 400 mg (每日標準劑量) 的波谷血中濃度,不同病人間的差異高達16倍1。2014年 Widmer 等人於《歐洲癌症雜誌》發表的綜論提到,imatinib 的藥物動力學曲線下面積變異係數為19%至83%。在藥效學方面已發現血液學反應、細胞基因體學反應、分子生物學反應和無惡化存活期等療效觀察點和波谷血中濃度有關。以目前為止的文獻資料看來,僅有 imatinib 的濃度閥值已有較完整的資料,被專家認為 imatinib TDM 是可做為臨床治療的指引2。歐洲腫瘤醫學會認為監測 imatinib 血中濃度對於所有的病人可能是重要的,且建議療效不彰、治療失敗、出現劑量限制毒性反應或不良反應的病人進行 imatinib TDM2。
表一 酪氨酸激酶抑制劑在不同病人間的藥物動力學變異性1
Imatinib 的口服身體可用率高達98%,且排除半衰期約18小時,因此非常適合以每日口服的方式給予3,而目前尚未發現食物會對 imatinib 的吸收造成影響2。儘管 imatinib 的治療效果佳、口服吸收好、排除半衰期長,具有很多優勢,但仍然會有效果不彰的情況,影響效果可能的因素包含:生理上的因素 (例如:基因型)、臨床上的特徵 (例如:疾病階段) 以及藥物的暴露量 (與藥物動力學有關)4。若患有胃腸道基質瘤 (GIST) 的病人曾進行重大的胃切除手術,其波谷血中濃度會較低5。此外,許多研究發現 imatinib 不論是用於慢性骨髓性白血病 (CML) 或 GIST,病人的服藥配合度都意外的低2,6(目前已有提到此趨勢的評估方法包含計算剩藥量、病人自評、醫師評估、家人敘述、藥局領藥紀錄等,配合度的標準則因研究而異)。而服藥配合度低已被證實為 imatinib 達不到療效的主要因素6。Imatinib 主要是透過 CYP3A4和 CYP3A5代謝,潛在藥物間的交互作用多,可能也是造成個體差異大的原因之一2。
貳、Imatinib 血中濃度與臨床意義
一、 慢性骨髓性白血病 (chronic myeloid leukemia,CML)
(一) 波谷血中濃度 (trough) 與療效關係的研究
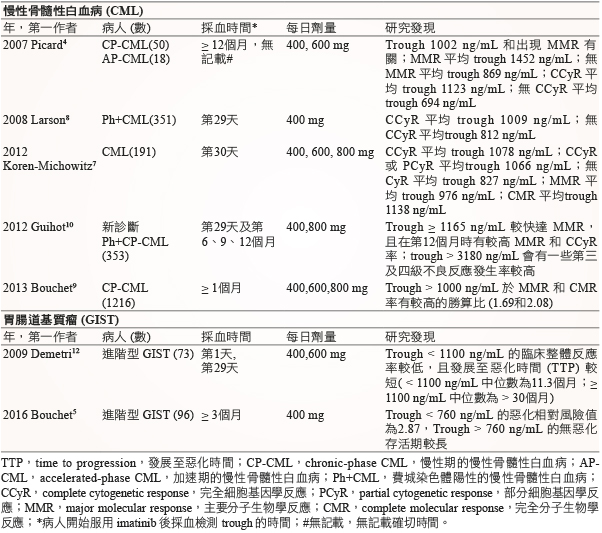
目前已有多篇研究發現 imatinib 的波谷血中濃度和治療 CML 的療效有關4,7-10。2007年 Picard 等人發現,有達到主要分子生物學反應 (major molecular response,MMR) 的病人,其平均波谷血中濃度較高,沒達到反應的病人則較低 (分別為1452 ng/mL 和869 ng/mL,p < 0.001)4。2008年 Larson 等人的研究顯示,有達到完全細胞基因學反應 (complete cytogenetic response,CCyR),其平均波谷血中濃度為1009 ng/mL,較沒達到反應的病人812 ng/mL 高,並發現達藥物穩定狀態的血中濃度 (Css) 和 MMR、長期的 CCyR 及無事件存活期 (event-free survival,EFS) 有關8。2012年 Koren-Michowitz 等人的研究結果也與前人相符,波谷血中濃度較高的病人 (平均1078 ng/mL) 有較佳的 CCyR。此外 Koren-Michowitz 等人研究顯示,肝、腎功能不全病人的平均波谷血中濃度和功能正常的人相似7。
(二) 參考 TDM 調整 imatinib 劑量的研究11
2015年 Rousselot 等人在《血液》發表 OPTIM-imatinib 試驗研究結果,評估3個月內新診斷的慢性期 CML 人,運用 TDM 來調整 imatinib 的劑量 (圖一)11。於收案後15天抽血,根據病人 imatinib 波谷血中濃度 (trough),分為1000 ng/mL 以上 (A3組) 和未達1000 ng/mL,並將未達1000 ng/mL 的病人隨機分配為參考 trough 增加劑量以達到1000 ng/mL 的組別 (A1組) 和維持傳統標準劑量的組別 (A2組)。A1及 A2組病人每個月會監測一次 imatinib trough,A3組則是3個月監測一次。發現僅35%的病人在一開始使用標準劑量即達1000 ng/mL,這一類的病人可能不需要更高劑量的 imatinib,另外65%的病人則未達1000 ng/mL。在試驗的第12個月時,A1組77%病人調高劑量,23%病人維持或降低劑量。在安全性上追蹤病人情況 (追蹤中位數31個月) 發現:A1和 A2組的不良反應率接近 (各別為58%和51%)、三組嚴重不良反應比例及停止治療比例類似。並提到 A1和 A2組停止治療原因不盡相同,A2組有較高比率病人因治療失敗停止 (A2組停藥病人中60%為治療失敗;A1組停藥病人中18%為治療失敗,P = 0.08),但未詳述這些病人停止治療和治療失敗的原因。在效果上,第12個月時評估 MMR 反應率,A1和 A3沒有統計學差異,但 A1的 MMR 比率明顯較 A2組高 (A1組63%;A2組37%,P = 0.031),相當於1.7倍的反應率11。
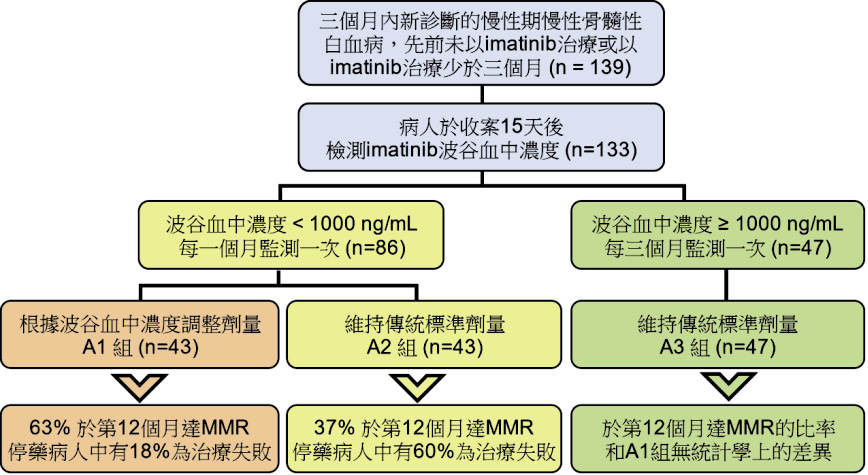
圖一 OPTIM-imatinib 試驗,2015年 Rousselot 等人發表11
二、 胃腸道基質瘤 (gastrointestinal stromal tumor,GIST)
2009年 Demetri 等人發現 (抽血時間為第1天和第29天),治療進階型胃腸道基質瘤 (Advanced GIST) 時,imatinib trough < 1100 ng/mL 的病人臨床整體反應率較低,且發展至惡化時間 (time to progression,TTP) 較短:< 1100 ng/mL 者的 TTP 中位數為11.3個月;≥ 1100 ng/mL 中位數為超過 30個月 (P = 0.0029)12。Echoute 等人以50名 GIST 病人 (34%局部進階型、62%轉移型) 行前瞻性研究,從病人服用 imatinib 起,長時間且有固定時間觀察抽血數值,演算出 GIST 病人服用 imatinib 的藥物動力學公式,推論 GIST 病人於服藥90天後,imatinib 的相對生物利用度降低29.3% (目前 CML 無類似研究結果)13。2016年 Bouchet 等人參考前述 Echoute 研究結果,對進階型 GIST 的病人服用400 mg imatinib 進行世代研究,定於服藥3個月後且為第一次惡化前至少採一次 trough (未統一採血時間),發現 trough < 760 ng/mL 的惡化相對風險值為2.87,trough > 760 ng/mL 的病人無惡化存活期較長5。因 Bouchet 採血點在服藥超過3個月後至惡化前,Demetri 在第29天,若依 Echoute 的藥動學研究來看,可能可解釋為何 Bouchet 研究的 trough 較 Demetri 的低。試驗設計上 Demetri 為理想狀態,Bouchet 較貼近現實,兩研究的病人皆為不能切除或轉移型 GIST,是否有其他變因使結果不同仍有待進一步研究釐清。
目前 imatinib 暴露量 (穩定期的 trough) 在 CML 和 GIST 的臨床反應之部分研究整理 (表二)。
表二 Imatinib 暴露量與臨床反應的關係
參、 監測 Imatinib 血中濃度於臨床的可行性
一、檢測方式
常見於文獻中的檢測方式為液相層析串聯式質譜儀 (liquid chromatography tandem mass spectrometry,LC-MS/MS) 和高效液相層析儀 (high performance liquid chromatography,HPLC)。此二種檢測設備費用高,且有技術性難度、分離與檢測耗時等因素,可能因此較不能被醫院普遍使用。2015年 Beumer 等人用同質奈米粒子免疫法,以分析儀檢測 imatinib 的濃度 (第一個用於檢測 imatinib 的自動化免疫法),並以 LC-MS/MS 檢測為比較測試,結果顯示不論在精準度、線性、曲線穩定性而言,同質奈米粒子免疫法為可信賴的分析方式14。
二、抽血時間
由於 imatinib TDM 預期是觀察藥物達到血中穩定狀態 (steady state) 的 trough,多數文獻以第29天至1個月以上為抽血的時間 (表二)4,5,7-10,12。Imatinib 排除半衰期約18小時,推估會在第6至7天達穩定狀態,若要提早觀察則是至少連續服用7天後檢測較為適當。但於 GIST 的病人,2012年 Eechoute 等人認為先前其他研究閥值1100 ng/mL 應為合適,但若僅監測第29天,之後病人實際的藥物暴露量可能會不足 (以 Eechoute 的藥動學公式推算,第29天時相對生物利用度會降低17%,90天後降低29.3%,達另一穩定狀態),因此 Echoute 認為 imatinib TDM 用於 GIST 病人,必須是在特定時間點進行,且在第一年的第三個月過後還要再次監測13。2012年 Jadson 於《臨床癌症研究》發表對 Echoute 研究的評論,認為 GIST 要等 imatinib 的清除率提高的時間過後再做 TDM (第3個月或是3個月後)3。
綜合目前的文獻看來,imatinib TDM 已具有一定程度的研究提供參考時間及數值,在檢測技術的普及上亦是可行的。
肆、討論與結論
Imatinib 效果良好,為目前用來治療 CML 和 GIST 的標準用藥,然而病人的 trough 變異相當大又和療效有關。造成 imatinib trough 較低可能因素:服藥配合度低、個體差異、交互作用、曾行重大胃切除手術等。有許多研究顯示病人服用 imatinib 配合度低的比例相當高,為無法達療效的主因,甚至可能增加除 imatinib 藥價外283%醫療花費6。因服藥配合度低可能會影響 trough,故若有 trough 低且治療狀況不佳的情況,亦應探討是否有服藥配合度的問題再決定調整劑量或換藥。就目前對 imatinib TDM 的相關研究,發現治療反應較佳的病人其 imatinib 的波谷血中濃度有較高的趨勢4,5,7-10,12,但大於3180 ng/mL 的第三及第四級不良反應發生率較高10。2015年 Rousselot 等人則運用 TDM 來引導調整 imatinib 的劑量,結果顯示可以有較高的療效反應11。因此對於治療反應不佳、出現嚴重不良反應、有交互作用的可能、有較高的低服藥配合度風險或曾進行重大胃切除手術的病人,可能可以優先考慮在 imatinib 的療程中執行 TDM。目前已有二個運用 imatinib TDM 的思考流程可供參考:一、2015年日本 Miura 提出 imatinib TDM 可用於反應不佳或出現無法忍受之不良反應的 CML 病人,以協助決定是否需調整劑量或是更換為第二代 TKI (圖二)15。二、2012年英國 Judson 提出 imatinib TDM 可能使用在進階型 GIST 的思考流程 (圖三)。
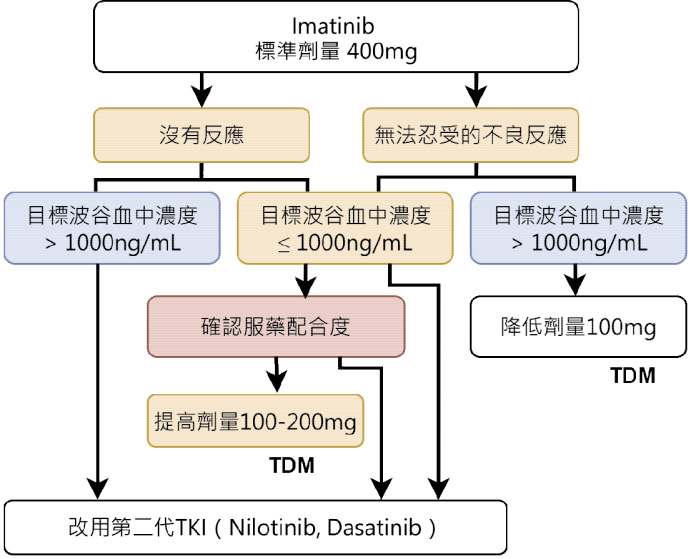
圖二 2015年日本 Miura 提出 imatinib TDM 用於 CML 的治療策略15
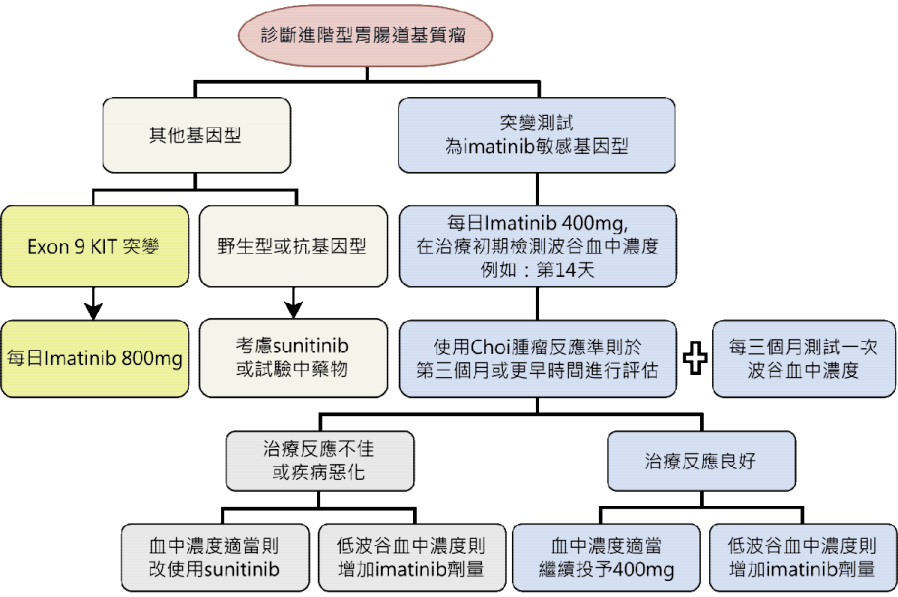
圖三 2012年英國 Judson 提出 imatinib TDM 可能的用途3
總而言之,imatinib TDM 在藥物治療上可能帶來協助包含:一、及早發現藥物的暴露量偏低,可避免治療效果不彰。二、若病人的實際暴露量偏高,可調整劑量以減少副作用。三、可幫助了解病人的服藥配合度。四、可幫助了解病人是否有因服用其他藥物而造成暴露量的改變。五、可幫助了解病人是否有因生理上的改變而造成暴露量的改變。六、提供醫療人員與病人個人化的參考資訊,以使治療能達最佳狀態,而達到藥事經濟學上的效益。
隨著科技進步,imatinib TDM 已有能快速、方便且準確的檢測技術可以提供數值給臨床參考14,能讓更多病人受惠。許多癌症治療的藥物和疾病更有結合運用 TDM 及藥物基因體學檢測的趨勢,可協助醫師給予病人個人化的藥物治療,而在這當中藥師責無旁貸,我們若能積極了解目前最新的研究和突破,就可提供病人更多的機會和協助,imatinib 是其中一個可以努力的例子。
Therapeutic Drug Monitoring of Imatinib: Clinical Significance and Practicability
Chien-Hua Wu, Chun-Wei Huang, Lian-Kwung Lin, Chun-Ta Huang
Pharmacist, Uni Pharma Co., Ltd.
Medical Research Manager, Uni Pharma Co., Ltd.
Abstract
Several studies demonstrated that fixed dose imatinib has great interpatient trough concentration variability in chronic myeloid leukemia (CML) and gastrointestinal stromal tumor (GIST). Besides, researchers have revealed that imatinib trough concentration in the steady state has a correlation with clinical efficacy in CML and advanced GIST. Those who have better response have higher imatinib trough concentration. Instead of significant interpatient pharmacokinetic variability, imatinib has extremely low adherence, high drug cost and long-term administration requirement. These reasons make imatinib a suitable candidate for therapeutic drug monitoring (TDM). It is worthwhile to discuss and investigate the clinical significance and the practicability of imatinib TDM.
參考資料:
1.Gao B, Yeap S, Clements A, et al: Evidence for therapeutic drug monitoring of targeted anticancer therapies. J Clin Oncol. 2012;30(32):4017-25.
2. Widmer N, Bardin C, Chatelut E, et al: Review of therapeutic drug monitoring of anticancer drugs part two--targeted therapies. Eur J Cancer. 2014;50(12):2020-36.
3. Judson I: Therapeutic drug monitoring of imatinib--new data strengthen the case. Clin Cancer Res. 2012;18(20):5517-9.
4. Picard S, Titier K, Etienne G, et al: Trough imatinib plasma levels are associated with both cytogenetic and molecular responses to standard-dose imatinib in chronic myeloid leukemia. Blood. 2007;109(8):3496-9.
5. Bouchet S, Poulette S, Titier K, et al: Relationship between imatinib trough concentration and outcomes in the treatment of advanced gastrointestinal stromal tumours in a real-life setting. Eur J Cancer. 2016;57:31-8.
6. Al-Barrak J, Cheung WY: Adherence to imatinib therapy in gastrointestinal stromal tumors and chronic myeloid leukemia. Support Care Cancer. 2013;21(8):2351-7.
7. Koren-Michowitz M, Volchek Y, Naparstek E, et al: Imatinib plasma trough levels in chronic myeloid leukaemia: results of a multicentre study CSTI571AIL11TGLIVEC. Hematol Oncol. 2012;30(4):200-5.
8. Larson RA, Druker BJ, Guilhot F, et al: Imatinib pharmacokinetics and its correlation with response and safety in chronic-phase chronic myeloid leukemia: a subanalysis of the IRIS study. Blood. 2008;111(8):4022-8.
9. Bouchet S, Titier K, Moore N, et al: Therapeutic drug monitoring of imatinib in chronic myeloid leukemia: experience from 1216 patients at a centralized laboratory. Fundam Clin Pharmacol. 2013;27(6):690-7.
10. Guilhot F, Hughes TP, Cortes J, et al: Plasma exposure of imatinib and its correlation with clinical response in the Tyrosine Kinase Inhibitor Optimization and Selectivity Trial. Haematologica. 2012;97(5):731-8.
11. Rousselot P, Johnson-Ansah H, Huguet F, et al: Personalized Daily Doses of Imatinib By Therapeutic Drug Monitoring Increase the Rates of Molecular Responses in Patients with Chronic Myeloid Leukemia. Final Results of the Randomized OPTIM Imatinib Study. Blood. 2015;126(23):133.
12. Demetri GD, Wang Y, Wehrle E, et al: Imatinib plasma levels are correlated with clinical benefit in patients with unresectable/metastatic gastrointestinal stromal tumors. J Clin Oncol. 2009;27(19):3141-7.
13. Eechoute K, Fransson MN, Reyners AK, et al: A long-term prospective population pharmacokinetic study on imatinib plasma concentrations in GIST patients. Clin Cancer Res. 2012;18(20):5780-7.
14. Beumer JH, Kozo D, Harney RL, et al: An Automated Homogeneous Immunoassay for Quantitating Imatinib Concentrations in Plasma. Ther Drug Monit. 2015;37(4):486-92.
15. Miura M: Therapeutic drug monitoring of imatinib, nilotinib, and dasatinib for patients with chronic myeloid leukemia. Biol Pharm Bull. 2015;38(5):645-54.

