摘要
轉移性大腸直腸癌 (mCRC) 的藥物治療原則為:一、RAS 原生型第一線可單用化療,或是化療併用 EGFR 抑制劑 [常用 cetuximab (CET)],或是化療併用 bevacizumab (BV);第二線則單用不同於第一線的化療藥品,或是化療併用 BV,或是 FOLFIRI 併用 aflibercept (或 ramucirumab);第三線可使用 regorafenib;二、RAS 突變型使用 EGFR 抑制劑無效,因此第一線只能單用化療,或是化療併用 BV。
第一線使用 BV,無論併用 FOLFIRI 或 FOLFOX,兩組之無惡化存活期和整體存活期皆無統計學上顯著差異,在台灣幾乎都是併用 FOLFIRI,其原因主要是因為受限於健保給付的規定。RAS 原生型第一線標靶藥物要選擇 BV 或 CET 仍有爭議,臨床上傾向以 BV 作為第一線治療,而將 CET 列為第三線治療。對於原發於右側大腸的 mCRC 患者不應併用 CET,因為沒有任何額外效益。未來加入免疫治療單獨使用或是合併其他藥物將使得 mCRC 的治療更加多元化。
關鍵字:轉移性大腸直腸癌、標靶治療、藥物治療策略、metastatic colorectal cancer、cetuximab、bevacizumab壹、前言
隨著許多有效的化療藥物與新一代標靶藥物的上市,近十年來轉移性大腸直腸癌 (metastatic colorectal cancer, 以下簡稱 mCRC) 病人的存活情況已大幅改善;然而如何組合這些藥物用在第一線及其後線治療,仍是現今 mCRC 治療的挑戰。本文將探討 mCRC 的藥物治療策略,特別在化療與標靶藥物併用的議題上。
貳、治療 mCRC 的藥物選擇
一、常用的化療藥物組合
FOLFOX [FOLinic acid (leucovorin)/ Fluorouracil (5-FU)/OXaliplatin]、FOLFIRI [FOLinic acid/Fluorouracil/IRInotecan] 、 XELOX [XELoda/OXaliplatin]。以上是常見的組合,並不是只有這些組合。也可視情形選擇單一化療藥物。其中5-FU 是嘧啶類似物的抗代謝劑,可阻斷 DNA 合成; oxaliplatin 可嵌入 DNA 內來抑制 DNA 複製;irinotecan 會抑制第一型拓樸異構酶 (topoisomerase I),導致 DNA 無法複製;leucovorin 則可增強5-FU 的藥效。Xeloda (capecitabine) 是唯一口服藥物,它進入體內會轉變成5-FU 以發揮其抗癌效果。
二、標靶藥物
(一)表皮生長因子受體 (epidermal growth factor receptor,EGFR) 抑制劑
由於癌細胞過度表現 EGFR,而這類藥品可抑制 EGFR ,如此可抑制腫瘤生長。藥品有單株抗體 cetuximab (Erbitux)、 panitumumab (Vectibix),健保皆有給付。
(二)作用於血管內皮生長因子 (vascular endothelial growth factor,VEGF) 路徑的藥品
由於癌細胞製造 VEGF,造成腫瘤的血管形成,使得腫瘤生長;而這類藥品可阻斷 VEGF 路徑,因此可抑制腫瘤生長。藥 品包括健保有給付的單株抗體 bevacizumab (Avastin),它可選擇性結合 VEGF 並中和其生物活性;以及目前健保尚未給付的 aflibercept (Zaltrap),此藥品是一個基因重組的融合蛋白質,包含了 VEGF 接受器 (VEGF receptor,VEGFR) 第一型和第二型的結合區,換言之,aflibercept 乃是一人工合成的 VEGFR,其與 VEGF 的親和力遠大於內源性 VEGFR,因此它可阻斷 VEGF 與其內源性接受器結合。另外,美國 FDA 有核准單株抗體 ramucirumab (Cyramza) 用於治療 mCRC,它是第二型 VEGFR 抑制劑,但此藥在台灣尚未取得衛福部 mCRC 適應症,只取得胃癌和非小細胞肺癌適應症。
(三)多重酪胺酸激酶抑制劑
藥品為口服的 regorafenib (Stivarga)。由於接受器酪胺酸激酶 (receptor tyrosine kinase) 和細胞的生長、分化、存活、凋亡有關,而此藥品是小分子,可進入細胞內抑制許多接受器酪胺酸激酶,VEGFR 是其中之一,如此可達到抗腫瘤的效果。健保有給付此藥品。
參、 mCRC 第一線、第二線、第三線治療原則1
一、 RAS 原生型 (RAS wild type, 以下簡稱 RAS WT)
即 RAS 沒有突變。RAS WT 是指所有的 RAS 皆沒有突變,包括 KRAS exon2,3,4以及 NRAS exon 2,3,4。RAS WT 第一線可單用化療,或是化療併用 EGFR 抑制劑,或是化療併用 bevacizumab (以下簡稱 BV);第二線則單用不同於第一線的化療藥品,或是化療併用 BV,或是 FOLFIRI 併用 aflibercept (或 ramucirumab);第三線可使用 regorafenib,若第一線沒有使用到 EGFR 抑制劑,則第三線可使用 EGFR 抑制劑。
二、 RAS 突變型 (RAS mutation type,以下簡稱 RAS MUT)
RAS MUT 者不可使用 EGFR 抑制劑, 因為無效。因此這類病人第一線只能單用化療,或是化療併用 BV ;第二線同 RAS WT;第三線為 regorafenib。
由於受限於健保給付,在台灣 RAS MUT mCRC 第一線治療藥物會選擇 FOLFIRI 併用 BV;第二線為 FOLFOX;第三線為 regorafenib,而 RAS WT mCRC 的治療策略則有多種選擇 (圖一),其中策略B在臨床上最常被使用。
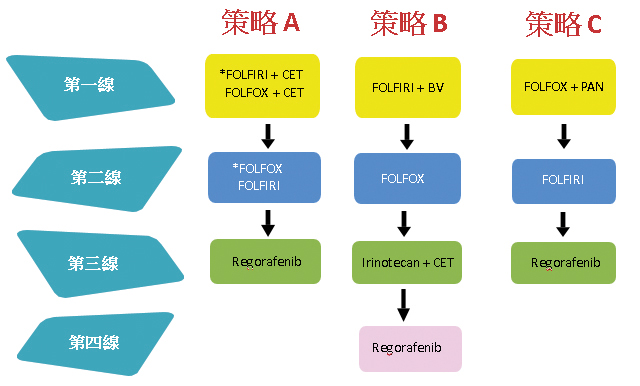
圖一 在台灣針對 RAS 原生型轉移性大腸直腸癌的藥物治療策略 (考量到健保給付)
肆、第一線使用化療合併標靶藥物
EGFR 和 VEGF 為目前標靶藥物的主要抑制標的。近年來數項研究針對化療併用標靶藥物作為第一線治療 mCRC 的療效進行探討,綜合數據和統合分析發現:
一、 BV 併用 FOLFIRI 與 BV 併用 FOLFOX 的比較
WJOG-4407G 第三期研究顯示,比較 BV 併用 FOLFIRI 和 BV 併用 FOLFOX,兩組無論在無惡化存活期 (progression - free survival,PFS) 和整體存活期 (overall survival,OS) 上皆沒有明顯差異,雖然 BV 併用 FOLFIRI 組的 OS 些微較長 (31.4 vs. 30.1個月)2。試驗期間兩組皆有將近一半的病人因疾病惡化而終止治療,而 BV 併用 FOLFIRI 組的病人因副作用而拒絕治療的比率較低。此外,接受 BV 併用 FOLFIRI 治療的病人當中,其 OS 與是否出現早期腫瘤縮小 (early tumor shrinkage,ETS,治療8週時腫瘤縮小超過20%則認為有 ETS) 有顯著的相關性,若有達到 ETS 者其 OS 明顯延長;然而此現象並未於 BV 併用 FOLFOX 組觀察到3。推測 ETS 在未來應可作為 FOLFIRI 之療效預測指標。
MAVERICC 第二期試驗結果也和 WJOG-4407G 研究一致,第一線使用 BV,無論併用 FOLFIRI 或 FOLFOX,兩組之 PFS 和 OS 皆無統計學上顯著差異4。在病人可持續治療的情況下,BV 併用 FOLFIRI 組的 OS 有優於 BV 併用 FOLFOX 組的趨勢 (27.5 vs. 23.9個月,HR 0.76,p = 0.086)4。
目前在台灣第一線使用 BV 的化療組合幾乎都是併用 FOLFIRI,其原因主要是因為受限於健保給付的規定。
二、BV 併用化療與 cetuximab (CET) 併用化療的比較
FIRE-3試驗比較 BV 併用 FOLFIRI 和 CET 併用 FOLFIRI,結果顯示兩者之 PFS 沒有差異,OS 則 CET 併用 FOLFIRI 勝出 (表一)5。然而,CALGB/SWOG 80405試驗比較 BV 併用化療 (FOLFIRI 或 FOLFOX) 和 CET 併用化療,結果顯示兩組無論在 PFS 或 OS 上皆無顯著差異 (表一)6。目前對於 RAS WT 之 mCRC 病人第一線標靶藥物要選擇 BV 或 CET 仍有爭議。臨床上傾向以 BV 作為第一線治療,而將 CET 列為第三線治療,主要原因是受限於健保只給付 BV 用在 mCRC 的第一線治療,而 CET 則健保可給付在第三線治療。
三、EGFR 抑制劑併用 oxaliplatin 為基礎的化療組合
MRC COIN 研究告訴我們,EGFR 抑制劑不建議和 XELOX 併用,因為效果差;而是應該與 FOLFOX 併用7。
表一 第三期臨床試驗 FIRE-3與 CALGB/SWOG 80405的比較5,6

伍、第二線及其後線藥物治療 mCRC
一、EGFR 抑制劑和 BV 的使用順序
第二線或第三線使用 EGFR 抑制劑的療效與第一線是否使用 BV 有關,有使用 BV 者其療效變差8。其原因與使用 BV 後造成細胞缺氧因而誘發 RAS 活化有關9。此外,研究發現若第一線使用 BV 治療失敗後,應將 EGFR 抑制劑放在第三線,因為第二線使用 EGFR 抑制劑時其療效明顯變差10。反之,第一線使用 EGFR 抑制劑則可調控 VEGF,如此有利於後續 BV 的治療9。綜合上述,EGFR 抑制劑可以第一線使用;又對於第一線使用 BV 者,EGFR 抑制劑應放在第三 線,而不是第二線。
二、Regorafenib
作用機轉為多重酪胺酸激酶抑制劑,可抑制腫瘤血管新生和腫瘤生長。健保給付條件是必須所有治療皆無效的 mCRC 病人,其治療包括 fluoropyrimidine、oxaliplatin、irinotecan 為基礎的化療、bevacizumab、EGFR 抑制劑 (若 RAS 為原生型)。使用本藥品要注意手足皮膚反應 (hand-foot skin reaction,HFSR) 的副作用,會引起皮膚發紅、水泡、過度角質化,病人可能因 HFSR 導致必須減量或停止使用本藥品。
陸、腫瘤原發位置與存活期的關係11
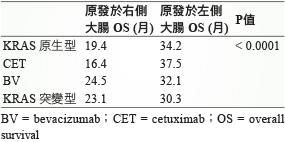
研究顯示 mCRC 病人若原發於左側大腸 (降結腸、乙狀結腸、直腸),其 OS 明顯比右側大腸 (盲腸、升結腸) 延長;橫結腸的結果類似右側大腸。同樣地,接受 CET 或 BV 治療者也是左側大腸的 OS 明顯比右側大腸延長,尤其是 CET 的結果更是驚人,左側大腸的 OS 足足比右側大腸延長21.1個月 (表二)。 根據此研究,臨床上對於原發於右側大腸的 mCRC 患者幾乎不會使用 CET。
表二 mCRC 病人之不同的腫瘤原發位置對於存活期的影響11
柒、免疫治療
癌症免疫治療是現今癌症治療的新潮流,其中免疫檢查點抑制劑 (immune checkpoint inhibitors,簡稱 ICIs) 已有不少突破性新藥,例如 ipilimumab、nivolumab、 pembrolizumab、atezolizumab。起初嘗試 ICIs 治療大腸直腸癌 (CRC) 的結果均顯示無效;然而後續研究發現針對『 DNA 錯誤配對修復機制有缺陷 (mismatch repair deficiency, dMMR)』或稱為『微衛星不穩定 (microsatellite instability, MSI)』的 CRC 病人單獨使用 pembrolizumab 就有高達 40%的反應率,若不屬於此族群的 CRC 病人,也就是『DNA 錯誤配對修復機制無缺陷 (mismatch repair proficiency, pMMR)』或稱為『微衛星穩定 (microsatellite stability, MSS)』者使用 pembrolizumab 的反應率則為0%,兩者有十分明顯的差別12。因此未來對於 MSI 的 CRC 病人可考慮選擇 ICIs。不過遺憾的是 CRC 中屬於 MSI 者比例偏低, 尤其 mCRC 病人中只有4%,對於絕大部份屬於 MSS 的 CRC 患者的免疫治療將是我們需要努力的課題。最近有一個小型第一期臨床試驗發現將 atezolizumab 合併 MEK 抑制劑 cobimetinib [MEK 即 MAPKK (mitogen- activated protein kinase kinase) 可活化 MAPK] 用來治療 MSS CRC 得到不錯的效果,其治療反應率可達20%13,這個初步結果令人振奮,後續研究仍在進行中。
捌、結論
現今治療 mCRC 的藥物已有多樣選擇,包括化療、作用於 EGFR 和 VEGF 路徑的標靶藥物,然而如何合理使用這些藥物需考慮多重因素,包括實證、病人本身狀況、腫瘤表現及位置、疾病進程、健保給付、病人意願;換句話說,mCRC 的治療是需要因人而異採取個人化的治療。具有 EGFR 表現且 RAS WT 之 mCRC 患者才能使用 EGFR 抑制劑。未來加入免疫治療單獨使用或是合併其他藥物將使得 mCRC 的治療更加多元化。
Drug Treatment Strategies for Metastatic Colorectal Cancer
Chi-Yuan Cheng, Tzu-Cheng Tsai
Department of Pharmacy, Chang Gung Memorial Hospital, Linkou
Abstract
The principles of drug treatment for metastatic colorectal cancer (mCRC) are: (1) RAS wild type: first-line with chemotherapy +/- EGFR inhibitor [cetuximab (CET) often used] or chemotherapy +/- bevacizumab (BV), second-line with chemotherapy (unlike first-line) +/- BV or FOLFIRI + aflibercept (or ramucirumab), third-line with regorafenib; (2) RAS mutant type: EGFR inhibitor is ineffective, hence, first-line only with chemotherapy +/- BV.
Fist-line treatment with BV plus FOLFIFI was not statistically significant difference compared with BV plus FOLFOX in terms of progression-free survival and overall survival for mCRC patients, in Taiwan FOLFIRI combination is preferred due to reimbursement limitation. Targeted agents of BV or CET, which one should be as the first-line choice for RAS wild type subjects is still controversial, although BV as first-line and CET as third- line are favored in clinical. mCRC arising in the right-sided colon should not add CET because there was no any additional benefit. In the future, cancer immunotherapy alone or in combination with other drugs will diversify mCRC treatment.
參考資料:
1.Sanz-Garcia E, Grasselli J, Argiles G, et al: Current and advancing treatments for metastatic colorectal cancer. Ex- pert Opin Biol Ther 2016;16:93-110.
2. Yamazaki K, Nagase M, Tamagawa H, et al: Random- ized phase III study of bevacizumab plus FOLFIRI and bevacizumab plus mFOLFOX6 as first-line treatment for patients with metastatic colorectal cancer (WJOG4407G). Ann Oncol 2016;27:1539-46.
3. Nagase M, Yamazaki K, Tamagawa H, et al: The impact of early tumor shrinkage on survival in WJOG4407G trial, a randomized phase III trial of mFOLFOX6 plus beva- cizumab versus FOLFIRI plus bevacizumab in first-line treatment for metastatic colorectal cancer. J Clin Oncol 2015;33(suppl 3; abstr 679).
4. Lenz HJ, Lee FC, Yau L, et al: MAVERICC, a phase 2 study of mFOLFOX6-bevacizumab (BV) vs FOLFIRI- BV with biomarker stratification as first-line (1L) chemo- therapy (CT) in patients (pts) with metastatic colorectal cancer (mCRC). J Clin Oncol 2016;34(suppl 4S; abstr 493).
5. Heinemann V, von Weikersthal LF, Decker T, et al: FOL- FIRI plus cetuximab versus FOLFIRI plus bevacizumab as first-line treatment for patients with metastatic colorec- tal cancer (FIRE-3): a randomised, open-label, phase 3 trial. Lancet Oncol 2014;15:1065-75.
6. Venook AP, Niedzwiecki D, Lenz HJ, et al: CALGB/ SWOG 80405: Phase III trial of irinotecan/5-FU/leucovo- rin (FOLFIRI) or oxaliplatin/5-FU/leucovorin (mFOLF- OX6) with bevacizumab (BV) or cetuximab (CET) for patients (pts) with KRAS wild-type (wt) untreated meta- static adenocarcinoma of the colon or rectum (MCRC). J Clin Oncol 2014;32(suppl; abstr LBA3).
7. Maughan TS, Adams RA, Smith CG, et al: Addition of cetuximab to oxaliplatin-based first-line combination che- motherapy for treatment of advanced colorectal cancer: results of the randomised phase 3 MRC COIN trial. Lan- cet 2011;377:2103-14.
8. Sato Y, Matsusaka S, Suenaga M, et al: Cetuximab could be more effective without prior bevacizumab treatment in metastatic colorectal cancer patients. Onco Targets Ther 2015;8:3329-36.
9. Wainberg ZA, Drakaki A: The importance of optimal drug sequencing in metastatic colorectal cancer: biological rationales for the observed survival benefit conferred by first-line treatment with EGFR inhibitors. Expert Opin Biol Ther 2015;15:1205-20.
10. Cascinu S, Rosati G, Nasti G, et al: A phase III multi- center trial comparing two different sequences of second/ third line therapy (irinotecan/cetuximab followed by FOLFOX-4 vs. FOLFOX-4 followed by irinotecan/cetux- imab) in K-RAS wt metastatic colorectal cancer (mCC) patients refractory to FOLFIRI/Bevacizumab. J Clin On- col 2015;33(suppl; abstr 3582).
11. Venook AP, Niedzwiecki D, Innocenti F, et al: Impact of primary (1º) tumor location on overall survival (OS) and progression-free survival (PFS) in patients (pts) with met- astatic colorectal cancer (mCRC): Analysis of CALGB/ SWOG 80405. J Clin Oncol 2016;34(suppl; abstr 3504).
12. Le DT, Uram JN, Wang H, et al: PD-1 blockade in tu- mors with mismatch-repair deficiency. N Engl J Med 2015;372:2509-20.
13. Bendell JC, Kim TW, Goh BC, et al: Clinical activity and safety of cobimetinib (cobi) and atezolizumab in colorec- tal cancer (CRC). J Clin Oncol 2016;34 (suppl; abstr 3502).
通訊作者:鄭吉元/通訊地址:桃園市龜山區復興街5號
服務單位:林口長庚紀念醫院藥劑部藥師/聯絡電話:(O) 03-3281200 ext 2915

