摘要
Darunavir/ritonavir 兩者皆屬於 HIV-1蛋白酶抑制劑 (protease inhibitors, PI),具選擇性地與 HIV-1蛋白酶的活性部位結合進而抑制病毒 Gag-Pol polyprotein 前驅物的分裂反應,遏阻成熟病毒顆粒的形成。Ritonavir 具有強的 CYP3A 抑制能力,常以低劑量100- 200 mg 與其它 PI 併用,可加強其他 PI 的藥物血中濃度以提高療效 (boosted PI)。然有 0.5%的病人會因為使用 darunavir/ritonavir 引起肝炎反應 (如急性肝炎、細胞溶解性肝炎)。對於使用 darunavir/ritonavir 合併感染B或C型肝炎的 HIV 病人,出現肝功能異常 (包括嚴重的肝臟不良事件) 的風險則會更高1。
本案例報導一位40歲B型肝炎帶原之男性 HIV 感染者,過去曾有巨細胞病毒感染史,因對多種抗反轉錄病毒藥物具有抗藥性,接受 darunavir/ritonavir 及 raltegravir 長達2-3個月。病人肝功能在用藥前原先都處於正常值,直到開始使用 darunavir/ritonavir 及 raltegravir 2-3個月後,血清轉胺酶 (Aspartate aminotransferase, AST;Alanine aminotransferase, ALT) 及 total bilirubin 分別上升至244 U/L、206 U/L 及7.7 mg/dL,推測可能原因與病人本身有慢性B型肝炎病史,使用 darunavir/ritonavir 誘發肝炎發作有關。本文後續將討論此病人使用 darunavir/ritonavir 發生肝功能異常的可能機制以及預後,提醒臨床醫療人員對於使用 darunavir/ritonavir 有發生肝功能異常之風險。
關鍵字:darunavir、ritonavir、protease inhibitors、B型肝炎
壹、前言
蛋白酶抑制劑是目前廣泛被用來預防或治療 HIV 感染以及後天免疫缺乏症候群的藥物。目前可用的蛋白酶抑制劑都可能短暫地引起無症狀的血清轉氨酶升高,在臨床上罕見造成急性肝損傷,其中 atazanavir 以及 indinavir 能夠輕微提高間接膽紅素濃度2,3。 在 HBV 或 HCV 合併感染的患者中,使用含蛋白酶抑制劑的高效能抗逆轉錄病毒治療 (highly active antiretroviral therapy, HAART) 可能會造成慢性B型或C型肝炎惡化1,2,4,5。然而因為蛋白酶抑制劑通常與其它抗逆轉錄病毒藥物合併給藥,使得釐清藥物肝損傷的相關性難度大為增加。因此本文將討論一位有慢性B型肝炎病史之 HIV 感染者,且對多種抗反轉錄病毒藥物具有抗藥性,接受 darunavir/ritonavir 及 raltegravir 治療後,疑 似因使用 darunavir/ritonavir 誘發肝炎發作。
貳、案例報告
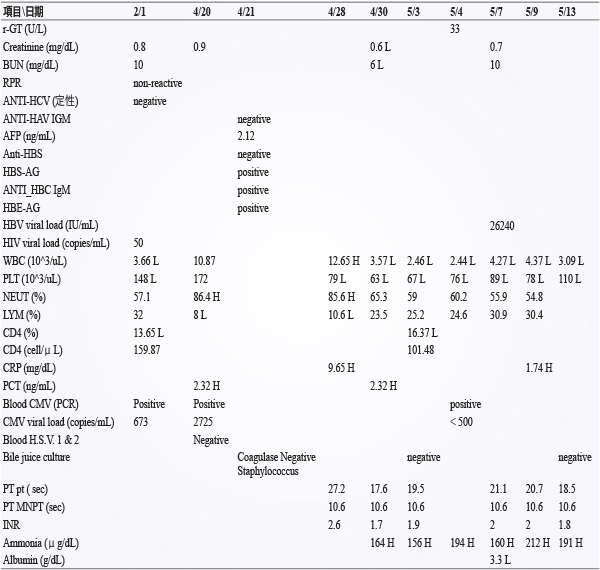
一位40歲男性病人,身高173公分,體重 56.6 公斤,戒菸多年,平時無喝酒、嚼檳榔或使用娛樂性藥物的習慣,為 B 肝帶原者,有第二型糖尿病與巨細胞病毒視網 膜炎等病史。於103/09 被發現感染 HIV 開始接受 HAART 治療,在104/10發現病人帶有 HIV 抗藥性基因 K65R、T69N、Y115F、 K101Q、Y181C、G190S、H221Y 對許多抗病毒藥物皆有抗藥性,105/02/01開始服用 darunavir 800 mg qd、ritonavir 100 mg qd、 raltegravir 400 mg q12h,接受前項藥物治療前 HIV viral load:50 copies/mL、CD4: 160 cells/μL、ALT/AST:27/21 U/L、total bilirubin:0.9 mg/dL、ANTI-HCV (定性): negative、CMV viral load:673 copies/mL、P. jirovecii (PCR):negative,治療期間病人規律回本院感染科門診就醫。在04/20病人抱怨發燒、肌肉酸痛、實驗室檢查 ALT、 AST 以及 total bilirubin 分別上升至206 U/L、 244 U/L、7.7 mg/dL、鹼性磷酸酶 (Alkaline phosphatase, ALP):112 U/L (圖一),因此入院接受檢查與治療。住院後,腹部電腦斷層報告顯示急性膽囊炎,立即接受經皮穿肝膽囊引流術治療,血液檢查 HBS-AG: positive、HBE-AG:positive、ANTI-HBC IGM:positive、Anti-HBS:negative、ANTI- HAV IGM :negative、AFP:2.21 ng/mL、 Blood H.S.V. 1 & 2:negative,被診斷為B 型肝炎帶原合併急性發作,04/22開始接受 entecavir 1 mg qd 治療。因為 CMV viral load 由673 copies/mL 上升至2725 copies/mL,且腹部電腦斷層報告懷疑 CMV hepatitis,04/27 開始接受 ganciclovir inj 500 mg q12h IV 治療。04/28肝功能檢查 ALT/AST:138/131 U/L 較入院時下降2倍,total bilirubin:19.7 mg/dL 較入院時上升2.5倍,意識狀態開始出現混亂且嗜睡,疑似藥物引起相關黃疸 而於04/30暫時停用 darunavir、ritonavir 與 raltegravir 使用。05/01追蹤肝功能檢查 ALT/ AST:77/87 U/L 較入院時下降2-3倍,total bilirubin 在停藥後由20.7 mg/dL 下降至16.7 mg/dL,INR 由2.6下降至1.7,Ammonia: 164μg/dL。在05/02醫師進行第二次給藥 darunavir 800 mg qd、ritonavir 100 mg qd、 raltegravir 400 mg q12h。05/03追蹤 CD4較 三個月前下降59 cells/μL 為101 cells/μL。 05/04追蹤 CMV viral load 為 < 500 copies/mL感染情形有獲得控制。05/07追蹤 HBV viral load 26240 IU/mL。05/09追蹤肝功能 total bilirubin 由16.4 mg/dL 上升至24.5 mg/dL,醫師停用 darunavir/ritonavir。05/12腹部超音波檢查顯示有肝硬化無腹水,肝功能抽血檢查 ALT/AST:65/91 U/L、total bilirubin:26.1 mg/dL 停用 raltegravir (表一、表二),Child- Pugh score 評估為11分顯示有嚴重肝硬化情形。因為家屬探視之方便性,05/14病人辦理轉院接受進一步治療。
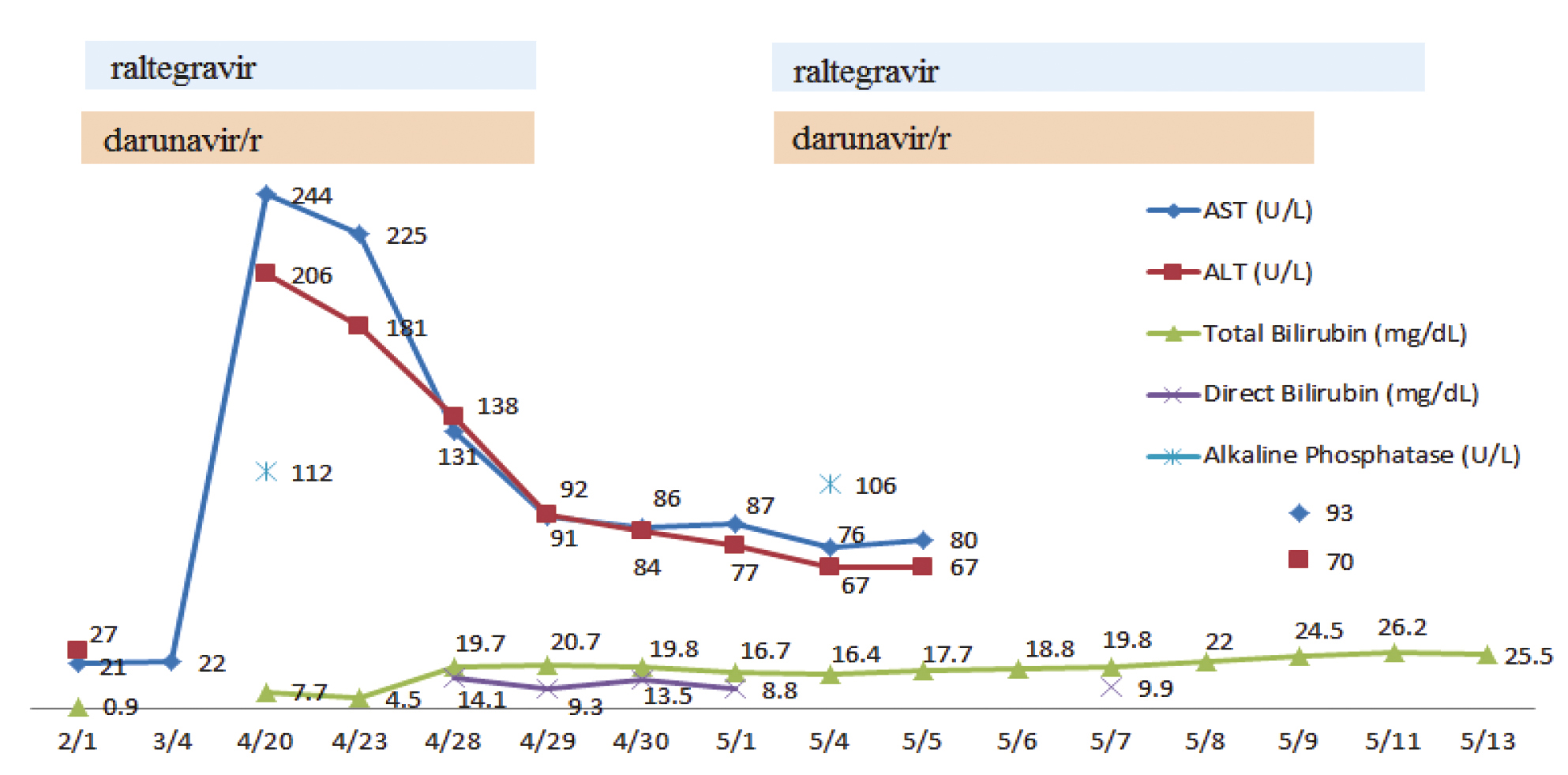
圖一 使用 darunavir/ritonavir 前後肝功能數值變化
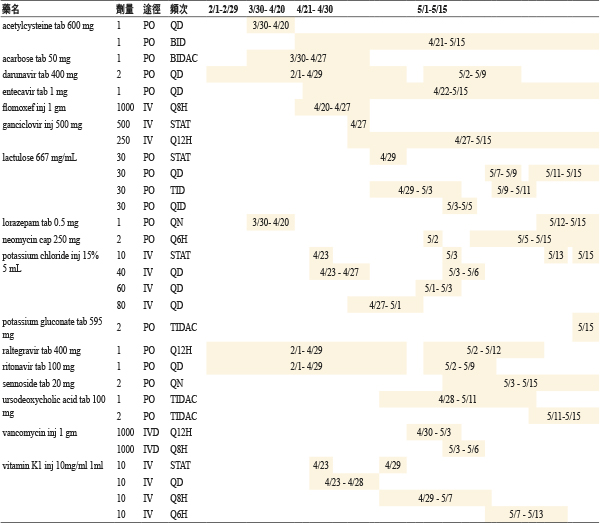
表一 用藥史
表二 檢驗報告
參、討論
一、Darunavir/ritonavir 引起肝炎發作之分析
個案在第一次使用 Darunavir/ritonavir 第80天出現 ALT、AST 以及 total bilirubin 分 別上升至206 U/L、244 U/L、7.7 mg/dL,腹部電腦斷層報告顯示為急性膽囊炎,血液檢查報告診斷為B型肝炎帶原合併急性發作, 隨後開始接受 entecavir 1 mg qd 治療急性B型肝炎發作,在第88天肝功能檢查 ALT/AST: 138/131 U/L 較入院時下降2倍,total bilirubin: 19.7 mg/dL 較入院時上升2.5倍,懷疑與使用 HARRT 藥物有關,醫師於第90天停用 darunavir、ritonavir 與 raltegravir。停藥後第 3天追蹤 total bilirubin 由20.7 mg/dL 下降至16.7 mg/dL,INR 由2.6下降至1.7。第二次使用 darunavir/ritonavir 與 raltegravir,用藥後第5天檢查 HBV viral load 26240 IU/mL, 第7天追蹤肝功能 total bilirubin 由16.4 mg/ dL 上升至24.5 mg/dL,腹部超音波檢查顯示肝硬化,醫師再次停用 HARRT 藥物。在 raltegravir 第 III 期臨床試驗研究中,HIV 感染者合併感染慢性 (不包括急性) 活動性B 型肝炎及/或C型肝炎的有治療經驗患者 (N= 114/699或16%) 及無治療經驗患者 (N = 34/563或6%) 出現 AST 及 ALT 異常現象的病人比例在兩個治療組中都有略為偏高的現象,但一般而言 raltegravir,在合併感染B型肝炎及/或C型肝炎之患者中的安全性表現和未合併感染B型肝炎及/或 C型肝炎的患者大致相當8-10,因此初步排除 raltegravir 與誘發 B型肝炎再活化之關聯性。另外,CMV 感染愛滋病人較常引起的併發症,包括:視網膜炎、大腸炎、間質性肺炎、肝炎等。肝炎的臨床表現影響是非常輕微,ALP 會上升,但 bilirubin 卻很少上升。CMV 感染會造成愛滋病人膽道系統潰瘍而形成硬化性膽管炎及總膽管至十二指腸出口的乳突狹窄,進而變成纖維化狹窄11。病人入院後經腹部電腦斷層檢查懷疑有 CMV hepatitis,04/27開始接受 ganciclovir inj 500 mg q12h IV 治療,住院期間追蹤ALP 與入院時比較皆無顯著變化,且在經由藥物的治療後 CMV viral load 從2725 copies/mL 下降至 < 500 copies/mL。 雖然,無法完全排除肝炎與 CMV 感染之關聯性,但從個案的用藥紀錄、疾病的進展以及文獻的佐證,疑似與 darunavir /ritonavir 誘發B型肝炎再活化有關。根據 AIDS inf 藥物交互作用2與 Lexicomp Drug interaction 查詢結果6,darunavir/ritonavir 與入院前或住院期間藥物併用無顯著交互作用存在。本案例亦使用 RUCAM7評分表來評估 darunavir/ ritonavir 造成肝毒性的潛在可能性,病人入院當天檢查 ALT/ALP:206/112 U/L,R ratio 為1.84,R < 2肝損傷的類型判斷為膽汁淤積型,其結果顯示具有可能性 (得分為6分)(表 三)。
表三 RUCAM 評分表7

二、HAART 造成肝毒性的機制及預後
抗逆轉錄病毒藥物引起的肝損傷 (drug induced liver injury, DILI),也可以從幾種病理生理機制來討論。例如引起過敏反應常見的藥物有 abacavir、nevirapine、ritonavir-boosted fosamprenavir。造成肝臟粒線體毒性主要為 dideoxynucleosides 類藥物例如 stavudine 或 didanosine。根據文獻報告幾乎所有 ritonavir- boosted 蛋白酶抑制劑皆可能引起肝臟脂肪變性。直接肝細胞應激 (direct liver cell stress) 常見於大多數 non–nucleosides 類藥物造成,例如 efavirenz 和 nevirapine 以及蛋白酶抑制劑 tipranavir。最後,免疫重建為所有使用抗逆轉錄病毒藥物的病人皆可能發生,對於伴隨病毒性肝炎共同感染的患者風險則會增加。預後主要取決於肝損傷的類型,肝細胞損傷型具有肝衰竭或肝硬化的高風險。而膽汁淤積型與混合型對於急性肝損傷則具有良好的預後,大多數的病人都可以完全恢復8。 另外,有文獻指出在免疫重建的過程中也可能會誘發B型肝炎的發作4。證據顯示過去有慢性病毒性肝炎的 HIV 患者是誘發肝指數上升的重要影響因素,若使用蛋白酶抑制劑來治療疾病則可能會增加肝臟轉氨酶升高的風險,其機制尚不清楚5。Darunavir/ritonavir 可能造成5.6-6.9%的病人 ALT 嚴重的上升4。從臨床試驗 phase IIb (POWER I、II 和 III) 分析次群組肝炎與 HIV 共同感染者,對照組為使用其他蛋白酶抑制劑的病人,這些病人在治療前的肝功能皆為正常,研究發現使用 darunavir/ritonavir 與肝炎共同感染者其肝臟轉胺酶會顯著上升8。Darunavir/ritonavir 造成肝炎的表現最初呈現低水平的肝臟轉胺酶上升,AST 和 ALT 升高正常上限的2-5倍,鹼性磷酸酶可能不受影響,如果持續使用 darunavir/ritonavir 將會造成進一步肝損傷包 括膽紅素大於正常上限的2倍、白蛋白降低以及最終 INR 上升4。有專家提出使用 HAART 藥物與 B/C 型肝炎病毒交互作用相關的肝臟 轉胺酶上升一般在幾個月內不會發生,故建議至少每三個月定期追蹤肝功能4。此病人過去有B肝帶原病史,使用 darunavir/ritonavir 與 raltegravir 治療 HIV 感染長達2-3個月,在第3個月發生急性B型肝炎發作,雖然,在住院期間歷經二次藥物停用,最後病人仍出現肝硬化情形,推測跟使用 darunavir/ritonavir 引起B型肝炎再活化有關。
三、研究限制
作者針對文章發表內容證據不足的地方做進一步討論,若個案為非藥物引起B型肝炎再活化,有許多文獻提到蛋白酶抑制劑也可能造成肝毒性發生,其中,使用全劑量 ritonavir 有最高的風險,故無法完全排除藥物直接造成肝細胞毒性的可能性。病人後來疾病進展為肝硬化,也可能降低 cytochrome P450活性,導致蛋白酶抑制劑暴露增加,毒性也可能會增加。另外,因為無 HBV viral load 基準值可以做比較,僅靠單點數值呈現可能較難讓人信服。此外,案例報告型態的文章常因醫療過程的執行無法完整提供相關證據來討論,也是本文受限的地方。
肆、結論
在治療 HIV 以及有相關合併症患者如老化,多重用藥,B型肝炎或C型肝炎共同感染,以及免疫重建等必須要特別留意。病毒性肝炎病史必須用實驗室測試結果證實。在用藥後臨床醫師需要隨時注意病人疾病的進展。最後,希望藉由此案例可以提醒醫療人員,對於有慢性肝炎病史之 HIV 病人使用蛋白酶抑制劑後可能有肝炎發作之風險,建議對肝功能進行密切的監測。
A Case Report of Suspected Darunavir with ritonavir Induced Recurrence of Hepatitis
Sheng-Ru Lin1, Ning-Chi Wang2, Cheng-Chin Hsien1
Department of Pharmacy1, Division of Infectious Diseases and Tropical Medicine2,
Tri-Service General Hospital
Abstract
Protease inhibitors (PIs) act selectively binding to the active site of human immunodeficiency virus (HIV)-1 protease, inhibiting the cleavage of the virus Gag-Pol polyprotein precursor, and then preventing the formation of mature virus particles. Darunavir and ritonavir both are PIs. Ritonavir has highly Cytochrome P450 3A inhibitory capacity and is often used in combined to other PIs to increase the serum drug concentration. A HIV positive patient with hepatitis B or C who used darunavir and ritonavir may has higher risk of abnormal liver function or severe hepatic adverse events.
A case report of a hepatitis B and HIV male carrier with the past history of cytomegalovirus infection and multiple antiretroviral drugs resistance used darunavir, ritonavir and raltegravir for 2-3 months. The liver functions (aspartate aminotransferase and alanine aminotransferase) and total serum bilirubin increased to 244 U/L, 206 U/L and 7.7 mg/dL, respectively. The possible mechanisms of drug reactions have been discussed and remind to health care professionals being aware.
參考資料:
1.Rivero A, Camacho A, Perez-Camacho I, et al: Darunavir in HIV/HVC/HVB coinfection. Enferm Infecc Microbiol Clin. 2008; 26 (Suppl 10):37-42.
2.Clinical guidelines on the use of antiretroviral agents in HIV-1 infected adults, adolescents and children. Available at http://aidsinfo.nih.gov/guidelines.(cited:05/20/2017)
3.Livertox database. Available at https://livertox.nlm.nih. gov/ProteaseInhibitors.htm. (cited:05/01/2017)
4.Ann S, David W, Soo CC: Complex Interactions of Da- runavir in Patients with HIV and Multiple Comorbidities: Understanding Toxicity in Two Cases with Very Different Outcomes. J AIDS Clin Res. 2014, 5:11.
5. Morsica G, Bianchi G, Bagaglio S, et al: Hepatic safety profile of darunavir with low-dose ritonavir (DRV/r) in HIV/HCV coinfected and HIV monoinfected patients. New Microbiol. 2011; 34:317-21.
6. Lexicomp® Drug interaction. Available at http:// www.uptodate.com. (cited:05/20/2017)
7. Gaby D, Rolf T: RUCAM in Drug and Herb Induced Liver Injury: The Update. Int J Mol Sci. 2016 Jan; 17(1): 14.
8.Surgers L, Lacombe K: Hepatoxicity of new antiretro- virals: a systematic review. Clin Res Hepatol Gastroen- terol.2013 Apr;37(2):126-33.
9.Isentress®藥品仿單。
10.Hurt CB, Napravnik S, Moore RD: Hepatic safety and tol- erability of raltegravir among HIV patients coinfected with hepatitis B and/or C. Antivir Ther. 2014;19(4):415-22.
11.Drew WL: Nonpulmonary manifestations of cytomega- lovirus infection in immunocompromised patients. Clin Microbiol Rev. 1992; 5:204-10.
通訊作者:林聖茹/通訊地址:台北市內湖區成功路二段325號
服務單位:三軍總醫院臨床藥學部藥師/聯絡電話:(O) 02-87923311

