摘要
近年來由於針對發炎反應中特定成分的生物製劑陸續被開發出來,革新了類風溼性關節炎的治療,目前的生物製劑涵蓋不同的作用機制以達治療效果,但生物製劑的治療可能增加感染風險。本案例是一名49歲女性病人,罹患類風濕性關節炎19年,在使用 tocilizumab 治療三個月後發生右前臂的蜂窩性組織炎。抽血檢驗發現,白血球值正常、嗜中性白血球及C反應蛋白數值稍微上升。在投予抗生素治療十二天後改善。兩個月後醫師再次投予 tocilizumab,蜂窩性組織炎復發,以 Naranjo score 評估表評分為6分,為極有可能相關之藥物不良反應。本案例報告的目的在提醒醫療人員使用生物製劑時,必須對可能發生嚴重感染提高警覺。
關鍵字:tocilizumab、rheumatoid arthritis、cellulitis、infection
壹、前言
近年由於治療類風濕性關節炎的生物製劑蓬勃發展,提供醫師對於治療困難的病人更多選擇。面對治療選擇的增加,醫師不只需要考量藥物的療效,更需要考量治療可能產生的風險,而生物製劑最顯著的風險之一即是感染1。本案例報告使用 tocilizumab 引起反覆性蜂窩性組織炎,藉此提醒醫療人員使用生物製劑治療時,應密切注意病人可能引發感染之併發症,以維護病人用藥安全。
貳、案例報告
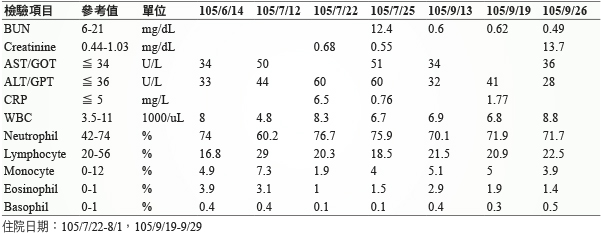
一位49歲女性病人,身高157公分,體重57公斤,過去無藥物及食物過敏記錄。病人於30歲時被診斷罹患類風溼性關節炎,在外院以 prednisolone 及 methotrexate 每週10 mg 治療, 因症狀漸續惡化,故於104年9月轉至本院風濕過敏免疫科就醫。醫師根據病人症狀調整用藥至 prednisolone 每天15 mg 及 methotrexate 每週 15 mg 治療,並於104年12月加入 leflunomide 每天20 mg 以控制病情 (表一)。由於症狀並未明顯改善,疾病活動指數28 (DAS28, disease activity score by 28 joints) 之分數為7.88,因此於105年4月19日開始 tocilizumab 大約每公斤體重4 mg 之劑量治療。三個月後 DAS28分數仍高達7.05分,故增加 tocilizumab 之劑量至每公斤體重8 mg。病人於104年7月18日晚上感覺右手前臂及手背疼痛腫脹並伴隨灼熱感,隨後有水泡出現,因而前往苗栗為恭醫院急診求治,並於105年7月21日自行至本院治療。於本院急診時,病人之右前臂及手背呈現嚴重發紅、發熱、腫脹及許多瘀青出血點 (圖一), 詢問病人病史,並未接觸任何化學藥劑或受到蟲咬,也未有發燒、咳嗽、頭痛等症狀。抽血檢查發現白血球值8300/uL、嗜中性白血球值76.7%及C反應蛋白值 (C-Reactive Protein, CRP) 6.5 mg/L。在蜂窩性組織炎診斷下,在急診先給予 oxacillin 2 g 每六時施打一劑,並於105年7月22日住院治療,給予 amoxycillin 1000 mg + clavulanic acid 200 mg 每八小時施打一劑,住院中右前臂之都普勒 (Doppler) 檢查,確認並無深部靜脈血栓,且血液細菌培養為陰性。病人治療後,症狀及生化血液值改善 (表二),於105年8月1日出院。出院後回門診追蹤暫停使用 tocilizumab。病人於105年 9月13日回診時,關節炎評估,其 DAS28分數為5.18分,醫師再度給予 tocilizumab 每公斤體重8 mg 治療。病人於105年9月18日出現右前臂及手背發紅腫脹之情形,因為蜂窩性組織炎復發,因此於105年9月19日入院治療。此次抽血檢驗結果,發炎相關數值皆正常 (表二)。住院時,醫師以 amoxycillin 1000 mg + clavulanic acid 200 mg 每八小時施打一劑治療,手臂腫脹發紅情形獲得改善後,105年9月21日改為 cefazolin sodium 每八小時施打1克之劑量治療,血液細菌培養亦為陰性,病人於105年9月 28日出院。返家後,口服投予 cefadroxil 500 mg 一天兩次持續治療七天,並以 DMARDs 藥物治療類風濕性關節炎,暫停使用生物製劑。
表一 病人用藥記錄

表二 實驗室檢驗值
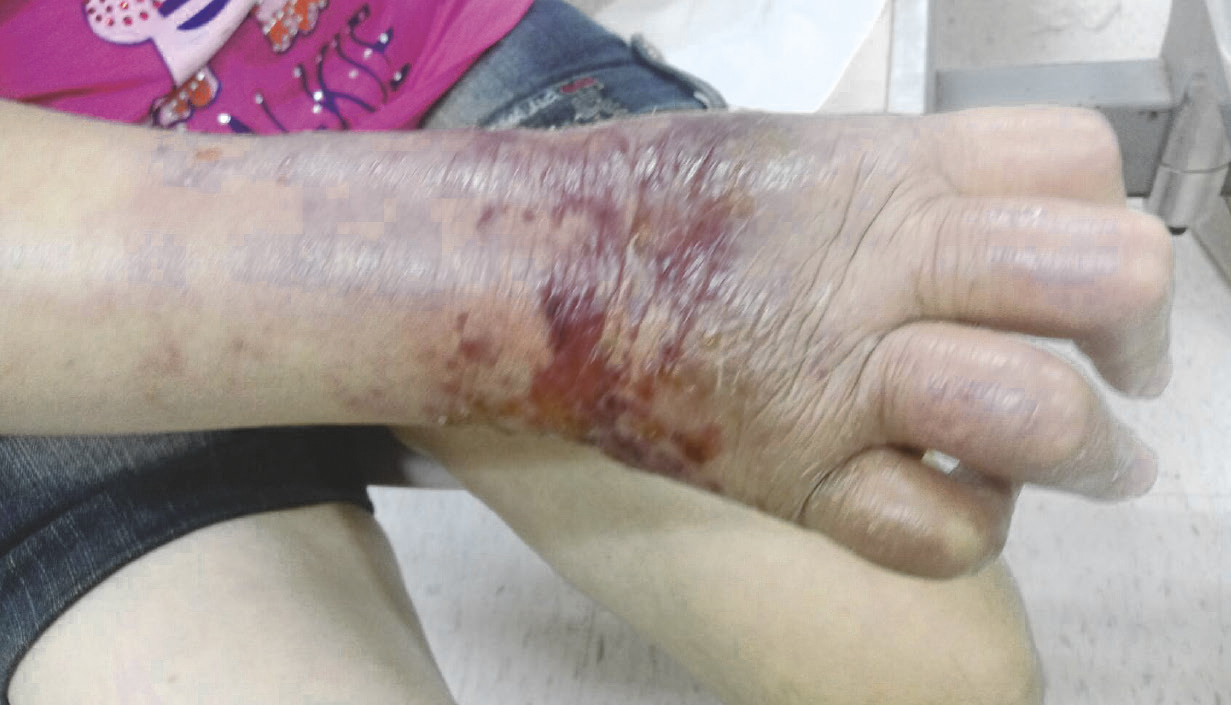
圖一 病人右手臂及手背之蜂窩性組織炎
參、討論
一、類風溼性關節炎之治療
目前類風濕性關節炎主要使用的藥物包括非類固醇抗發炎藥 (NSAIDs)、類固醇、疾病修飾抗風濕病藥 (disease modifying anti- rheumatic drugs,DMARDs),以及生物製劑等。由於細胞激素及免疫細胞在類風濕性關節炎之致病機制中扮演重要角色,因此近期發展出對抗這些標靶之生物製劑。美國風溼病醫學會、歐洲抗風濕病聯盟及亞太風濕醫學會治療建議,DMARDs 仍為類風濕性關節炎治療的第一線藥物,可單獨使用或合併治療。當 DMARDs 治療無效時,建議可利用生物製劑進行疾病的控制2-4 。已核准的生物製劑當中,有些是直接抑制發炎物質例如抗腫瘤壞死因子 (tumor necrosis factor-α, TNF-α)、第六介白質 (interleukin-6, IL-6), 另外也有對抗免疫細胞,例如 T細胞及B細 胞等6。抗腫瘤壞死因子的生物製劑有 soluble receptor 及單株抗體,是治療類風濕性關節炎最先問世之生物製劑,包括 etanercept、 infliximab、adalimumab、golimumab 及 certolizumab pegol1。Tocilizumab 為人類第六介白質受體之單株抗體 IgG1,能與第六介白質受體 (IL-6R) 結合,阻斷發炎反應與後續之關節損傷5。Rituximab 可與B淋巴細胞上的 CD20抗原結合,使 CD20+ B細胞減少。Abatacept 是一種融合蛋白,藉與 CD80/ CD86結合而抑制T細胞活化。目前許多臨床試驗證實這些生物製劑對於治療類風濕性關節炎的效果相似,但由於其結構及作用機轉有差異,所以治療效果也有個體上的差異6。 這些生物製劑,比傳統之 DMARDs 能更快更有效控制病情。
二、 安全性之實證研究:新一代生物製劑之感染議題
由於生物製劑抑制或阻斷某些細胞激素或T、B細胞,因此會增加感染的可能性6。常見的感染以下呼吸道感染為首,其次為皮膚及軟組織的感染,其他還包括骨關節感染及泌尿道感染1。由於抗腫瘤壞死因子是最早用於治療類風濕性關節炎的生物製劑,因此其安全性的研究最多。2006年一篇系統性回顧綜述,發現使用抗腫瘤壞死因子的單株抗體 infliximab 或 adalimumab 與對照組相比,產生嚴重感染的發生率是對照組的兩倍 (Odds ratio=2)。其嚴重感染的定義為導致住院,需靜脈注射抗生素或死亡的感染7。至於 tocilizimab 也有系統性的回顧研究,結果發現 tocilizumab 相較於對照組並未有顯著增加嚴重感染的風險,但是若使用較高的劑量 (8 mg/kg),則產生嚴重感染的風險比對照組增加1.3倍 (Odds ratio = 1.3)8。針對其他生物製劑之嚴重感染發生率的系統性回顧研究,如 abatacept 及 rituximab,相較於對照組未增加嚴重感染的風險,但在高劑量下產生嚴重感染的風險比對照組增加9,10。近期針對使用生物製劑產生嚴重感染的系統性回顧研究,將使用劑量分成三種劑量範圍:標準劑量 (美國 FDA 核准之劑量範圍)、高劑量 (高於標準劑量) 及低劑量 (低於標準劑量),進行安全性分析,結果以標準劑量或高劑量治療類風溼性關節炎之病人,發生嚴重感染的風險顯著高於使用低劑量生物製劑的病人11。
2014年一篇收入了70篇研究的系統性回顧,研究當時已核准的生物製劑與 DMARDs 相比,病人發生伺機性感染的風險增加 (Odds ratio= 1.79)12。伺機性感染包括李斯特菌、諾卡氏菌,非傷寒沙門氏菌和非結核分枝桿菌等感染。此外,也可能發生病毒,真菌或寄生蟲的感染,包括帶狀或單純皰疹、水痘、肺囊蟲、隱球菌和利甚曼病等感染。而且使用生物製劑會增加 Mycobacterium tuberculosis 感染的發生率,因此在使用生物製劑前,必須先檢測是否有潛在性的結核感染,並給予適當的防治性藥物13,14。
三、國外文獻案例討論及不良反應評估
Tocilizumab 為人類第六介白質受體單株抗體,可抑制發炎因子 C 反應蛋白 (C-Reactive Protein,CRP) 的製造,因此當病人使用 tocilizumab 發生蜂窩性組織炎時,其抽血檢驗數值增加往往並不明顯。日本曾報告兩例因為使用 tocilizumab 發生蜂窩性組織炎15,案例一為62歲女性,有七年的類風溼性關節炎病史,以每四週給予 tocilizumab 8 mg/kg 治療,在第六個週期施打完畢後的二十天,病人被所飼養的寵物狗輕咬右手肘,七天後至醫院主述右手肘局部紅腫疼痛但未伴隨發燒。抽血檢驗結果,CRP 值正常,白血球及嗜中性白血球數目正常,但較過去基準值稍微增加,病人的症狀在投與抗生素盤尼西林後三天緩解。案例二為49歲女性,有二十年的類風溼性關節炎病史,同樣以每四週給予 tocilizumab 8 mg/kg 治療,於第五個週期發生左手局部紅腫疼痛且伴隨發燒,但未有任何咬傷或刀傷的紀錄。抽血檢驗結果 CRP 值正常,白血球及嗜中性白血球數目較過去基準值稍微增加,症狀也在投與抗生素後緩解。此國外兩案例在症狀緩解後,再次投與 tocilizumab 並未再出現蜂窩 性組織炎的症狀。本案例與其比較,在施打的第四週期發生蜂窩性組織炎,發生時間較早,抽血檢驗結果呈現白血球數值正常,嗜中性白血球數目及 CRP 值稍微增加,雖然症狀在投予抗生素後緩解,但再次投與 tocilizumab 蜂窩性組織炎復發。探討本案例之藥物不良反應相關性,以 Naranjo score 評估表評分為6分 (表三),此案例「極有可能」因使用 tocilizumab 引起反覆性蜂窩性組織炎。CRP 是由肝臟製造出的急性期反應物 (acute phase reactant),受到人類第六介白質的調控。因此當使用 tocilizumab 時,不建議使用 CRP 值的上升當作感染的指標。以本案例及國外的兩案例發現,病人的白血球數目及 CRP 值皆不太會上升,因此必須對感染的臨床表徵提高警覺15。
表三 藥物不良反應相關性—Naranjo Score 評估表

肆、結語
本案例因使用 tocilizumab 引起蜂窩性組織炎,其白血球數值及 CRP 值未明顯上升,因此臨床上對於感染症狀需保持高度警覺,如局部紅、腫及發熱等症狀,可作為蜂窩性組織炎的依據;發生腹痛等症狀,需警覺是否為憩室炎,不建議以白血球數值及 CRP 值作為感染之判斷。本案例報告旨在提醒醫療人員使用生物製劑時,需要密切留意感染的併發症,確保用藥安全。
Tocilizumab Induced Recurrent Cellulitis: A Case Report
Ya-Fang Cheng1, Shue-Fen Luo2, Tzu-Cheng Tsai1
Department of Pharmacy, Chang Gung Memorial Hospital, Linkou1
Department of Rheumatology, Allergy and Immunology,
Chang Gung Memorial Hospital, Linkou2
Abstract
The treatment of rheumatoid arthritis has been revolutionized in recent years by the development of biologics targeting specific components of inflammation. The current biological agents consist of different mechanisms to achieve therapeutic effects. It has been clear that biological agents may be associated with an increased risk of infections. We report a 49-year-old female with 19-year history of rheumatoid arthritis. She received intravenous tocilizumab treatment and developed right hand and forearm cellulitis three months later. Laboratory examination showed a normal WBC count, and the neutrophil and CRP level were only slightly increased. Cellulitis resolved after antibiotics treatment for twelve days. Tocilizumab was resumed two months later and patient had recurrent cellulitis. The Naranjo score was 6 points and this adverse drug event can be classified as probable. This case report is to alert clinicians for infections while using biological agents.
參考資料:
1.1.Manjari Lahiri, William G. Dixon: Risk of infection with biologic antirheumatic therapies in patients with rheuma- toid arthritis. Best Practice & Research Clinical Rheuma- tology 2015; 29: 290-305.
2.Jasvinder A. Singh, Kenneth G. Saag, S. Louis Bridges JR, et al: 2015 American College of Rheumatology Guideline for the Treatment of Rheumatoid Arthritis. Ar- thritis Rheumatol. 2016;68(1):1-26.
3.Josef S Smolen, Robert Landewé, Johannes Bijlsma et al: EULAR recommendations for the management of rheumatoid arthritis with synthetic and biological disease- modifying antirheumatic drugs: 2016 update. Ann Rheum Dis 2017; 0:1-18.
4.Chak Sing LAU, Faith CHIA, Andrew HARRISON et al: APLAR rheumatoid arthritis treatment recommendations. International Journal of Rheumatic Diseases 2015; 18: 685-713.
5.Nishimoto N, Hashimoto J, Miyasaka N, et al: Study of active controlled monotherapy used for rheumatoid arthri- tis, an IL-6 inhibitor (SAMURAI): evidence of clinical and radiographic benefit from an x ray reader-blinded ran- domized controlled trial of tocilizumab. Ann Rheum Dis 2007;66(9):1162-1167.
6.James R. O' Dell: Therapeutic Strategies for Rheumatoid Arthritis. N Engl J Med 2004;350: 2591-602.
7.Bongartz T, Sutton AJ, Sweeting MJ, et al: Anti-TNF antibody therapy in rheumatoid arthritis and the risk of serious infections and malignancies: systematic review and meta-analysis of rare harmful effects in randomized controlled trials. JAMA 2006;295(19):2275-2285.
8.Campbell L, Chen C, Bhagat SS, et al: Risk of adverse events including serious infections in rheumatoid arthritis patients treated with tocilizumab: a systematic literature review and meta-analysis of randomized controlled trials. Rheumatol Oxf 2011; 50(3): 552-562.
9.Van Vollenhoven RF, Emery P, Bingham III CO, et a: Long-term safety of rituximab in rheumatoid arthritis: 9.5- year follow-up of the global clinical trial programme with a focus on adverse events of interest in RA patients. Ann Rheum Dis 2013; 72(9): 1496-1502.
10.Alten R, Kaine J, Keystone E, et al: Long-term safety of subcutaneous abatacept in rheumatoid arthritis: integrate analysis of clinical trial data representing more than four years of treatment. Arthritis Rheumatol 2014; 66(8): 1987-1997.
11.Singh JA, Cameron C, Noorbaloochi S, et al: Risk of seri- ous infection in biological treatment of patients with rheu- matoid arthritis: a systematic review and meta-analysis. Lancet. 2015; 386:258-265.
12.Kourbeti IS, Ziakas PD, Mylonakis E. Biologic therapies in rheumatoid arthritis and the risk of opportunistic infec- tions: a meta-analysis. Clin Infect Dis 2014; 58(12): 1649-1657.
13. 陳怡行、蘇維鈞、謝松洲等:2015年修訂版風濕病醫 學會免疫風濕病患接受腫瘤壞死因子抑制劑類生物製 劑結核感染篩檢與防治共識建議。Formosan Journal of Rheumatology 2015; 29:1-8.
14. Dixon WG, Hyrich KL, Watson KD, et al: Drug-specific risk of tuberculosis in patients with rheumatoid arthritis treated with anti-TNF therapy: result from the British Society for Rheumatology Biologics Register (BSRBR). Ann Rheum Dis. 2010;69(3):522-528.
15. Syed Farhan Bari, Afsha Khan, Tom Lawson: C reactive protein may not be reliable as a marker of severe bacterial infection in patients receiving tocilizumab. BMJ Case Rep 2013; 1-2.
通訊作者:鄭雅芳/通訊地址:桃園市龜山區復興街5號
服務單位:林口長庚紀念醫院藥劑部藥師/聯絡電話:(O) 03-3281200 ext 3730

