摘要
每個癌細胞都要分裂,包括癌細胞也要分裂成兩個細胞,而 CDK4/6 Cyclin-dependent kinase (細胞週期激酶) 是促進細胞分裂週期的重要蛋白,CDK4/6抑制劑會抑制癌細胞分裂,CDK4/6會藉由磷酸化一種腫瘤抑制蛋白 Rb (Retinoblastoma protien 視網膜母細胞瘤蛋白) 釋放 E2F (E2 transcription factor) 轉錄因子來調控細胞週期 G1到S期的進行,而 CDK4/6抑制劑則是阻止 Rb 蛋白磷酸化,使細胞停留在 G1期,使其不會進行週期而死亡。目前 FDA 核准的 CDK4/6抑制劑有:Palbociclib、Ribociclib 和 Abemaciclib1,2。
Palbociclib (IBrance 愛乳適) 是第一個我國食藥署核准上市的。Palbociclib 對管狀乳癌具有高度的活性,尤其是 ER 陽性乳癌。Palbociclib 與抗雌激素藥物併用可抑制 Rb 磷酸化作用,從而增強 Rb 再活化作用,致使 E2F 訊息傳遞降低及生長停滯;利用病人 ER 陽性乳癌異種移植模型 (HBCx-34) 所進行的活體試驗顯示,palbociclib 與 letrozole 併用可進一步增強對 Rb 磷酸化的抑制作用、下游訊息傳遞及劑量依賴性腫瘤生長抑制作用3,4。
關鍵字: CDK4/6、PARP inhibitor、palbociclib、olapari
壹、前言
三陰性乳癌細胞的分化常呈現高惡性度,更易有淋巴結轉移。相同期別下,復發的機會較其他類型的乳癌為高,腦部轉移的比例也高。一旦轉移或復發,可用的藥物治療選擇又比其他類型少,因此預後很差。三陰性型乳癌在初次治療後的1-3年為復發高峰期,之後會顯著降低至與其他類型接近的程度。另外,三陰性乳癌的病人帶有 BRCA1突變的機會較高,根據西方國家的資料,三陰性型的乳癌病人有 BRCA1基因缺陷比例達25%,而一般乳癌病人則為2%。BRCA1/2 基因突變和遺傳性乳癌相關,BRCA2基因突變引起的乳癌臨床上可能是 ER 陽性,但 BRCA1絕大多數臨床上為三陰型表現,所以藉由 PARP inhibitor 製劑被發明,為我們帶來治療新契機。
乳癌抑制基因 (如 Breast Cancer1/2,BRCA1/2) 可以透過同源重組 (homologous recombination,HR) 的方式修復受損的去氧核醣核酸 (deoxyribonucleic acid, DNA),一旦 BRCA1基因突變便會導致乳癌,治療 BRCA1時雖對鉑金類藥物敏感,但癌細胞可能透過 PARP (poly ADP-Ribose polymerase) 的鹼基切除方式來抑制聚腺苷酸二磷酸核糖轉移酶 (Poly ADP-Ribose Polymerase, PARP),或週期素依賴激酶 (cyclin dependent kinase,CDK) 的藥品研發成為近年主流。
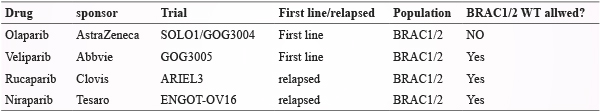
PARP 是一種去氧核醣核酸 (deoxyribonucleic acid,DNA) 修復酶,能測知 DNA 的結構損傷片段而被激活,進行聚腺苷二磷酸核糖基化,癌細胞會利用 PPAR 使其得以不斷的生長與增殖;PARP 抑制劑便是讓乳癌細胞的 DNA 無法及時修復,致使細胞週期中斷而凋亡,目前經藥政單位核准上市的有 Lynparza (Olaparib)、Rubraca (Rucaparib)、Zejula (Niraparib) (表一)7,8。
表一 PARP inhibito r 系列藥物比較7,8
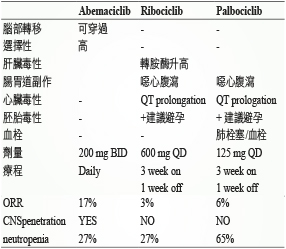
CDK 是細胞週期中的關鍵因素之一,CDK4/6會磷酸化視網膜母細胞瘤蛋白 (Retinoblastoma protien,Rb) 釋放 E2F (E2 transcription factor) 轉錄因子來調控細胞週期 G1到S期的進行,而 CDK4/6抑制劑則會停止癌細胞分裂,是阻止 Rb 蛋白磷酸化,使細胞停留在 G1期,細胞週期無法進行而死亡1,2。目前經藥政單位核准上市的有「愛乳適」(Ibrance,Palbociclib) (表二)9。
表二 各總 CDK4/6藥物比較表9
貳、 CDK4/6抑制劑愛乳適 Ibrance (palbociclib 75/100/125毫克)
可與芳香抑制劑 (aromatase inhibitor) 合併使用。對於雌激素受體為陽性、第二型人類表皮生長因子受體 (HER2) 呈陰性之局部晚期或轉移性乳癌之婦女,Ibrance 可合併 fulvestrant 用於先前接受過內分泌治療者。停經前/停經前後婦女,接受內分泌治療應合併黃體生成素-釋放激素 (luteinizing hormone-releasing hormone;LHRH) 致效劑。
每日一次口服125毫克 palbociclib,連續治療21天後,停止治療7天,以28天為一個完整的週期。只要患者可獲得臨床效益,應持續使用 Ibrance 治療,或持續治療至出現無法接受的毒性反應為止,與 palbociclib 併用時,letrozole 的建議劑量為在整個28天週期中持續每天一次口服2.5毫克。與 palbociclib 併用時,fulvestrant 的建議劑量為於第1、15、29天肌肉注射500毫克,之後則每月注射一次。嚴重副作用需停藥在開始使用 Ibrance 治療之前、各週期開始時、最初2個週期的第14天、以及臨床顯示有必要時,應監測全血球計數。建議於絕對嗜中性白血球計數 (ANC) ≥ 1000/mm3且血小板計數 ≥ 50,000/mm3的情況下才可接受 Ibrance 的治療。輕度肝功能不全 (總膽紅素 ≤ 1倍正常值上限[ULN]且 [AST] > 1倍 ULN,或總膽紅素 > 1.0至1.5倍 ULN 且 AST 為任意值) 的患者,並不須調整 Ibrance 的劑量 (表三)10,11。
表三 白血球計數與 Ibrance 調整劑量方式10,11

對輕至中度腎功能不全 (肌酸酐廓清率[CrCl] ≥ 30毫升/分鐘) 的患者,並不需調整 Ibrance 的劑量。對重度腎功能不全 (CrCl < 30毫升/分鐘) 或需接受血液透析治療的患者,目前並無足夠的資料可作為劑量調整12。
一、藥物交互作用
在空腹狀態下,約有13%的人會出現 palbociclib 之吸收率與暴露量極低的現象。進食可使這小部份人的 palbociclib 暴露量升高,但不會使其他人的 palbociclib 暴露量發生具臨床關聯性之程度的改變。和在隔夜空腹狀態下投予 palbociclib 相比較,隨高脂食物投藥時,palbociclib 的 AUCinf 與 Cmax 分別會升高21%與38%,隨低脂食物投藥時分別會升高12%與 27%,於投予 palbociclib 的1小時前與2小時後進用中脂食物時則分別會升高13%與24%。此外,進食可使 palbociclib 之暴露量的個體間及個體內異性明顯降低:根據這些結果,palbociclib 應與食物並服。
因為 palbociclib 由 CYP3A 代謝,所以併用 CYP3A 抑制劑會使藥物濃度上升,和僅投與單劑125毫克的 palbociclib 相比較,合併200 mg itraconazole 會使 AUC 和 Cmax 分別升高87%和34%,應避免與強效 CYP3A4抑制劑併用包括 clarithrmycin、indinavir、itracozaole、ketocozaole、ritonavir13。
如果和 CYP3A 誘導劑併用會使 palbociclib 濃度下降,和僅投與125 mg palbociclib 合併600 mg,rifampin 會使 AUC 與 Cmax 分別降低85%和70%,併用 PPI (rabeprazole) 會使 pabociclib 的 AUC 和 Cmax 分別降低62%和80%。
二、臨床試驗
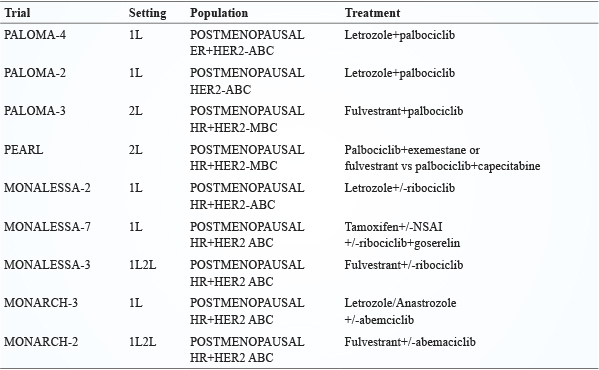
在 PALOMA3研究,後期或已轉移乳癌女性,且曾經接受內分泌治療失敗或再發,比較 palbociclib 加上內分泌治療 (fulvestrant),與只接受內分泌治療,對未惡化存活 (progression free survival, PFS) 的影響。在 PALOMA2研究則是與 Letrozole 併用 (表四)14。
表四 CDK4/6 inhibitor 臨床試驗比較由下面臨床試驗得知,由 CDK4/6抑制劑搭配芳香酶抑制劑效果都較比只用芳香酶抑制劑效果好14
參、Lynparza (50 mg olaparib)
建議起始劑量為200 mg (四粒50 mg 膠囊) 服用每天兩次每天總劑量400 mg,如需要減低劑量,那麼減少至100 mg (兩粒50 mg 膠囊) 服用每天兩次,每天總量200 mg 避免同時使用強度 CYP3A 抑制 clarithromycin、ketoconzole、vorconazole、ritinovir、indinavir、verapamil 降低 Lynparza 至150 mg (3粒50 mg 膠囊,有研究指出總共60和56例患者分別進行安全性和 PK 分析評估;57名患者進入了B部分。在食物存在的情況下,olaparib 吸收速度較慢 (Tmax 延遲了2.5 h),導致峰值血漿暴露量 (Cmax) 下降約21%(幾何平均值的比率為90%CI),所以盡量避免與高脂肪共餐使用,妊娠婦女避免服用避免致畸胎,也避免哺乳,孕婦分級為D級。
Olaparib 會引起骨隨增生 MDS/AML,若有肺炎要馬上停用 Lynparza,不良反應有貧血、噁心、嘔吐、頭痛、血小辦減少、中性球減少併用 CYP3A 抑制劑會使 olaparib 藥物濃度上升例如 voricoanazole/posaconazole/itraconaole/clarithromycin/nafcillin/如果真不能避免那就從400 mg BID 調降至150 mg BID。併用 CYP3A誘導劑會使 olaparib 藥物濃度下降,例如:amprenavir、aprepitant、atazanavir、crizotinib、darunavir、ritonavir、rifampicin (會降低 olaparib AUC 87%)、efavirenz (會降低 olaparib AUC 50-60%)15。
尚未研究肝受損對 Lynparza 暴露的影響。Lynparza 臨床試驗排除膽紅素 > 1.5 × ULN 和 AST/ALT ≥ 2.5 × ULN (存在肝轉移時 ≥ 5 × ULN) 的患者。根據初步數據,與腎功能正常的患者 (CLcr > 80 mL/min) 相比,輕度腎功能不全患者 (CLcr = 50-80 mL/min) 的平均暴露量 (AUC) 增加了1.5倍。對於 CLcr 為50-80 mL/min 的患者,不需要調整起始劑量的劑量,但應密切監測患者的毒性,中度或重度腎功能不全患者 (CLcr < 50 mL/min) 或透析患者無臨床症狀。
肆、總結
我國近六成乳癌患者為 ER (雌激素受體) 陽性,HER2 (表皮生長受體) 陰性;新標靶 CDK4/6抑制劑即是針對此類患者,CDK4/6抑制劑搭配荷爾蒙治療相較於只用荷爾蒙,PFS (即並無惡化存活期) 多出10.3個月,可達24.8個月,HER2陰性乳癌晚期治療選擇少,CDK4/6抑制劑為我們帶來治療新契機。
Potential Biomarkers of CDK4/6 Inhibitors In advanced Breast Cancer
Xing-Tong Liu
Department of Pharmacy, Kuang Tien General Hospital
Abstract
In normal cell cycle progression, transition of G0/G1 phase to synthesis (S) phase for breast and other cells is regulated by association of cyclin D and cyclin-dependent kinases 4 and 6 (CDK4/6) that leads to phosphorylation of retinoblastoma (Rb) protein. Imbalance of this cyclin D-CDK4/6-inhibitors of CDK4/6-Rb phosphorylation pathway is associated with tumorigenesis of hormone receptor-positive (HR+), human epidermal growth factor receptor 2-negative (HER2−) breast cancers. Despite effective first-line endocrine therapy, HR+/HER2− metastatic breast cancers remain still incurable. Currently, advances in understanding of cell cycle checkpoints are evolving as promising strategy to target in treatment of various types of cancers including breast cancer. Therapies that target this cell cycle machinery in HR+/HER2− breast cancers are getting approval by the US Food and Drug administration (FDA) including palbociclib.
參考資料:
1.Asghar U, Witkiewicz AK, Turner NC, Knudsen ES (2015) The history and future of targeting cyclin-dependent kinases in cancer therapy. Nat rev Drug discov 14(2):130-146. https://doi. org/10.1038/nrd4504.
2. Nwabo Kamdje AH, Seke Etet PF, Vecchio L, Muller JM, Krampera M, Lukong KE (2014) Signaling pathways in breast cancer: therapeutic targeting of the microenvironment. Cell Signal 26(12):2843-2856. https://doi.org/10.1016/j.cellsig.2014.07.034.
3. kinase Sioc-d, 4, 6 by PD 0332991 and associated antitumor activity in human tumor xenografts.Dickson MA (2014) Molecular pathways: CDK4 inhibitors for cancer therapy. Clin Cancer Res 20(13):3379–3383. https://doi.org/10.1158/1078-0432. CCR-13-1551.
4. Fry DW, Harvey PJ, Keller PR, Elliott WL, Meade M, Trachet E, Albassam M, Zheng X, Leopold WR, Pryer NK, Toogood PL (2004) Specific inhibition of cyclin-dependent kinase 4/6 by PD 0332991 and associated antitumor activity in human tumor xenografts. Mol Cancer Ther 3(11):1427-1438.
5. Cicenas J, Valius M (2011) The CDK inhibitors in cancer research and therapy. J Cancer Res Clin Oncol 137(10):1409–1418. https:// doi.org/10.1007/s00432-011-1039-4.
6. Roy R, Chun J, Powell SNNat Rev Cancer. 2011 Dec 23; 12(1):68-78.[PubMed] [Ref list]
7. Farmer H, McCabe N, Lord CJ, Tutt AN, Johnson DA, Richardson TB, Santarosa M, Dillon KJ, Hickson I, Knights C, Martin NM, Jackson SP, Smith GC, Ashworth A Nature. 2005 Apr 14; 434(7035):917-21.
8. Searchresults:RoscovitineANDbreastcancer. Available at http://clinicaltrials.gov/ct2/results? term5roscovitine1AND1breast1cancer. Accessed November 4, 2014.
9. DeMichele A, Sanders Clark A, Heitian D et al: A phase II trial of an oral CDK 4/6 inhibitor, PD0332991,in advanced breastcancer.JClinOncol 2013;31(suppl):519a.
10. DeMichele A, Sanders Clark A, Heitian D et al: A phase II trial of an oral CDK 4/6 inhibitor, PD0332991,in advanced breastcancer.JClinOncol 2013;31(suppl):519a.
11. Finn RS, Crown JP, Boer K et al: Results of arandomizedphaseIIstudyofPD-0332991,acyclin dependent kinase (CDK) 4/6 inhibitor, in combination with letrozole vs letrozole alone for first-line treatment of ER1/HER2- advanced breast cancer (BC) [abstract 1000]. Ann Oncol 2012;23(suppl 2): ii43-ii45.
12. Finn RS, Crown JP, Lang I et al: The cyclindependent kinase 4/6 inhibitor palbociclib in combination with letrozole versus letrozole alone as first-line treatment of oestrogen receptorpositive, HER2-negative, advanced breast cancer (PALOMA-1/TRIO-18):Arandomisedphase2study. Lancet Oncol 2015;16:25-35.
13. Ibrance (palbociclib) [prescribing information]. Available at http://www.accessdata.fda.gov/drugsatfda_docs/label/2015/207103s000lbl.pdf. Accessed February 24, 2015.
14. A study of palbociclib (PD-0332991) 1 letrozole vs. letrozole for 1st line treatment of postmenopausal women with ER1/HER2- advanced breast cancer (PALOMA-2). Available at http://clinicaltrials.gov/ct2/show/NCT01740427. Accessed November 4, 2014.
15. Targeting the DNA repair defect in BRCA mutant cells as a therapeutic strategy. Farmer H, McCabe N, Lord CJ, Tutt AN, Johnson DA, Richardson TB, Santarosa M, Dillon KJ, Hickson I, Knights C, Martin NM, Jackson SP, Smith GC, Ashworth ANature. 2005 Apr 14; 434(7035):917-21. [PubMed] [Ref list]
通訊作者:劉星彤/通訊地址:台中市大甲區經國路321號
服務單位:光田綜合醫院藥學部藥師/聯絡電話:(O) 04-26885599 ext 4145

