摘要
在多數國家,慢性腎臟病約有20%起因為腎絲球腎炎,此疾病最常侵犯年輕族群,往往會演變成末期腎臟疾病1。慢性腎絲球腎炎中,以A型免疫球蛋白腎病變發生率最高,且為造成慢性腎臟病、末期腎臟衰竭最主要原因之一2。改善全球腎臟病預後組織 (Kidney Disease: Improving Global Outcomes; KDIGO) 於2012制訂該疾病治療指引,本篇文章依照疾病診斷、治療與預後等面向並結合實證資料介紹此疾病,以案例進行討論,希望能使藥師們對於此疾病更加深入了解,提升照護品質。
關鍵字: IgA 腎炎、IgA 腎病變、腎絲球腎炎、IgA nephropathy、glomerulonephritis
在台灣,造成末期腎臟疾病四大原因依序為糖尿病、慢性腎絲球腎炎、高血壓、慢性間質性腎炎3。慢性腎絲球腎炎最常侵犯年輕族群1,當中以A型免疫球蛋白腎病變(immunoglobulin A nephropathy,簡稱 IgAN) 發生率最高,且為造成慢性腎臟病、末期腎臟衰竭最主要的原因之一2。
壹、流行病學
全球 IgAN 平均年發生率約0.2-2.9/十萬人。此疾病可能發生於任何年紀,其中以20至39歲的發生率最高。種族部分以亞洲人、高加索人發生率較黑人高。性別比方面,美國、歐洲研究中疾病發生率男女比為2:1,於亞洲族群發生率則男女比例相近。由於此疾病需靠尿液篩檢及腎臟切片才能確診,故疾病發生率又與該地區或國家之社經、衛生政策,如定期尿液篩檢、執行腎切片技術與安全性等皆有關4。在中國,於常規尿液篩檢出無症狀血尿者,後續進行腎切片約有45%顯示為原發性腎絲球腎炎;在日本,則約30-32.9%顯示為 IgA 腎炎。
貳、臨床表徵及診斷
IgAN 與大部分慢性腎絲球腎炎相似,臨床表現多樣化。輕微者或疾病初期可能有無症狀顯微血尿,通常於黏液相關感染後,如呼吸道、腸胃道感染後數天出現肉眼可見血尿,可能合併無症狀蛋白尿或腎病症候群;嚴重者可能出現疾病惡化快速的腎絲球腎炎。隨著疾病進展,可能出現水腫、蛋白尿、高血壓、腎功能惡化等情形。一般病人在罹患此疾病約20年後,可能進展至末期腎臟病。據美國統計,30歲以上病人首次被診斷為 IgAN 時,其疾病往往已進展至慢性腎臟病第三至五期。
目前沒有能特定針對 IgAN 的檢驗方法,初步可利用病史、臨床症狀與常規尿液檢查進行篩檢,欲確診需利用腎切片組織染色,如免疫螢光顯影,於組織切片中腎絲球系膜可發現明顯 IgA 免疫沉積物。在臨床上,是利用觀察腎絲球、腎小管等組織變化來評估疾病嚴重度與疾病預後5,IgAN 進展成 ESRD 在腎切片結構上會發現新月形壞死性腎絲球病變或嚴重的腎絲球硬化。
對於 IgAN 一般常使用 Oxford MEST-C 分類法來表示病理組織特徵,作為疾病嚴重度、預測預後重要因子,分別為:(一)腎絲球系膜過度增生、(二)微血管過度增生、(三)腎絲球硬化或沾黏、(四)腎小管間質性纖維化、(五)新月形形成,按照嚴重度給予不同等級,嚴重程度越高、分數越高。目前無明確證據顯示此疾病具有遺傳性,但在全基因組關聯分析 (Genome-wide association studies) 中發現15個常見風險變異基因。在東亞,出現風險基因的機率較高,可能是較高疾病盛行率的原因6。造成次發性 IgAN 的原因包含發炎性腸道疾病 (inflammatory bowel disease)、HIV、結核、肝炎、肝硬化、淋巴瘤等。
參、病理機轉
由於 IgAN 病人接受腎移植後仍會有復發情形,故 IgAN 往往被視為全身性疾病。近年來對於疾病機轉有較多認識,主要假說為多發病機制模型4-6:首先,產生結構缺乏半乳糖的 IgA1 (galactose-deficient IgA1, Gd-IgA1) 以及將 Gd-IgA1 視為自體免疫抗原的自體免疫抗體兩者結合,形成腎炎免疫複合體。腎炎免疫複合體沉積在腎絲球同時刺激系膜細胞,使系膜細胞增生、活化補體及過度製造細胞外基質、細胞因子、angiotensin II 等,可能影響腎絲球通透性、造成腎小管損傷。部分細胞因子造成足細胞損傷、凋亡,組織上呈現腎絲球硬化,而蛋白尿的發生與足細胞缺乏有關。
肆、治療方式
若只是輕微尿液檢查異常如孤立性血尿、沒有或有輕微的蛋白尿,但腎絲球過濾率 (GFR) 與血壓正常的病人僅需定期追蹤腎功能、蛋白尿、血壓等變化即可。目前針對此疾病沒有特效的治療方式7,主要仍以使用 renin–angiotensin system (RAS) blockade 類藥物作為血壓、蛋白尿控制用藥,其他則包含血脂控制、限鹽飲食、戒菸與避免腎毒性藥物。若持續中度至嚴重蛋白尿 (超過六個月,大於每日1 g)、控制不佳的高血壓 (> 140/90 mmHg) 以及腎功能持續惡化,則需要治療以減緩 IgAN 進展成 ESRD。
治療方式分為一般治療與免疫治療。一般治療部分,2012年改善全球腎臟病預後組織 (Kidney Disease: Improving Global Outcomes; KDIGO) 針對每日尿蛋白大於1 g患者建議長期使用 angiotensin-converting enzyme inhibitors (ACEI) 或 angiotensin-receptor blockers (ARBs) 可減少蛋白尿、減緩腎功能惡化。根據2013年的一篇系統性綜論8,使用 ACEI 或 ARB 約可減少每日0.73 g 尿蛋白 (95%信賴區間 [confidence interval; CI] 為每日減少0.39-1.06 g)。單獨使用 ACEI 或 ARB 時,血清肌酐酸 (serum creatinine; Scr) 沒有顯著變化。IgAN 病人使用降血壓藥物可控制血壓、減少蛋白尿,建議依照血壓調整藥物劑量。IgAN 合併每日尿蛋白小於1 g 者,血壓控制目標為小於130/80 mmHg;若每日尿蛋白大於1 g,血壓控制目標為小於125/75 mmHg。另外,魚油包含 omega-3不飽和脂肪酸,具有抗腎絲球發炎效果,該類病人可以使用魚油輔助治療,延緩 SCr 上升,但是在長期效果部分仍不明。
免疫治療部分,KDIGO 建議接受症狀治療 (包含 ACEI 或 ARB 至少3至6個月)、GFR > 50 mL/min 但每日尿蛋白仍大於1 g 者,使用高劑量、短療程的類固醇治療,建議療程為6個月,可減緩腎功能持續惡化、減少進展為 ESRD 之風險。2015年的一篇系統性綜論顯示9,單獨使用類固醇每日減少0.49 g 尿蛋白 (95% CI 每日減少0.25-0.72 g),進展為 ESRD 之風險降低約56%(risk ratio 0.44; 95% CI 0.25-0.8);使用類固醇合併 RAS 抑制劑降低約84%(risk ratio 0.16; 95% CI 0.04-0.59)。若病人腎功能快速惡化或組織切片出現新月形 (crescentic),KDIGO 建議使用其他免疫抑制劑如 cyclophosphamide 合併類固醇,可減少蛋白尿,但是並未顯著減少進展為末期腎臟疾病之風險。部分中國研究顯示,mycophenolate mofetil 可減少蛋白尿,但目前研究多為人數少、且追蹤期短的小型研究,仍需更多研究證明療效與安全性5。
伍、案例報告
個案為一25歲女性,身高159公分、體重96公斤。無特殊過去病史、過敏史。過去例行健康檢查發現無症狀血尿,2013年因腎結石接受體外震波術,2016年曾因肺炎住院治療,住院期間出現肉眼可見血尿,同時有持續數月下肢水腫、泡沫尿;同年5月至本院腎臟科門診就醫,除了接受相關抽血、尿液檢查,也安排腎切片進一步診斷。檢查結果 blood urea nitrogen (BUN):26 mg/dL、Scr:1.6 mg/dL,利用 CKD Epidemiology Collaboration 估算 eGFR:44 mL/min/1.73 m2,屬慢性腎臟病第三期。尿液檢查方面,尿蛋白:3+;urine protein and creatinine ratio:5 mg/g;24小時尿液檢測 daily protein loss:12.69 g/day。腎切片病理報告顯示腎絲球內系膜細胞增生、腎小管局部退化與萎縮、間質部分明顯發炎細胞浸潤、血管部分無明顯病變,初步病理診斷為間質性腎炎、不排除為 IgA 腎病變。同時也安排其他檢查,排除其他可能間接引起相似腎絲球腎炎的原因,如紅斑性狼瘡 (SLE)、肝炎、HIV 等。
個案於2016年5月開始一般治療,服用 valsartan 80 mg tab (PO) QD,但是病人反應使用後頭暈、血壓偏低,故僅有使用一週。於同月也開始免疫治療,使用 prednisolone 15 mg tab (PO) TID,兩週後因腸胃道副作用將劑量減低至 prednisolone 15 mg tab (PO) BID。
六月底病人出現水腫、體重增加、頭痛、嘔吐等症狀,同時檢測 albumin:1.9 g/dL 並住院治療,當時血壓偏高 (180/104 mmHg) 且 SCr 較以往上升至3.4 mg/dL、BUN:45 mg/dL,eGFR:18 mL/min/1.73 m2,診斷符合慢性腎臟病第四期。因腎功能持續惡化、血壓控制不佳,依照血壓變化調整降血壓藥品 valsartan 80 mg tab (PO) QD、nifedipine 30 mg tab (PO) QD、doxazosin 2 mg tab (PO) Q12H。十月,疑似腸胃道感染,腹瀉嚴重,腎功能急遽惡化,SCr 上升至8.4 mg/dL、BUN:56 mg/dL,eGFR:6 mL/min/1.73 m2,符合慢性腎臟病第五期診斷。入院給予脈衝治療 methylprednisolone 1 g (IV) QD,持續4天,後續以 prednisolone 20 mg tab (PO) BID 持續治療。關於此疾病治療用藥與相關檢驗數值 (表一~四)。
表一 治療藥物免疫治療
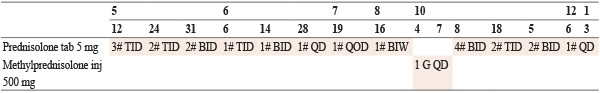
表二 治療藥物一般治療
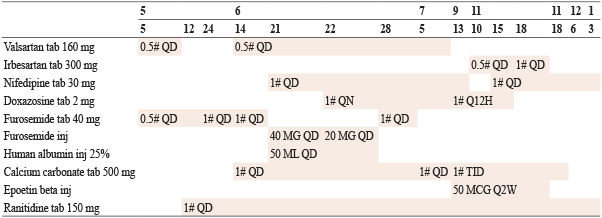
表三 相關檢驗數值-尿液檢查
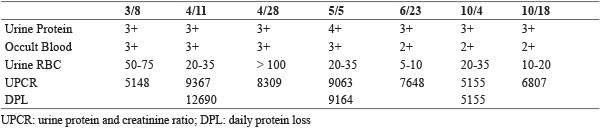
表四 相關檢驗數值-血液生化
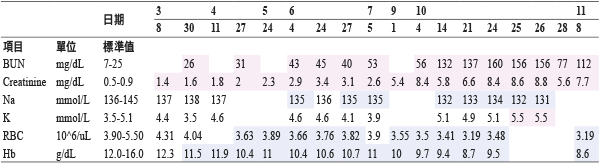
陸、討論
一、 當腎功能更差時,可以使用類固醇治療嗎?
病人自2016年5月底初診斷為 IgAN,當時 eGFR:44 mL/min/1.73 m2。KDIGO 治療指引建議 GFR > 50 mL/min 且持續蛋白尿患者使用類固醇治療,然而 GFR 介於30-50 mL/min 之間,甚至是腎功能更差的病人經常被相關試驗排除。VALIGA 回溯性世代研究收錄1,147位病人10,97%為白種人,利用 propensity scor 與次組別分析方式,針對 GFR < 50 mL/min 有使用類固醇組別,相對於僅使用 ACEI 或 ARB 組別,腎功能下降速率較緩慢且有更高比例病人可以達到減少每日蛋白尿。2017年全球類固醇用於 IgAN 治療評估11(Therapeutic Evaluation of Steroid in IgA Nephropathy Global; TESTING) 研究為多國多中心、雙盲、隨機對照試驗,收納 GFR 介於20-120 mL/min/1.73 m2 間、每日尿蛋白大於1 g,已接受 ACEI 或 ARB 至少三個月以上之 IgAN 患者,隨機分派接受高劑量類固醇 (口服0.6-0.8 mg/kg/day methylprednisolone) 或安慰劑至少兩個月,之後再以每月減少每日8 mg 藥物劑量,治療期6-8個月。然而此試驗因安全因素提前結束,因為使用高劑量類固醇發生嚴重不良反應高於安慰劑組的4.63倍 (95% CI 1.63-13.2)。試驗組中有11位 (8.1%) 受試者發生嚴重感染症,包含兩位因感染症死亡。在治療效益部分,使用類固醇可減緩腎功能下降、進展至 ESRD 風險。
綜合以上文獻的結論,針對 GFR < 50 mL/min 患者,使用類固醇治療仍可減少蛋白尿、延緩腎功能惡化,但是效果可能相對較差,且使用上須密切追蹤與類固醇相關副作用,如感染、糖尿病、骨質疏鬆等,尤其需注意使用高劑量類固醇其感染病發生率可能高於預期。
二、 當指引建議藥物無法使血壓控制達標,有無其他選擇?
當病人初診斷為 IgAN 時,GFR 為44 mL/min/1.73 m2,但蛋白尿情形嚴重 (每日尿蛋白 > 1 g),使用 valsartan 80 mg tab (PO) QD 治療,血壓控制目標為小於125/75 mmHg,疾病初期血壓控制良好。因為疾病惡化快速,出現水腫、頭痛等腎功能惡化症狀與血壓控制不佳。據2013年一篇系統性綜論指出8,降血壓藥物仍是最有效的非免疫治療,其中仍以 RAS blockade 或合併其他降血壓藥物可減少每日尿蛋白,但是對於減少其他重大腎臟或心臟血管風險、死亡率助益不顯著。其他藥物部分如鈣離子阻斷劑對於蛋白尿、腎功能惡化緩解、進展至 ESRD 無明顯效益。為讓血壓達到控制目標,仍建議合併不同作用機轉降血壓藥物控制血壓,故分別加上 nifedipine 及 doxazosine,依照血壓控制情形調整藥物劑量。按照目前治療,個案24小時尿蛋白4月為12690 mg,8月減少至3624 mg。
三、疾病預後
除了上述持續蛋白尿、控制不良高血壓,此個案有其他 IgA 腎病變不良預後因子,如肥胖、持續顯微性血尿、高三酸甘油脂等。IgA 腎病變10年腎臟存活率約為80-90%,罹患IgA 腎病變的病人12年後約有23%、20年後約有50%可能進展為末期腎臟病。病人於2016年10月初發生持續性腹瀉、疑似消化道相關感染,當時疾病進展至末期腎臟疾病,自初步診斷至進展至末期腎臟疾病時間不到一年,相對於大部份的病例來說進展快速。2016年11月已開始規則血液透析、2017年1月接受腎移植評估,至今仍等待腎移植。
柒、結論
IgA 腎病變是最常見的腎絲球腎炎,且此疾病大多侵犯年輕族群,及早確診並配合血壓、血脂等控制可減緩疾病進展或延長進展至末期腎臟病的時間。期待未來能對於疾病病理機轉更加深入了解,發展出侵入性更小的診斷方法以及更精準的醫療方式。而藥師可協助評估用藥並且提供相關疾病與藥物資訊、追蹤藥物可能副作用與不良反應,使病人照護更加完整。
Introduction to IgA Nephropathy with a Case Report
Yi-Fen Zou1, Ting-Ying Wang1, Chih-Wei Huang1, Cheng-Chih Hsieh2
Department of Pharmacy Practice, Tri-Service General Hospital1
Department of Pharmaceutical Management, Medical Affairs Bureau Ministry of National Defense2
Abstract
Glomerulonephritis account for about 20% of chronic kidney disease cases in most countries. IgA nephropathy (IgAN) frequently affects young people and is the most common primary glomerulonephritis that can progress to renal failure. KDIGO (Kidney Disease: Improving Global Outcomes) published a clinical practice guideline for glomerulonephritis in 2012. We summarize current evidence of IgAN diagnosis, treatment, prognosis with a case discussion, hoping to make everyone more aware of this disease and improve quality of medical care.
參考資料:
1.Floege J, Amann K. Primary glomerulonephritides. The Lancet. 2016;387(10032):2036-2048.
2. Zhang C, Zeng X, Li Z, Wang Z, Li S. Immunoglobulin A nephropathy: current progress and future directions. Transl Res. 2015;166(2):134-144.
3. Hwang SJ, Tsai JC, Chen HC. Epidemiology, impact and preventive care of chronic kidney disease in Taiwan. Nephrology (Carlton). 2010;15 Suppl 2:3-9.
4. Lai KN, Tang SC, Schena FP, et al: IgA nephropathy. Nat Rev Dis Primers. 2016;2:16001.
5. Wyatt RJ, Julian BA. IgA nephropathy. N Engl J Med. 2013;368(25):2402-2414.
6. Magistroni R, D'Agati VD, Appel GB, Kiryluk K. New developments in the genetics, pathogenesis, and therapy of IgA nephropathy. Kidney Int. 2015;88(5):974-989.
7. Radhakrishnan J, Cattran DC. The KDIGO practice guideline on glomerulonephritis: reading between the (guide)lines--application to the individual patient. Kidney Int. 2012;82(8):840-856.
8. Reid S, Cawthon PM, Craig JC, Samuels JA, Molony DA, Strippoli GF. Non-immunosuppressive treatment for IgA nephropathy. Cochrane Database Syst Rev. 2011(3):CD003962.
9. Vecchio M, Bonerba B, Palmer SC, et al: Immunosuppressive agents for treating IgA nephropathy. Cochrane Database Syst Rev. 2015(8):CD003965.
10. Tesar V, Troyanov S, Bellur S, et al: Corticosteroids in IgA Nephropathy: A Retrospective Analysis from the VALIGA Study. J Am Soc Nephrol. 2015;26(9):2248-2258.
11. Lv J, Zhang H, Wong MG, et al. Effect of Oral Methylprednisolone on Clinical Outcomes in Patients With IgA Nephropathy: The TESTING Randomized Clinical Trial. JAMA. 2017;318(5):432-442.
通訊作者:鄒宜芬/通訊地址:台北市內湖區成功路二段325號
服務單位:三軍總醫院臨床藥學部藥師/聯絡電話:(O) 02-87923311 ext 34297

