摘要
嵌合抗原接受器T細胞 (chimeric antigen receptor-T cell,CAR-T) 是T淋巴細胞 (T細胞) 透過基因工程改造以殲滅帶有可辨認的特殊標記之癌細胞,此療法結合了基因治療與免疫治療。目前已有2個 CD19 CAR-T 產品在美國上市,即 KymriahTM (tisagenlecleucel,CTL019) 用於治療兒童和年輕成人 (2-25歲) 的頑固性B細胞急性淋巴細胞白血病,以及 Yescarta (axicabtagene ciloleucel,KTE-C19) 用於治療已接受過至少2種治療方案後仍復發的成人瀰漫性大B細胞淋巴瘤患者。使用 BCMA CAR-T 治療多發性骨髓瘤具有相當潛力。CAR-T 應用在固態腫瘤 (solid tumor) 上至今仍無重大突破,其中 EGFRvIII CAR-T 治療膠質母細胞瘤和 GD2 CAR-T 治療神經母細胞瘤值得期待。使用 CAR-T 產品要小心細胞激素釋放症候群 (cytokine release syndrome) 副作用以及神經毒性,曾有致死案例發生。病人若出現任何明顯異狀,要儘早投予 tocilizumab,嚴重者需要 tocilizumab 併用類固醇。
關鍵字: 免疫治療、chimeric antigen receptor、CAR-T
壹、前言
2017年美國 FDA 核准了兩個嵌合抗原接受器T細胞 (chimeric antigen receptor-T cell,CAR-T) 產品上市:KymriahTM (tisagenlecleucel,CTL019)、Yescarta (axicabtagene ciloleucel,KTE-C19)。CAR-T 是T淋巴細胞 (T細胞) 透過基因工程改造以殲滅帶有可辨認的特殊標記之癌細胞,此療法結合了基因治療與免疫治療,是T細胞輸入療法 (adoptive T-cell therapy,ACT) 之中最常使用者。CAR-T 的發現是繼免疫檢查點抑制劑 (immune checkpoint inhibitor) 後,進一步將癌症治療帶入一個新境界。
貳、CAR-T 的強大力量
要殺死癌細胞需要依靠T細胞,尤其是細胞毒殺T細胞 (cytotoxic T cells)。當抗原呈現細胞 (antigen-presenting cells),主要是樹突細胞 (dendritic cells) 發現癌細胞時,會將癌細胞分解後當作抗原呈現給T細胞。腫瘤抗原必須先結合「主要組織相容性複合體 (major histocompatibility complex, MHC)」形成抗原-MHC 複合體後,才能與T細胞上相對應此抗原-MHC 複合體的T細胞接受器 (T cell receptor) 結合,如此T細胞才能辨認癌細胞,而將以擊殺1。
CAR-T 的優勢是它的作用和 MHC 無關,因此即使癌細胞無 MHC 表現或是 MHC 有缺陷,仍然會被 CAR-T 所攻擊,只要癌細胞上有和 CAR-T 相對應的腫瘤抗原存在即可2。CAR-T 是相當強悍的免疫“刺客”,它可以一個接著一個找出癌細胞並直接殺死,其模式就如同T細胞攻擊病毒2。
參、CAR-T 的治療過程
抽取癌症病人自身的血液,經由白血球分離機 (leukapheresis) 取得T細胞,接著送到實驗室,以無害的病毒當作載體 (vector),將一段腫瘤特定抗原的基因植入T細胞內,於是能辨識此特定標誌的 CAR-T 就產生了3。接著,擴增 CAR-T 的數量,再回輸到病人體內。為確保 CAR-T 能發揮最大功效,再回輸之前,病人要先接受高劑量化療,盡量將體內原有的淋巴細胞排空 (lymphodepletion),如此可幫助身體接受 CAR-T4。
肆、 CAR (chimeric antigen receptor) 的結構
CAR 主要包含抗原辨識和T細胞訊息傳遞兩大部分 (圖一)5。抗原辨識部分為片段抗體 (single-chain variable fragment,scFv),此抗體是針對腫瘤抗原,例如:CD19是B淋巴細胞 (B細胞) 相關白血病 (B-cell leukemia) 和淋巴瘤 (B-cell lymphoma) 表面的主要抗原,因此 CD19 CAR 結構中的 scFv 即是針對 CD19。T細胞訊息傳遞部分則可活化T細胞,以進行擊殺癌細胞。第一代 CAR 的T細胞訊息傳遞部分為 CD3ζ [CD3ζ是T細胞接受器 (T-cell receptor) 的子單元 (subunit)];第二代 CAR 為 CD3ζ加上共同刺激 (co-stimulatory) 分子 CD28或4-1 BB;第三代 CAR 為 CD3ζ同時加上 CD28與4-1 BB (圖一)5。由於共同刺激分子的加入,提升了 CAR 的增生和促進細胞激素 (cytokine) 產生,以及延長 CAR 的存活時間6。
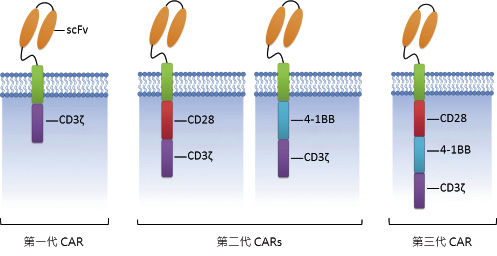
圖一 CAR (chimeric antigen receptor) 的結構5
伍、CAR-T 的臨床應用
目前 CAR-T 在血液科癌症有相當不錯的成果,尤其是B細胞衍生的白血病和淋巴瘤;至於在固態腫瘤 (solid tumor) 方面仍有待努力。
一、 B細胞急性淋巴細胞白血病 (B-cell acute lymphoblastic leukemia,B-ALL)
ALL 一旦復發,其治療困難,存活期為數週至數個月。2017年8月30日,美國 FDA 根據第2期 ELIANA 試驗結果,批准第一個 CAR-T 產品— KymriahTM (tisagenlecleucel,CTL019),用於治療兒童和年輕成人 (2-25歲) 的頑固性 B-ALL。 CTL019單次治療費用為美金475,000元 (新台幣約1400萬),一次治療即可。ELIANA 試驗結果顯示,63位病人接受一次 CTL019治療後,其中有52位在3個月內疾病達到完全緩解 (complete remission),其完全緩解率為83%。後續觀察這些治療有反應的病人,其6個月的疾病無復發率和存活率分別為75%和89%,1年的疾病無復發率和存活率分別為64%和79%7。對於頑固性 B-ALL 病人,CTL019可以提供持久有效的治療。
二、 瀰漫性大B細胞淋巴瘤 (diffuse large B-cell lymphoma,DLBCL)
DLBCL 是屬於侵襲性B細胞非何杰金氏淋巴瘤 (non-Hodgkin lymphoma,NHL),一旦復發,其預後不好;因此,臨床上十分需要新藥。依據第2期 ZUMA-1試驗結果,2017年10月18日,美國 FDA 核准 Yescarta (axicabtagene ciloleucel,KTE-C19) 上市,用於治療已接受過至少2種治療方案後仍復發的成人 DLBCL 患者。ZUMA-1結果發現,KTE-C19單次治療 DLBCL,其客觀反應率 (objective response rate,ORR) 為82%,其中完全反應率 (complete response rate) 為54%,且經15.4個月追蹤後,完全反應率仍可達40%8。KTE-C19單次治療費用為美金373,000元 (新台幣約1100萬)。已核准可用於治療 B-ALL 的 CTL019也在 DLBCL 的治療上看到不錯的效果。第2期 JULIET 研究發現,對於已接受過至少2種治療方案後仍復發的成人 DLBCL 患者,給予 CTL019單次治療,其 ORR 為53.1%,其中完全反應率為39.5%,且經6個月追蹤後,完全反應率仍可達30%9。目前美國 FDA 正在優先審查 CTL019用於治療 DLBCL 的申請書。
三、 多發性骨髓瘤 (multiple myeloma,MM)
MM 為骨髓內漿細胞 (plasma cell) 惡性增生所導致之癌症,至今仍無法治癒。B細胞成熟抗原 (B-cell maturation antigen,BCMA) 會呈現在漿細胞的表面,於是可針對 BCMA來製造CAR-T10。研究顯示,35位頑固性或復發的 MM 患者,接受 BCMA CAR-T 治療,有33位達到完全緩解,完全緩解率高達94%11,這個初步的結果仍有待後續的觀察。
四、固態腫瘤 (solid tumor)
雖然 CAR-T 治療血液科癌症有不錯的成績,但是 CAR-T 應用在固態腫瘤上至今仍無重大突破,其原因有缺乏腫瘤專一性抗原來做為 CAR-T 的標的、腫瘤微環境中許多抑制性因子使得 CAR-T 無法有效發揮作用、CAR-T 由血液運送至腫瘤處的過程受阻、腫瘤的異質性 (heterogeneity) 等4,12。目前 CAR-T 治療固態腫瘤的臨床試驗絕大部分都還處在第1期,選定的腫瘤抗原有mesothelin、HER2、EGFRvIII、GD2等,其中 EGFRvIII 是膠質母細胞瘤 (glioblastoma) 的專一性抗原、GD2會呈現於神經母細胞瘤 (neuroblastoma) 表面13。
陸、CAR-T 的安全性
CAR-T 的挑戰是如何找到腫瘤專一性抗原,使其只消滅癌細胞,而不會傷害到正常組織。某種程度上來說,CD19算是相當完美的標的,因為雖然正常B細胞上也帶有 CD19,因此 CD19 CAR-T 也會殺害正常B細胞,但是可以給予病人輸注免疫球蛋白來解決這個問題。然而,許多癌症之腫瘤抗原也多多少少會出現在正常細胞表面,因此 CAR-T的安全性是一重要的議題。
使用 CAR-T 產品要小心細胞激素釋放症候群 (cytokine release syndrome,CRS) 副作用,其症狀有發燒、發冷、極度疲倦、頭痛、噁心、呼吸喘、心跳加快、低血壓等,以及神經毒性 (neurotoxicity) 包括腦病變、譫妄、癲癇發作等,曾有致死案例發生;因此我們要提高警覺,病人若出現任何明顯異狀,要儘早投予介白素6 (interleukin-6,IL-6) 抑制劑 tocilizumab,對於已住進加護病房之嚴重等級 (≥ grade 3) 副作用者,需要 tocilizumab 併用類固醇來治療14。
柒、結論
自免疫檢查點抑制劑 ipilimumab 問市後,癌症免疫治療即進入一新紀元;其後 CD19 CAR-T 產品被核准,更將癌症治療帶入一個新境界。CAR-T 可以說是癌症免疫治療的升級版,其結合基因工程和免疫治療,被賦予使命去攻擊帶有特定標誌的癌細胞。目前已有2個 CD19 CAR-T 產品在美國上市,雖然療效顯著,但是其價格相當昂貴,將會衝擊到臨床使用。另方面來說,CAR-T 大致上是安全的,但仍有可能發生嚴重 CRS 以及神經毒性,甚至致命,因此使用上需要提高警覺。
CAR T-Cell Therapy: Both Gene Therapy and Immunotherapy
Chi-Yuan Cheng1, Yi-Cheng Chen1, Tzu-Cheng Tsai1, Wen-Cheng Chang2
Department of Pharmacy, Chang Gung Memorial Hospital, Linkou1
Department of Oncology, Chang Gung Memorial Hospital, Linkou2
Abstract
CAR (chimeric antigen receptor) T cells are T lymphocytes (T cells) that genetically engineered to destroy cancer cells with the recognizable specific marker. CAR T-cell therapy is both a gene therapy and an immunotherapy. Currently, there are two CD19 CAR-T products available in the United States, namely KymriahTM (tisagenlecleucel, CTL019) for the treatment of patients of age 2-25 years with refractory B-cell acute lymphoblastic leukemia, and Yescarta (axicabtagene ciloleucel, KTE-C19) for the treatment of adult patients with relapsed or refractory diffuse large B-cell lymphoma after two or more lines of systemic therapy. BCMA CAR-T seems to be a potential one to treat multiple myeloma. The application of CAR-T for solid tumors has no major findings until now, of which EGFRvIII-CAR T therapy for glioblastoma and GD2-CAR T therapy for neuroblastoma are worth expecting. CAR T-cell therapy products may cause cytokine release syndrome and neurotoxicity, and even fatal. For patients with any obvious abnormalities, tocilizumab should promptly administered, and severe cases require tocilizumab plus corticosteroids.
參考資料:
1.Murphy K: Janeway's Immunobiology, 8th ed. New York. Garland Science, 2012:202-3.
2. 鄭吉元、蔡慈貞、張文震,癌症免疫治療:癌症治療新紀元. 藥學雜誌 2017;33:35-9.
3. Levine BL, Miskin J, Wonnacott K, et al: Global manufacturing of CAR T cell therapy. Mol Ther Methods Clin Dev 2016;4:92-101.
4. Srivastava S, Riddell SR: Chimeric antigen receptor T Cell therapy: challenges to bench-to-bedside efficacy. J Immunol 2018;200:459-68.
5. Brudno JN, Kochenderfer JN: Chimeric antigen receptor T-cell therapies for lymphoma. Nat Rev Clin Oncol 2018;15:31-46.
6. Casucci M, Bondanza A: Suicide gene therapy to increase the safety of chimeric antigen receptor-redirected T lymphocytes. J Cancer 2011;2:378-82.
7. Pulsipher M, Buechner J, Grupp SA, et al: Global registration trial of efficacy and safety of CTL019 in pediatric and young adult patients with relapsed/refractory (R/R) acute lymphoblastic leukemia (ALL): update to the interim analysis. Presented at 2017 SOHO Annual Meeting. Abstract ALL-152.
8. Neelapu SS, Locke FL, Bartlett NL, et al: Axicabtagene ciloleucel CAR T-cell therapy in refractory large B-cell lymphoma. N Engl J Med 2017;377:2531-44.
9. Schuster SJ, Bishop MR, Tam CS, et al: Primary analysis of JULIET: a global, pivotal, Phase 2 trial of CTL019 in adult patients with relapsed or refractory diffuse large B-cell lymphoma. Presented at 59th American Society of Hematology Annual Meeting and Exposition. Abstract 577.
10. Mikkilineni L, Kochenderfer JN: Chimeric antigen receptor T-cell therapies for multiple myeloma. Blood 2017;130:2594-602.
11. Fan F, Zhao W, Liu J, et al: Durable remissions with BCMA-specific chimeric antigen receptor (CAR)-modified T cells in patients with refractory/relapsed multiple myeloma. Presented at 2017 ASCO Annual Meeting. Abstract LBA3001.
12. Wang Y, Luo F, Yang J, et al: New chimeric antigen receptor design for solid tumors. Front Immunol 2017;8:Article 1934.
13. Mirzaei HR, Rodriguez A, Shepphird J, et al: Chimeric antigen receptors T cell therapy in solid tumor: challenges and clinical applications. Front Immunol 2017;8:Article 1850.
14. Neelapu SS, Tummala S, Kebriaei P, et al: Chimeric antigen receptor T-cell therapy - assessment and management of toxicities. Nat Rev Clin Oncol 2018;15:47-62.
通訊作者:鄭吉元/通訊地址:桃園市龜山區復興街5號
服務單位:林口長庚紀念醫院藥劑部藥師/聯絡電話:(O) 03-3281200 ext 2915

