摘要
類風濕性關節炎是一種全身性自體免疫疾病,臨床上以多個關節滑膜組織慢性發炎和關節破壞為主要特徵。類風濕性關節炎常發生在正值生育年齡的婦女,為了控制疾病進展並預防進一步的關節或器官損傷,常需要長期使用免疫抑制治療。臨床上,在懷孕時期仍需要使用藥物治療。主要的治療藥物如:methotrexate,卻不建議使用在妊娠哺乳期間。抗腫瘤壞死因子 (tumour necrosis factor inhibitors, TNFi) 生物製劑是目前被認為可作為妊娠期間,活動性類風濕性關節炎的替代治療選擇。但是,相關生物製劑臨床經驗太有限,安全性資料不夠令人信服。Certolizumab pegol (簡稱 CZP,商品名為 Cimzia) 是抗腫瘤壞死因子生物製劑,結構特殊僅含有 PEGylation 之 Fab' 部位,並缺乏 Fc 部位,理論上不會穿過胎盤進入胎兒。本文以現有文獻回顧探討 CZP,在懷孕及授乳的類風濕性關節炎病人使用的安全性。最終結論建議懷孕或哺乳的類風濕性關節炎病人可以考量 CZP 作為治療選擇之一。
關鍵字: 類風濕性關節炎、懷孕、Certolizumab pegol、CZP、tumour necrosis factor inhibitors
壹、前言
類風濕性關節炎 (rheumatoid arthritis, RA) 是以多個關節滑膜組織慢性發炎和關節破壞為主要特徵的自體免疫疾病1,2。RA常發生於正值生育年齡的婦女。由於懷孕期間的治療同時影響到母親和未出世的孩子,因此,罹患 RA 的孕婦治療時,通常會以對孕婦安全的藥物,作為第一選擇考量2。近幾年已經證實抗腫瘤壞死因子 (tumour necrosis factor inhibitors, TNFi) 的生物製劑,可以有效治療 RA,降低關節破壞的速度、改善身體機能及增進生活品質。TNFi 生物製劑是 IgG 單株抗體的衍生物,可阻斷腫瘤壞死因子細胞激素的作用3,個別結構差異造成半衰期長短及穿過胎盤能力不同。TNFi 是妊娠期間生物製劑選擇治療選項之一4,5,同時歐洲風濕疾病聯盟 (European League Against Rheumatism , EULAR) 建議可作為妊娠期間活動性類風濕性關節炎的替代治療選擇3。但是,相關生物製劑臨床經驗太有限,安全性資料不夠令人信服。Certolizumab pegol (簡稱 CZP) 僅含有 PEGylation 之 Fab' 部位,缺乏 Fc 部位,理論上不會在第二、第三孕期穿過胎盤進入胎兒6。臨床上使用可作為單一療法,也可併用非生物製劑之疾病調節抗風濕藥物 (disease modifying anti-rheumatic drug, DMARD) 治療7。
治療 RA 的藥物於懷孕及哺乳期間需小心使用,有些藥品於妊娠哺乳期間不建議使用(表一)1,3。本文介紹 CZP 並回顧相關文獻,探討使用 CZP 在懷孕及授乳的 RA 病人的安全性。
表一 NSAIDs 與免疫抑制劑用於孕哺婦之專家意見與共識1,3

貳、Certolizumab pegol 藥物介紹
一、適應症
(一)類風濕性關節炎
治療對至少一種 DMARD 無適當療效之成人中至重度活動性 RA。CZP 和 methotrexate 併用時,證實可減緩X光檢測下關節傷害的惡化速度。
(二)僵直性脊椎炎
用於曾對非類固醇抗發炎藥物 (NSAIDs) 反應不佳或耐受性不良的重度活動性僵直性脊椎炎成人患者。
(三)乾癬性關節炎
用於曾對 DMARD 療法反應不佳的成人患者8。
二、作用機轉
TNF-α 是誘發發炎反應的重要細胞激素之一,能抑制 RA、僵直性脊椎炎、乾癬及乾癬性關節炎等自體免疫病人過度分泌的腫瘤壞死因子,可以抗發炎及免疫調節,進而達到抑制關節發炎的效果。CZP 是由大腸桿菌基因重組之人源化抗體 Fab'片段,純化後與聚乙二醇 (polyethylene glycol, PEG) 共軛結合形成複合物,稱為 PEGylation 抗體,PEG 化修飾的抗體可以進一步延長半衰期。有別於其它 TNFi 生物製劑,CZP 僅含有抗體之 Fab' 部位,因缺乏 Fc 部位 (圖一),故不會活化補體。同時因缺乏 Fc 部位,無法與新生兒 Fc 受體 (FcRn) 結合,不會在第二、第三孕期從母體經胎盤進入胎兒2,7-9。
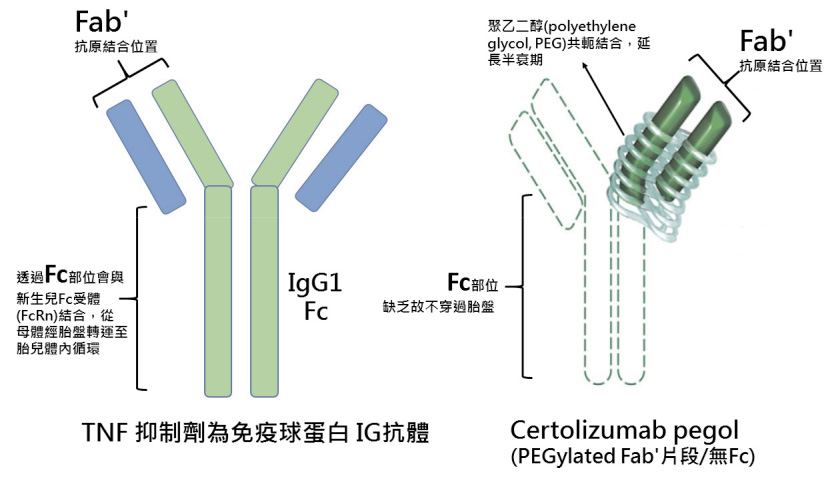
圖一 Certolizumab pegol 結構示意圖6
三、建議劑量
CZP 是針筒預充填式注射用溶液,一支內含200 毫克。用於 RA 治療之起始劑量為:初始400毫克,在第二週與第四週各給予400毫克7。維持劑量為每二週注射一劑200毫克,或每四週打400毫克,方便病人回診再施打,不需帶藥回家保存,提高病人遵醫囑性。腎及肝功能不全病人,尚無此族群使用的研究,現有資料不足無法提供劑量建議。大於65歲患者的老年族群劑量不須調整8。
四、給藥途徑
CZP 需皮下注射給藥,當需要施打400毫克劑量時,應進行兩次200毫克皮下注射,注射部位必須輪替,須避開僵硬、皮膚脆弱、瘀血或發紅部位8。
五、藥物動力學
CZP 血漿濃度與劑量成比例。穩定態之分佈體積為6-8公升。在皮下給藥注射後54-171小時,CZP 達到最高血中濃度。與靜脈注射相比,皮下注射之生體可用率約為80%(76-88%)。CZP 為 PEGylation 之 Fab' 片段抗體,PEG 化修飾的抗體可以延長半衰期,最終排除相的半衰期 (t1/2) 約為14天7,8。
六、禁忌症
禁用於對成份過敏、活動性肺結核或其他嚴重感染如:敗血症、膿瘍或伺機性感染及中度或重度心衰竭 (NYHA classes III/IV)8。
七、注意事項
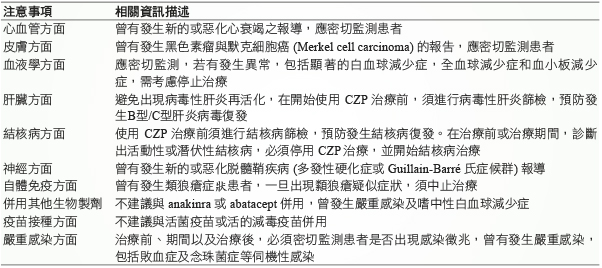
應保存於外紙盒避光,儲存於2-8°C冷藏,不可冷凍。不可與其他藥品混合使用。CZP 可能導致病人免疫力降低,造成增加感染的風險、病毒性肝炎再活化或使帶有結核桿菌者的結核病發作。其他相關注意事項 (表二)7,8。
表二 Certolizumab pegol 使用注意事項7,8
八、健保給付規範
我國健保於106年11月1日起給付 CZP,也是目前免疫製劑健保給付規範中,唯一未將懷孕及授乳病人列入使用禁忌,可健保給付用於懷孕及授乳的 RA 病人之藥物。因此,如果懷孕或哺乳中仍須使用生物製劑,可以考量 CZP 作為治療選擇。雖然 CZP 的適應症有 RA、僵直性脊椎炎及乾癬性關節炎,但目前健保僅在 RA 通過給付,至於僵直性脊椎炎及乾癬性關節炎病人,則仍需自費使用。
參、 Certolizumab pegol 臨床療效與副作用探討
2017年,考科藍發表一篇系統性回顧文獻,探討 CZP 對成人活動性類風濕性關節炎療效與副作用風險。文獻搜尋截至2016年9月,共收錄14個隨機對照試驗,5499位受試者,大多數受試者為女性。分析5個試驗 (1445位受試者) 發現,接受隔週 CZP 200毫克的病人6個月後 ACR 50(註一) 有明顯改善 (RR = 3.80,95%CI = 2.42-5.95,I2 = 56%),需要被治療人數為4(NNTB = 4,95% CI = 3-5),100個使用過 CZP 的病人中,25個覺得改善程度有超過50%(絕對風險差 = 25%,95%CI = 20%-33%)。嚴重不良事件被定義為惡性腫瘤和所有感染,尤其是結核病與死亡。分析9個試驗 (3927位受試者) 的嚴重不良事件發生率,追蹤期達12-24週,在100位使用 CZP 的病人中有9人出現,而使用安慰劑的100位患者中有6人出現 (3%絕對傷害,95%CI= 1%-4%,NNTH = 33)10。
在2016年於 Lancet 發表的 EXXELERATE 試驗,直接比較一種 TNFi 失敗後,更換為另一種 TNFi 的臨床療效和安全性。結果顯示,即使在第12週時治療療效不佳,將 CZP 組與 adalimumab 組藥品互換,在互換的第12週後仍有近6成病人有療效,CZP 組與 adalimumab 組的療效相當11。
註一:ACR 是美國風濕病學院所訂定的 RA 症狀變化量表,ACR 50相當於病人腫脹關節數、觸痛關節數、疼痛、失能指數、發炎指數C反應蛋白、醫師的綜合評估及患者對活動能力的自我評估等有50%改善。
肆、 Certolizumab pegol 懷孕及哺乳安全性探討
一、懷孕安全性探討
自體免疫疾病如 RA,常需要長期藥物治療,而 RA 對多數女性病人而言,儘管妊娠期間通常疾病活動性有所改善,但仍有一定數量的 RA 病人在妊娠期間仍需要藥物治療。TNFi 生物製劑是目前認為妊娠期間的活動性 RA 的替代治療選擇。在妊娠前三個月使用需注意 TNFi 是否會增加流產或畸形的風險。歐洲風濕疾病聯盟 (EULAR) 系統性文獻回顧了曾使用 TNFi 的2492例懷孕婦女,探討使用 TNFi 是否會增加流產或畸形的風險,結果顯示使用 TNFi 的孕婦之流產率或先天性畸形沒有增加。其中有362例使用 CZP 的懷孕婦女,與未用藥組相比,沒有增加流產或畸形的風險3。
在第二、第三孕期使用藥物治療,需要考慮藥物通過胎盤的可能性。因為在第二、第三孕期,TNFi (IgG 單株抗體) 藥物的 Fc 部位會與新生兒 Fc 受體 (FcRn) 結合,從母體經胎盤主動轉運至胎兒體內循環。TNFi 中的 infliximab 為嵌合的人類-小鼠單株抗體,曾被報導會穿過胎盤。文獻指出懷孕期間接受 infliximab 治療的女性,於出生後達6個月的新生兒血清中還能檢驗到 infliximab2。但是 CZP 之結構僅含有 IgG 抗體之 Fab' 部位,因缺乏 Fc 部位,故理論上不會穿過胎盤。
一項前瞻性、多中心臨床試驗,於2014年1月至2016年11月在法國、荷蘭、瑞士和美國的11個中心進行,包含16 位懷孕超過30週女性連續接受 CZP,其中15位的維持劑量施打方式為每2 週一次200毫克,另一位使用維持劑量每4週一次400毫克治療,最後一劑 CZP 是在生產分娩前平均11天 (介於1-27天) 給藥。檢定法所能測得 CZP 最低定量極限濃度為0.032μg/mL。結果發現產婦分娩時的 CZP 血漿濃度為24.4μg/mL (4.96-49.4μg/mL),與非懷孕女性所觀察到的血漿濃度一致。在取得之14位嬰兒出生血液檢體中,有13 位嬰兒檢體出生時測得之 CZP 藥物濃度低於定量極限;另一份檢體之出生濃度為0.042μg/mL,且嬰兒/母體血漿濃度比為0.0009。所有嬰兒於第4週及第8 週時藥物濃度均低於定量極限。此研究證實在第三孕期懷孕女性使用 CZP,藥物不會或極微量從胎盤轉移至新生兒體內8。
日本曾報導 CZP 用於一例孕婦,從懷孕28週至40週時生產,一直使用至生產後8週,使用期間母體都能測到血漿濃度 (22-40μg/mL),除了疾病嚴重度有獲得改善,使用藥物期間乳汁檢體之藥物濃度均低於定量極限。新生兒出生後的第3天,血液檢體藥物濃度均低於定量極限,同時沒有報導對新生兒產生任何不良影響12。
二、哺乳安全性探討
母乳可傳遞多種免疫球蛋白和抗發炎因子,以保護嬰兒對抗疾病。儘管母乳哺育對於兒童健康和發育極為重要,但 RA 病人尚須考量藥物是否分泌至乳汁,是否會隨著乳汁進入嬰兒體內而帶來風險。目前,生物製劑分泌至乳汁相關的藥物動力學發表資訊不足,常常造成產婦與醫師選擇用藥與是否哺育母乳兩難的困境。
一項前瞻性、上市後在美國及歐洲進行的多中心臨床試驗,包含17 位生產完並已連續接受至少3劑 CZP 的哺乳女性。在137份母乳檢體中,有77份 (56%) 之 CZP 濃度低於定量極限 (< 0.032μg/mL),其它的乳汁藥物濃度介於定量極限與0.0758μg/mL 之間。在任何時間點於乳汁測得之最高濃度,均小於1%的成人接受維持治療劑量之平均預期血漿濃度。該實驗結果顯示,CZP 藥物轉移至乳汁濃度幾乎無或微量。哺乳嬰兒之全身接觸量偏低,加上 CZP 為蛋白質,僅含有抗體之 Fab' 部位,缺乏 Fc 部位,即使透過乳汁經口攝入後,也會在腸胃道內分解,生體可用率極低,該研究結果支持母乳哺育期間繼續 CZP 治療13。
伍、總結
目前實證資料顯示,當第一種 TNF inhibitor 失敗後,在互換的第12週後仍有近6成病人有療效,CZP 組與 adalimumab 組兩種治療方式互換的臨床療效和安全性相當11。因 CZP 胎盤轉移性低,歐洲抗風濕病協會提出,如懷孕中仍須使用,CZP 可作為治療選擇之一3。國內健保於106年11月1日起,給付 CZP 使用於 RA,懷孕及授乳的 RA 病人仍可繼續使用,不需停藥。RA 病人若想懷孕,需與醫師討論調整藥物治療。懷孕期間疾病控制得當,將有助於平安生育。藥師也應該發揮專業角色,提供相關安全性資料,幫助醫師及病人選擇適當藥物。
New Choice of Treatment for RA Patients During Pregnancy and Lactation
Chia-Ling Yu1, Li-Huei Chiang1, Wei-Min Cho2, Tzu-Cheng Tsai1
Department of Pharmacy, Chang-Gung Memorial Hospital, Linkou1
Department of Pharmaceutical Materials Management,
Chang-Gung Memorial Hospital, Taoyuan2
Abstract
Rheumatoid arthritis is a systemic autoimmune disease characterized by chronic inflammation of synovial and multiple joints destruction. Rheumatoid arthritis often affects childbearing age women. To keep disease activity under control and prevent joint or organ damage, long-term immunosuppressive therapy is required in these patients. There is a need for adequate disease control during pregnancy. MTX is teratogenic and should be avoided during pregnancy and lactation. Tumour necrosis factor inhibitors (TNFi) are considered compatible with use during pregnancy. However, the clinical experience of biological agents is too limited to have safety for pregnancy and lactation. Certolizumab pegol is a pegylated Fc-free anti-TNF drug. Certolizumab pegol prevents to transfer across the placenta, because there is lack of the Fc fragment. This review considers certolizumab pegol treatment is safe for pregnancy and breast-feeding women. All these results support continuation of certolizumab pegol treatment for RA patients during pregnancy and breast feeding.
參考資料:
1.De Jong PH, Dolhain RJ. Fertility, pregnancy, and lactation in rheumatoid arthritis. Rheumatic Disease Clinics of North America.2017; 43(2):227-237.
2. Förger F. Treatment with biologics during pregnancy in patients with rheumatic diseases. Reumatologia. 2017; 55(2):57-58.
3. Gotestam Skorpen C, Hoeltzenbein M, Tincani A, et al: The EULAR points to consider for use of antirheumatic drugs before pregnancy, and during pregnancy and lactation. Ann Rheum Dis. 2016; 75:795–810.
4. Narula N, Al-Dabbagh R, Dhillon A, et al: Anti-TNFα therapies are safe during pregnancy in women with inflammatory bowel disease: a systematic review and meta-analysis. Inflamm Bowel Dis. 2014; 20(10):1862-9.
5. Shihab Z, Yeomans ND, De Cruz P. Anti-Tumour Necrosis Factor α Therapies and Inflammatory Bowel Disease Pregnancy Outcomes: A Meta-analysis. J Crohns Colitis 2016; 10:979-88.
6. Porter C, Armstrong-Fisher S, Kopotsha T, et al: Certolizumab pegol does not bind the neonatal Fc receptor (FcRn): consequences for FcRn-mediated in vitro transcytosis and ex vivo human placental transfer. J Reprod Immunol 2016; 116:7-12.
7. Fechtenbaum M, Md Yusof MY, Emery P. Certolizumab pegol in rheumatoid arthritis: current update. Expert Opin Biol Ther. 2014 ;14(6):841-50.
8. Product Information: Cimzia(R), Certolizumab pegol solution for injection. UCB Pharma S.A, 2017.
9. Mariette X, Förger F, Abraham B, et al: Lack of placental transfer of certolizumab pegol during pregnancy: results from CRIB, a prospective, postmarketing, pharmacokinetic study. Ann Rheum Dis 2018; 77 (2): 228-233.
10. Ruiz Garcia V, Burls A, Cabello JB, et al: Certolizumab pegol (CDP870) for rheumatoid arthritis in adults. Cochrane Database Syst Rev. 2017; 9: CD007649.
11. Smolen JS, Burmester GR, Combe B, et al: Head-to-head comparison of certolizumab pegol versus adalimumab in rheumatoid arthritis: 2-year efficacy and safety results from the randomised EXXELERATE study. Lancet 2016; 388: 2763-74.
12. Morita T, Fujimoto K, Shima Y, et al: Minimal neonatal transfer of certolizumab pegol in a Japanese patient with rheumatoid arthritis.Ann Rheum Dis Published Online First: doi:10.1136/annrheumdis-2017-212366.
13. Clowse ME, Förger F, Hwang C, et al: Minimal to no transfer of certolizumab pegol into breast milk: results from CRADLE, a prospective, postmarketing, multicentre, pharmacokinetic study. Ann Rheum Dis. 2017;76:1890-1896.
通訊作者:游佳玲/通訊地址:桃園市龜山區復興街5號
服務單位:林口長庚紀念醫院藥劑部藥師/聯絡電話:(O) 03-3281200 ext 3730

