摘要
滅菌生理食鹽水為常見的傷口護理用品之一,其藥品分級的類別多為指示藥或醫療器材,少數為處方藥,多數藥局皆有提供滅菌生理食鹽水。然而,部份滅菌生理食鹽水的仿單與包裝,未明確標示開封後的使用期限 (Beyond-use date, BUD),且藥局對此也無一致的說法,使民眾無法獲得正確的資訊。
本調查透過實地訪問與歸納台中市與彰化縣共100間藥局對滅菌生理食鹽水開封後使用期限之認知,對照其與美國藥典以及本次調查中的滅菌生理食鹽水之仿單及包裝標示並討論,期望藥局能建構與提供正確的說法,使民眾能在正確的使用期限內使用滅菌生理食鹽水,減低傷口感染與惡化的風險。
關鍵字:滅菌生理食鹽水、開封後使用期限、sterile normal saline solution、beyond-use date
壹、前言
滅菌生理食鹽水為常見的傷口護理用品之一,其主要功能為沖洗傷口以維護傷口之清潔。本調查之滅菌生理食鹽水的成分為0.9%氯化鈉水溶液,且不含防腐劑及其他成分。使用期限 (Beyond-use date, BUD) 的定義1:無菌調製的製劑 (Compounded sterile preparation, CSP),經施用後不能再次使用的日期或時間,而安定性與儲存環境為無菌調製製劑受汙染風險的重要影響因素。本調查之目的為透過實地訪問藥局,針對有關滅菌生理食鹽水使用期限之說法進行歸納,並討論其認知是否能提供民眾正確的滅菌生理食鹽水使用期限,以減少滅菌生理食鹽水開封後受到汙染的可能性,進而降低傷口感染的風險。
貳、調查方法
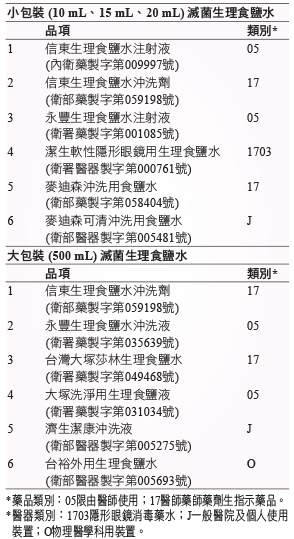
一、調查方式:實地訪問。二、調查時間:自107年7月9日至107年8月20日。三、調查地點:台中市與彰化縣共100間藥局 (附件)。四、受訪對象:藥師、藥局員工,共100人。五、調查事項:藥局對小包裝及大包裝滅菌生理食鹽水開封後儲存與使用期限之認知。六、提問題目:(一)藥局提供滅菌生理食鹽水的品項。(二)若用於沖洗傷口,各品項滅菌生理食鹽水,開封後的使用期限有多久。七、本調查之小包裝及大包裝滅菌生理食鹽水的成分為0.9%的氯化鈉水溶液,且不含防腐劑及其他成分,品項 (表一)。
附件 受訪藥局清冊

表一 藥局提供滅菌生理食鹽水之品項
參、調查結果
實地訪問100間藥局,其中82間藥局有提供小包裝滅菌生理食鹽水,這82間藥局對於「室溫儲存之小包裝滅菌生理食鹽水,開封後使用期限」的認知,有54間藥局認為開封後需一次用完,7間藥局認為開封後可儲存1天,4間藥局認為開封後可儲存2至3天,2間藥局認為開封後可儲存1周至未滿1個月,5間藥局認為開封後至標籤上的有效期限仍可使用,10間藥局認為開封後應盡快用完。調查結果之統計圖 (圖一)。
實地訪問100間藥局,皆有提供大包裝滅菌生理食鹽水,這100間藥局對於「室溫儲存之大包裝滅菌生理食鹽水,開封後使用期限」的認知,有1間藥局認為開封後可儲存1天,5間藥局認為開封後可儲存2至3天,15間藥局認為開封後可儲存1周至未滿1個月,30間藥局認為開封後可儲存1個月,21間藥局認為開封後可儲存超過1個月,14間藥局認為開封後至標籤上的有效期限仍可使用,14間藥局認為開封後應盡快用完。調查結果之統計圖 (圖二)。
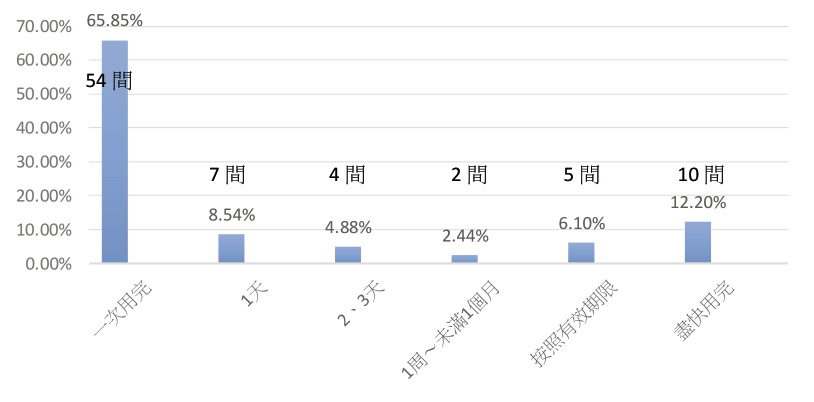
圖一 藥局對室溫儲存之小包裝滅菌生理食鹽水,開封後使用期限的認知
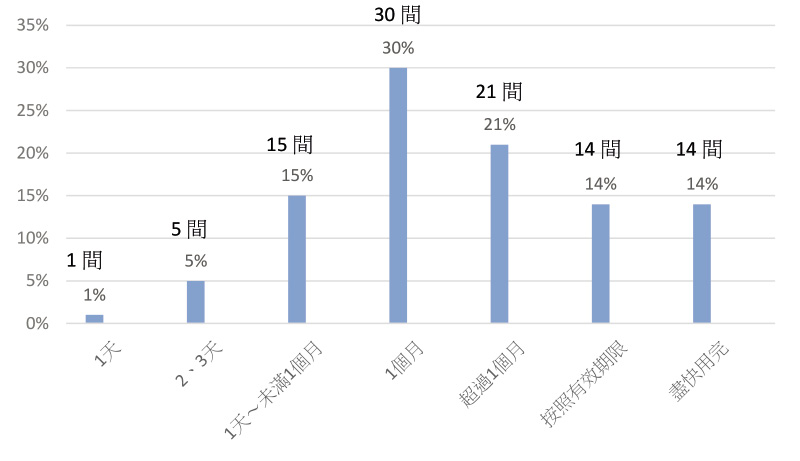
圖二 藥局對室溫儲存之大包裝滅菌生理食鹽水,開封後使用期限的認知
肆、討論
滅菌生理食鹽水為沖洗傷口常用的護理用品,其無菌狀態對傷口護理的重要性不容忽視。滅菌生理食鹽水開封後,屬於非無菌狀態 (non-sterile condition),因此,開封後在正確的使用期限內使用,才能減低傷口感染的風險。
根據美國藥典 (United States Pharmacopeia,USP)<797>2對調製無菌製劑的微生物汙染風險分類 (Compounded sterile preparations microbial contamination risk levels),藥局或民眾居家等環境,無法達到 ISO Class5的空氣品質,滅菌生理食鹽水開封後處於高風險環境,因此,滅菌生理食鹽水開封後屬於高汙染風險的無菌製劑 (High-Risk Level CSPs),所以,在沒有通過無菌試驗的情況下,於控制室溫,應妥善儲存且暴露時間不超過24小時。此外,本調查之滅菌生理食鹽水為小包裝之單劑量安瓿瓶及大包裝之塑膠瓶,根據美國藥典<797> (附件)3,「未達到 ISO Class5的空氣品質時,可密閉的容器在開封後之使用期限,建議不超過1小時」,「單劑量包裝的安瓿瓶,開瓶後未用完之殘量應丟棄」。
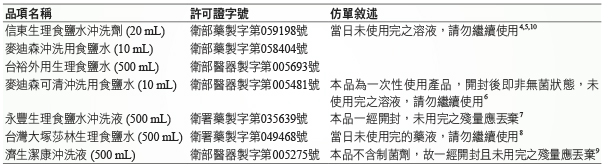
本次調查中的12項滅菌生理食鹽水仿單與包裝中,有7個品項 (58.3%) 明確標示開封後的使用期限 (表二):
表二 本次調查中,仿單與包裝具明確標示開封後使用期限的滅菌生理食鹽水
根據此次調查結果,發現藥局對滅菌生理食鹽水開封後之使用期限無一致說法,對於小包裝的使用期限,多數藥局認為其開封後無蓋子供密閉,故應1次用完 (82間藥局有54間,佔65.85%(圖一),此說法與美國藥典和本次調查中的品項之仿單及包裝標示的使用期限較為相近;而藥局對大包裝的使用期限,則是認為其開封後有蓋子可供密閉,100間藥局有86間藥局明確表示使用期限,其中85間表示使用期限超過1天,(86間藥局中有85間,佔98.84%(圖二),然而,此說法與美國藥典和本次調查中的品項之仿單及包裝標示的使用期限仍有相當程度的落差。對照美國藥典<797>2對「高風險無菌製劑建議不超過24小時的暴露時間」,與美國藥典<797> (附件)3,對「單劑量可密閉的容器在開封後之使用期限,建議不超過1小時」,以及 (表二) 仿單及包裝標示「一次性使用」或「當日使用」的使用期限,本次接受調查的全部藥局,皆未明確告知民眾滅菌生理食鹽水開封後之非無菌狀態對於傷口感染風險之影響,亦未提供民眾正確的開封後使用期限與儲存方法的概念。
伍、結論
滅菌生理食鹽水為沖洗傷口的藥品或醫療器材,依美國藥典對調製無菌製劑的風險分類2,滅菌生理食鹽水開封後屬於高汙染風險的無菌製劑,因此,在沒有通過無菌試驗的情況下,於控制室溫,應妥善儲存且暴露時間不超過24小時。若以美國藥典<797> (附件)3,對不同容器無菌調製製劑之使用期限分類,「未達到 ISO Class5的空氣品質時,可密閉的容器在開封後之使用期限,建議不超過1小時」,「單劑量包裝的安瓿瓶,開瓶後未用完之殘量應丟棄」。此次對100間藥局之調查結果發現,藥局對滅菌生理食鹽水開封後的使用期限尚未建立共識,因此,期望藥局能建構與提供正確的說法,使民眾能在正確的使用期限內使用滅菌生理食鹽水,減低傷口感染與惡化的風險。
Pharmacies’ Statements about the Beyond-use Date of the Sterile Normal Saline Solution
Xin-Yi Wu1, Kai-Yu Chang1, Chien-Chiang Chiu2, Hung-Yu Huang2, Wen-You Liao2
Department of Pharmacy, China Medical University1
Jiu-Yu Drugstore & Company2
Abstract
Sterile normal saline solution is one of the common wound management materials. It is classified into three categories, including prescription drugs, instruction drugs, and medical devices. As a result, it is often purchased in the pharmacies. However, most package inserts of them are not marked clearly about the beyond-use date (BUD). Furthermore, there are no consistent statements declared by the pharmacists. Consequently, people may not get the right information about the beyond-use date of the sterile normal saline solution.
This investigation was progressed by field research, and the respondents were pharmacists and staffs of the one hundred pharmacies in the Taichung City and Changhua County. By means of comparing statements about the beyond-use date of the sterile normal saline solution declared by pharmacists with the United States Pharmacopeia (USP), establishing and providing standard information about the beyond-use date of the sterile normal saline solution is suggested to pharmacists in order to decrease the risk of wound infection.
參考資料:
1. American Society of Health-System Pharmacists. Drug Distribution and Control: Preparation and Handling–Guidelines; p. 117.
https://www.ashp.org/-/media/assets/policy-guidelines/docs/guidelines/compounding-sterile-preparations.ashx
2. 2012 U.S. Pharmacopeia-National Formulary [USP 35 NF 30]. Rockville, Md: United States Pharmacopeial Convention, Inc; 2012. [797] Pharmaceutical Compounding— Sterile Preparations; p. 6.
https://www.snmmi.org/files/docs/USP%20797.pdf
3. 2012 U.S. Pharmacopeia-National Formulary [USP 35 NF 30]. Rockville, Md: United States Pharmacopeial Convention, Inc; 2012. [797] Pharmaceutical Compounding— Sterile Preparations; p. 28.
https://www.snmmi.org/files/docs/USP%20797.pdf
4. Taiwan Biotech Company, LTD. Package inserts of Normal Saline Solution (MHW Medicine Manufacturing No.059198). Taiwan, 2017. 1p
5. Aseptic Innovative Medicine Co., LTD. Package inserts of Normal Saline Solution(MHW Medicine Manufacturing No. 058404). Taiwan, 2017. 1p
6. Aseptic Innovative Medicine Co., LTD. Package inserts of Clean Saline Solution(MHW Medical Device Manufacturing No. 005481). Taiwan, 2016. 1p
7. Y F CHEMICAL CORP. Package inserts of N.S. IRRIGATION (DOH Manufacturing No. 035639). Taiwan, 2016. 6p
8. Taiwan Otsuka Pharmaceutical Co., Ltd. Package inserts of Normal saline solution(DOH Manufacturing No. 049468). Taiwan, 2018. 1p
9. Chi Sheng Pharma & Biotech Co., Ltd. Package inserts of Jacon Cleaning Solution(MHW Medical Device Manufacturing No. 005275). Taiwan, 2018. 3p
10. Tai Yu Chemical & Pharmaceutical Co., Ltd. Package inserts of Topical Saline Solution(MHW Medical Device Manufacturing No. 005693). Taiwan, 2017. 1p
通訊作者:邱建強/通訊地址:台中市太平區樹孝路45號
服務單位:玖裕藥局藥師/連絡電話:(O) 04-23917005

