摘要
近幾年癌症免疫療法的快速發展為癌症治療開啟新頁,其中最受矚目且應用最廣的莫過於免疫檢查點抑制劑 (immune checkpoint inhibitor,ICPi),包括 CTLA-4與 PD-1/PD-L1抑制劑。此類藥物透過調控人體既有的免疫機制來達到毒殺癌細胞之效果,目前臨床上已用於治療黑色素瘤、肺癌、腎細胞癌、淋巴癌、胃癌、肝癌、大腸直腸癌與泌尿道癌等疾病。對於進展快速且難以治癒之癌症如黑色素瘤,部分病人使用免疫檢查點抑制劑後能產生明顯而且持久的療效,醫界因此大受鼓舞,紛紛投入相關研究與產品開發。然而,新藥物也與以往使用化療藥物發生迥異的免疫相關副作用 (immune-related adverse event,irAE),雖然大部分的 irAE 都是可恢復的,但仍有少數病人會引起嚴重的 irAE 甚至導致死亡,因此及早辨識與適當處置 irAE 是一門相當重要的課題。本文將探討 ICPi 常見或重要的 irAE,以及在發生 irAE 時如何處理。
關鍵字:免疫檢查點抑制劑、免疫相關副作用、immune checkpoint inhibitor (ICPi)、immune-related adverse event (irAE)
壹、前言
目前核准用於治療癌症的免疫檢查點抑制劑 (immune checkpoint inhibitor,ICPi) 有三類機轉:拮抗第四類細胞毒殺T細胞抗原 (cytotoxic T lymphocyte antigen-4,CTLA-4) 的藥物如 ipilimumab,第一類程序性細胞死亡蛋白質 (programmed cell death-1,PD-1) 抑制劑如 nivolumab、pembrolizumab 和其配體 (PD-1 ligand,PD-L1) 抑制劑如 atezolizumab、avelumab 與 durvalumab (表一)1。由於 ICPi 的作用機轉是活化體內免疫反應,因此其副作用可能會影響全身的器官,統稱為「免疫相關副作用」(immune-related adverse event,irAE)2。
貳、ICPi 常見或重要之 irAE
使用 CTLA-4抑制劑的病人發生 irAE 的機率有90%;而 PD-1/PD-L1抑制劑發生 irAE 的機率則有70%。大部分的 irAE 發生於起始治療後的3-6個月內,但也有在治療停止1年後才發生 irAE 的記錄3。併用 CTLA-4與 PD-1/PD-L1抑制劑會增加 irAE 發生率與嚴重程度。依發生部位整理如下:
表一 已核准使用之 ICPi1

一、皮膚或黏膜相關
使用 CTLA-4或 PD-1/PD-L1抑制劑治療黑色素細胞瘤 (melanoma) 病人常可見白斑 (vitiligo) 產生,其他較常見副作用為皮疹或紅斑。史蒂芬氏-強森症候群 (Stevens-Johnson syndrome,SJS) 與毒性表皮溶解症 (toxic epidermal necrolysis, TEN) 也曾有案例報告4。大約有5%病人可能有口乾等類似修格蘭氏症候群 (Sjogren's syndrome) 症狀產生3。
二、胃腸道相關
腹瀉是 ICPi 引起最常見胃腸道相關的 irAE,約三成接受 CTLA-4抑制劑治療病人可能產生腹瀉的副作用,其發生率比 PD-1/PD-L1抑制劑高3。CTLA-4抑制劑引起的結腸炎臨床症狀與克隆氏症 (Crohn's disease) 相似,由結腸鏡檢可發現紅斑與潰瘍,組織學檢測也可見淋巴細胞與嗜中性白血球浸潤引起的發炎反應或膿腫3。嚴重腹瀉可能發生腸穿孔導致病人死亡,因此,中度以上的腹瀉需要立即安排檢查與進行適當處置2。
三、內分泌相關
ICPi 引起甲狀腺功能低下的比例遠高於甲狀腺功能亢進,臨床研究發現,後者雖會逐漸恢復,但仍會繼續演變為甲狀腺功能低下3。
CTLA-4抑制劑引起腦下垂體炎 (hypophysitis) 的比例約10%,導致促腎上腺皮質素 (ACTH)、促甲狀腺素 (TSH)、濾泡刺激素 (FSH)、黃體激素 (LH)、生長激素與催乳素等激素部分或全部分泌量下降3。此類副作用不容易被發現,因為其臨床症狀較不具特異性,例如:頭痛、疲倦、肌肉無力、面色蒼白、便秘、體重減輕、食慾下降或噁心等。特定賀爾蒙分泌不足的臨床症狀為:TSH 分泌不足可能引起體重上升、便秘、心搏過緩、注意力不集中或認知障礙;LH/FSH 分泌不足可能發生勃起障礙或月經失調;ACTH 減少則會造成姿態性低血壓、低血鈣或低血鈉等症狀3。
ICPi 可能引起腎上腺炎,導致腎上腺功能不足;然而,腦下垂體炎也可能引起腎上腺功能不足,兩者區分是前者血中的腎上腺皮質醇 (cortisol) 濃度低,而 ACTH 高,後者則是腎上腺皮質醇和 ACTH 的濃度皆低。此外,ICPi 也可能誘發第一型糖尿病,導致病人需長期使用胰島素控制血糖3。
四、肝臟相關
大部分使用 ICPi 引起的肝炎無症狀,能藉由檢測血清肝臟酵素異常發現,約6-14週後可測得肝臟酵素值上升5,然而病人可能沒有臨床表癥,或只有輕微肝臟腫大、門靜脈周圍水腫和淋巴腫大3。若要確認是否為使用 ICPi 引發之肝炎,應排除病毒感染或其他因素,必要時需進行肝臟組織切片來驗證3。
五、肺臟相關
雖然 ICPi 引起的肺部發炎反應 (pneumonitis) 僅有1%3,但若沒有及時處理,其症狀可能變嚴重甚至危及生命,因此醫療相關人員應提高警覺病人是否出現乾咳、進展性的呼吸急促或呼吸有異音等症狀,特別是有肺部原發性或轉移性腫瘤病人更需要小心監測。ICPi 引起的肺部發炎反應相較於其他 irAE 發生較晚,約在使用藥物數個月後產生6。
六、眼或神經相關
曾有鞏膜上皮炎 (episcleritis)、結膜炎 (conjunctivitis)、葡萄膜炎 (uveitis) 或眼眶炎 (orbital inflammation) 案例報告於使用 CTLA-4抑制劑病人身上。為了儘早發現,應請病人注意用藥後是否有出現視力模糊、飛蚊症、閃光、畏光、色差或視野變化、眼睛紅腫痛等症狀出現,並即時反應5。
CTLA-4抑制劑可能引起神經方面的副作用包括格林-巴利症候群 (Guillain Barré syndrome)、無菌性或淋巴性腦膜炎 (aseptic or lymphocytic meningitis)、可逆性後腦病變症候群 (posterior reversible encephalopathy syndrome)、腸道神經發炎 (inflammatory enteric neuropathy) 或橫貫性脊髓炎 (transverse myelitis)。
七、血液相關
ICPi 治療固態腫瘤 (solid tumor) 罕見血球低下副作用,此副作用較常發生在治療淋巴瘤時。紅血球再生不良 (red cell aplasia)、自體免疫性嗜中性球低下 (autoimmune neutropenia)、全血球低下 (pancytopenia) 和後天性A型血友病 (acquired hemophilia A) 可能與使用 CTLA-4抑制劑有關3;PD-1/PD-L1抑制劑也可能發生骨髓增生異常(myelodysplasia)、貧血 (anemia) 和嗜中性白血球低下 (Neutropenia) 等 irAE2。
八、其他
使用 ICPi 病人常見的副作用為倦怠 (fatigue),另約有5%可能發生關節炎或關節痛 (polyarthritis or arthralgia) 的 irAE。腎臟相關 irAE 包括間質性腎炎伴隨發炎性腎皮質腫大 (interstitial nephritis with inflammatory cortical renal enlargement)、肉芽腫性腎炎 (granulomatous nephritis) 或腎小球狼瘡樣腎炎 (glomerular lupus-like nephropathy),其發生率約1%3。CTLA-4和 PD-1抑制劑也可能引起免疫性胰臟酵素升高,大部分案例僅是檢驗值異常,並無任何臨床症狀,但若發生腹痛合併澱粉酶 (amylase) 或脂解酶 (lipase) 上升時,建議應施行影像學檢測以確認是否發生胰臟炎之 irAE3,5。
參、irAE 處置建議
ICPi 引起 irAE 處置可參考美國癌症免疫治療學會 (Society for Immunotherapy of Cancer,SITC)、歐洲腫瘤醫學會 (European Society for Medical Oncology,ESMO)、美國臨床腫瘤學會 (American Society of Clinical Oncology,ASCO) 或美國國家癌症資源網 (National Comprehensive Cancer Network,NCCN) 所發布的治療建議或指引5-8。依據 irAE 嚴重程度可分為輕度 (grade 1)、中度 (grade 2)、重度 (grade 3) 和危及生命 (grade 4) 四種等級。
使用免疫抑制劑可以降低過度活化的免疫反應,類固醇通常是第一線使用的免疫抑制劑,而當類固醇效果不佳時則考慮使用其他免疫抑制劑,例如:infliximab、mycophenolate。研究發現發生 irAE 後使用免疫抑制劑,並不會影響 ICPi 的療效1。
輕度 irAE 的處置,建議使用支持性療法或症狀治療,並持續監測 irAE,多數病人於醫師評估後 ICPi 可繼續治療。中度 irAE 的處置,除了症狀治療外,另需投與低劑量類固醇 (0.5-1 mg/kg),此時建議會診專科醫師並考慮暫停 ICPi 治療。重度或危及生命的 irAE 則應停止使用 ICPi 及安排病人住院治療並會診專科醫師,此時應投與高劑量類固醇 (1-2 mg/kg)。而當類固醇不需再使用時,應以至少一個月的期間逐漸降低劑量,因為太快停用類固醇,irAE 可能會復發 (表二)9。
病人的療效與 irAE 的嚴重程度是評估 ICPi 是否繼續使用的關鍵。若病人使用 ICPi 有療效,之後即使因發生嚴重 irAE 不得不停止治療,其療效仍可持續8。
表二 處置 irAE 的一般原則9
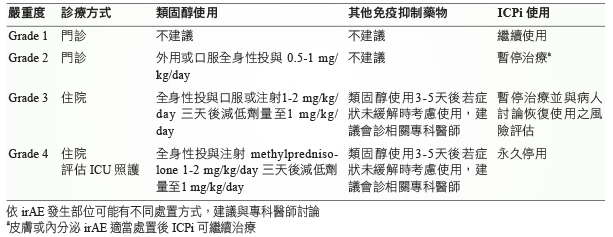
肆、結論
由於從開始使用 ICPi 到停止使用後一年間都可能發生 irAE,以及嚴重的 irAE 若沒有及時處置恐危及生命,因此醫療人員應隨時保持警覺及定期更新 ICPi 相關知識,病人也應被充分告知接受 ICPi 治療後可能產生的副作用與注意事項,包括定期回診追蹤檢查和及時反映任何新產生的症狀。
ICPi 在許多癌症治療上已看到顯著成果,包括病人存活期延長和生活品質改善。整體而言,ICPi 的副作用發生率比傳統化療低,且大部分 irAE 都是可恢復的。由於未來的趨勢是不同機轉的 ICPi 併用、或是 ICPi 合併化療或放療等,如此將會增加 irAE 的發生率和嚴重度,因此藥師更應熟悉 irAE 的症狀及其處理,以確保病人用藥的安全性。
Immune-related Adverse Event of Immune Checkpoint Inhibitor
Yi-Cheng Chen1, Chi-Yuan Cheng1, Tzu-Cheng Tsai1,2
Department of Pharmacy, Chang Gung Memorial Hospital, Linkou1
Department of Long Term Care, Hsin Sheng College of Medical Care and Management2
Abstract
Immune checkpoint inhibitors such as CTLA-4 and PD-1/PD-L1 blockade have been in the limelight among several cancer immunotherapies during the last few years. These drugs augment the immunologic reaction against tumor cells in several cancer types including melanoma, lung cancer, renal cell carcinoma, lymphoma, gastric cancer, hepatocellular carcinoma, colorectal cancer and urothelial carcinoma. Immune checkpoint blockade has shown remarkable benefit and durable response in the treatment of advanced melanoma. However, the new category of medication has led to a different spectrum of dysimmune toxicity termed immune-related adverse event (irAE). Although most irAE could be manageable, serious and even fatal irAE still happened in few cases; hence, early diagnosis and proper management of the irAE are a very important issue. This article will discuss common or notable irAE, and how to deal with irAE.
參考資料:
1. Postow MA, Sidlow R, Hellmann MD: Immune-Related Adverse Events Associated with Immune Checkpoint Blockade. N Engl J Med 2018;378:158-68.
2. Spain L, Diem S, Larkin J: Management of toxicities of immune checkpoint inhibitors. Cancer Treat Rev 2016;44:51-60.
3. Michot JM, Bigenwald C, Champiat S, et al: Immune-related adverse events with immune checkpoint blockade: a comprehensive review. Eur J Cancer 2016;54:139-48.
4. Weber JS, Kahler KC, Hauschild A: Management of Immune-Related Adverse Events and Kinetics of Response With Ipilimumab. J Clin Oncol 2012;30:2691-7.
5. Puzanov I, Diab A, Abdallah K, et al: Managing toxicities associated with immune checkpoint inhibitors: consensus recommendations from the Society for Immunotherapy of Cancer (SITC) Toxicity Management Working Group. J Immunother Cancer 2017;5:95.
6. Haanen JBAG, Carbonnel F, Robert C, et a: Management of toxicities from immunotherapy: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up. Annals of Oncology. 2017;28(suppl_4):iv119-iv42.
7. Brahmer JR, Lacchetti C, Thompson JA: Management of Immune-Related Adverse Events in Patients Treated With Immune Checkpoint Inhibitor Therapy: American Society of Clinical Oncology Clinical Practice Guideline Summary. J Oncol Pract. 2018:JOP1800005.
8. Thompson JA: New NCCN Guidelines: Recognition and Management of Immunotherapy-Related Toxicity. J Natl Compr Canc Netw. 2018;16(5S):594-6.
9. Champiat S, Lambotte O, Barreau E, et al: Management of immune checkpoint blockade dysimmune toxicities: a collaborative position paper. Ann Oncol. 2016;27(4):559-74.
通訊作者:陳宜正/桃園市龜山區復興街5號
服務單位:林口長庚紀念醫院藥劑部藥師/聯絡電話:(O) 03-3281200 ext 3572

