摘要
Colchicine 在臨床上用於痛風的治療已多年,常見的副作用以腸胃道不適為主,而慢性腎衰竭的病人則有較高的風險出現神經肌肉方面的病變。本案例為一名54歲男性,患有末期腎臟病接受腹膜透析治療,急性痛風發作使用 colchicine 0.5 mg QD 治療一個月後,出現肌肉無力伴隨 creatine kinase 值升高 (1460 U/L)、肌電圖及體感覺誘發電位檢查結果異常之現象,入院經檢查及評估,排除可能原因後,懷疑為 colchicine 導致神經肌肉病變之不良反應,而症狀在停藥後逐漸改善。藉由此案例的分享,提醒醫療人員,透析病人使用 colchicine,建議調降劑量為0.3 mg BIW,並留意可能發生的不常見但嚴重之併發症。。
關鍵字:colchicine、myopathy、dialysis、ADR
貳、前言
秋水仙素 (colchicine) 是已使用數百年之久的藥物,可用在許多發炎性疾病,如 familial Mediterranean fever (FMF)、Behçet's syndrome、pericarditis 等,目前最常用於急性痛風發作的治療與預防。Colchicine 常見的副作用主要為胃腸道不適,如噁心、嘔吐、腹部絞痛及腹瀉,其他較嚴重的像骨髓抑制、神經肌肉病變、肝臟細胞損傷等副作用,則較易發生在透析病人身上1-3。本案例是透析病人使用 colchicine 引起神經肌肉病變之藥物不良反應,藉此提醒醫療人員透析病人使用 colchicine 治療時,應密切注意病人可能發生的嚴重併發症,以維護病人用藥安全。
參、病例報告
本案例為一位54歲男性,身高162公分,體重61公斤,曾對 ertapenem 過敏。過去有末期腎臟病、貧血、痛風、高血壓、胃潰瘍及白內障等病史,於2015年開始接受腹膜透析治療,並長期使用藥物控制潛在疾病 (表一)。
表一 病人發生 ADR 當時使用之門診藥物

2017年2月1日由於痛風發作,醫師開立 colchicine 0.5 mg 一天一次,持續使用一個多月後,因四肢漸進性無力持續一個禮拜,因此於3月9日至神經內科就診。根據病人描述,起初爬樓梯時特別費力且無法擰毛巾,後來從座椅起身需旁人協助,但仍可自行行走及維持基本日常活動。除此之外,病人無麻木、壓痛或大小便失禁等其他狀況,並表示在症狀發生前未從事任何激烈的運動。因此醫師初步懷疑可能為急性炎性脫髓鞘多神經根神經病變 (AIDP) 或急性運動性軸索神經病變 (AMAN),建議住院做進一步評估及治療。
病人於3月9日入院後,生命徵象穩定,意識清楚,神經理學檢查顯示有全面性反射減低 (diffuse hyporeflexia),伴隨雙側上肢遠端及下肢近端肌肉力量下降的症狀,腦神經功能檢查正常,無感覺異常現象。腦脊髓液分析結果,total protein 為48.4 mg/dL (normal range, 15-45 mg/dL),略微升高,其餘檢驗項目皆為正常,可排除腦部感染。此外細胞學檢查結果無腫瘤細胞檢出,可排除腫瘤影響。之後陸續安排胸部X光、心電圖、電腦斷層及其他自體免疫疾病相關檢查,皆為正常。肌電圖-神經傳導速度檢查 (EMG-NCV) 及體感覺誘發電位檢查 (SSEP),顯示病人有輕微多發性運動感覺神經病變,以下肢較為嚴重,且四肢皆有周邊感覺傳導缺損。抽血檢查發現 creatine kinase (CK) 值為1460 U/L (normal range, male 20-200 U/L),有異常升高跡象 (表二)。
表二 CK、Myoglobin 檢驗數值追蹤表

住院期間延續門診的藥物治療,但肌肉無力狀況未改善。由於病人痛風發作情況已改善,因此醫師於3月11日停用 colchicine。停藥後,病人自述手部無力的現象有些微改善,因此初步排除 AIDP 及 AMAN。於3月13日追蹤 CK 值,由1460 U/L 降為719 U/L,另測得 myoglobin 值為3087 ng/mL (normal range, male 17-105 ng/mL)。由於病人狀況穩定且症狀持續恢復,CK 值由719 U/L 降為468 U/L、myoglobin 值由3087 ng/mL 降至2157 ng/mL,因此於3月15日出院,持續門診追蹤。二星期後回診,CK 值142 U/L、myoglobin 值328 ng/mL,大幅下降至近正常範圍,肌肉無力現象也已顯著改善。
肆、討論
「肌肉病變」是個廣義的詞,泛指任何與肌肉結構或功能受損相關的疾病,常見的原因有發炎反應、內分泌疾病、電解質不平衡、藥物和毒素、感染以及橫紋肌溶解等,病人多數有不等程度肌肉無力的主述,而正確的診斷則有賴於病史的詢問及臨床檢查來釐清致病原因。
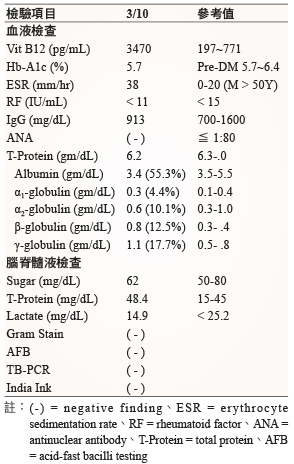
針對此個案,病人因肌肉無力入院,經檢查發現 CK、myoglobin 值升高,懷疑是肌肉相關問題;神經傳導檢查 (EMG-NCV 及 SSEP) 顯示多發性運動感覺神經病變。同時進行其他的相關檢查 (表三),包含:ANA (antinuclear antibody)、RF (rheumatoid factor)、ESR (erythrocyte sedimentation rate)、IgG 皆正常,蛋白質電泳分析並無 γ-globulin 增多情形,排除自體免疫疾病;vitamin B12升高可能為洗腎補充 vitamin B complex 造成,可排除因 vitamin B12缺乏引起的週邊神經病變;血糖及 HbA1c 正常,且病人自述無糖尿病病史,可排除糖尿病神經病變;腦脊髓液生化分析正常,無細菌病毒檢出,可排除腦部感染,細胞學檢查並無發現腫瘤細胞,亦可排除腦部腫瘤影響。然而,住院期間並未檢驗電解質,因而無法評估其影響。另病人主述近期未從事激烈運動,因此排除運動產生的肌肉病變。
表三 其他鑑別診斷相關檢驗數值
在進行上述檢查期間,因痛風狀況穩定,於3/11停用 colchicine,其餘藥物皆延續門診之使用。檢視併用藥物並搜尋文獻,部份藥物亦有肌肉相關之副作用:carvedilol (hypotonia 1-3%)4、amlodipine (muscle weakness ≤ 2%)5、olmesartan (muscle weakness ≥ 4%)6、febuxostat (myositis 2.8%)7,且正巧與 colchicine 的起始使用時間相當 (表一),但由於上述藥物仍持續使用,且病人的臨床症狀及檢驗數值皆有改善,故在排除可能之疾病及其他併用藥物之嫌後,推論此案例可能為 colchicine 引起之神經肌肉病變。
Colchicine 是一種微管聚合抑制劑 (microtubule polymerization inhibitor),藉由與細胞內的微管蛋白 (tubulin) 結合,干擾微管蛋白聚合成微管 (microtubule),進而抑制白血球移行與吞噬作用,以產生抗發炎效果3,8,9。其常見的副作用為腸胃道方面的症狀,如噁心、嘔吐及腹瀉等,而神經肌肉病變並不常發生,根據文獻搜尋,因 colchicine 導致神經肌肉病變的案例報告並不多,實屬不常見之不良反應。因此藉由本案例報告進行深入探討。
一、 Colchicine 引起神經肌肉病變之鑑別診斷
根據文獻指出,colchicine 所引起的神經肌肉病變通常造成四肢靠近軀幹的近端肌肉無力,下肢影響較為顯著,以及遠端肌肉反射減弱、輕微感覺異常等症狀,並伴隨 creatine kinase (CK) 升高,可高達正常上限值的10-20倍,且與症狀嚴重程度呈正比。而這些症狀是可逆的,通常可在停藥數天或數週後回復2,8-12。此外,在肌電圖 (EMG) 及神經傳遞速度檢查 (NCV) 也會發現全身性肌肉病變,伴隨遠端肌肉軸索性多發性神經病變 (axonal polyneuropathy) 的異常變化,這種神經病變通常無症狀或引起輕度感覺異常以及減少深層肌腱反射 (deep tendon reflexes)10,11。而組織病理學方面,則會在肌肉的冷凍或石蠟切片中看到肌纖維內有液泡樣的變化 (vacuolar changes)(圖一、二)8,12。由於上述的理學檢查在其他神經肌肉病變亦可能呈現相同的異常變化,因此不具特異性,無法藉此判斷是否為藥物所造成。故臨床上不建議常規執行肌肉切片進行鑑別診斷,仍須仰賴其他可能疾病的排除及停藥後症狀的改善與否,以評估是否為 colchicine 引起的神經肌肉病變2,8,12。
二、 導致不良反應之機轉及危險因子探討
根據文獻,colchicine 引起之神經肌肉病變為造成直接性的肌細胞傷害,可能同時影響骨骼肌及周邊神經細胞,但以肌肉病變較為明顯2,10。目前致病機轉尚未明確,但歸納幾位學者的研究,推論可能的機轉包括:(一)細胞內自噬性液泡 (autophagic vacuoles) 過度生成,造成富含水解酵素的溶小體外膜損壞,導致通透性增加,使得蛋白水解酶釋放至細胞質中,而造成肌肉纖維功能退化9。(二)藥物干擾微管的形成,造成周邊神經軸突傳導受損,以及破壞肌肉細胞骨架,導致肌肉損傷。而此一機轉正巧與近端肌肉無力、遠端肌肉反射減弱之典型症狀吻合3,10。不良反應的症狀從輕微的肌肉疼痛、無力,到嚴重的橫紋肌溶解12。
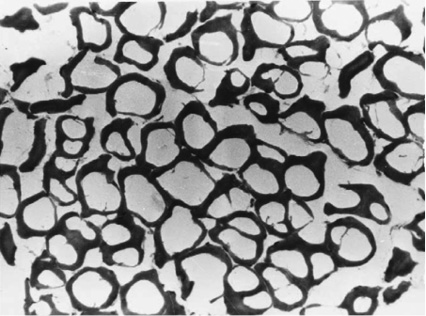
圖一 經蘇木素-伊紅染色 (Hematoxylin eosin stain),在100倍顯微鏡下之肌肉組織冷凍切片12
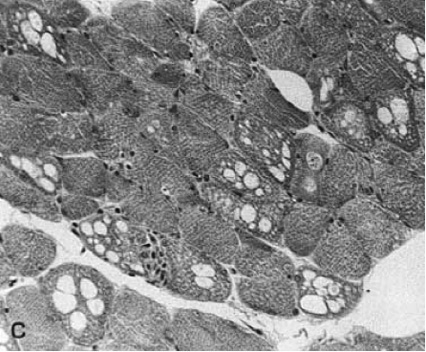
圖二 在200倍顯微鏡下之肌肉組織石蠟切片8
在藥物動力學方面,Colchicine 約16%由肝臟 CYP3A4代謝,而以原型態從尿液排除比例為40-65%,末期腎臟病病人的清除率相較於正常腎功能病人減少約75%,且無法由透析移除13。綜觀上述之藥物動力學特性,若同時併用 CYP3A4抑制劑或患有慢性腎衰竭,特別是透析病人,則可能造成 colchicine 濃度蓄積而增加肌肉病變之風險。因此,除了應盡量避免與 CYP3A4抑制劑併用外,對於洗腎病人,colchicine 在預防痛風發作的劑量建議調整為每週二次,每次0.3 mg,而急性發作的治療,則建議單次給予0.6 mg,且2週內不建議重覆給予,若已經使用 colchicine 作為預防用藥,當急性發作時則不建議再使用 colchicine14。另外,也應避免同時服用其他具有肌肉方面毒性的藥物 (如:HMG CoA reductase inhibitor),減少肌肉病變的風險9。
三、國外文獻案例討論及不良反應評估
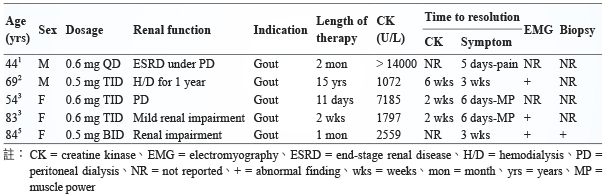
文獻回顧國外因使用 colchicine 引起神經肌肉病變之案例報告,整理如表四1-3,9。不良反應發生族群為慢性腎衰竭病人,因 colchicine 未依病人腎功能情形調整劑量或頻率,而在使用後的數週至數月發生不良反應。本案例同為慢性腎衰竭病人,接受腹膜透析治療,在服用 colchicine 0.5 mg 一天一次,治療急性痛風發作約一個月後,出現肌肉無力症狀,入院後肌電圖檢查異常,同時進行相關檢查排除其他疾病,而症狀於停用 colchicine 後逐漸改善,3個星期後完全回復,且 CK 值也在19天後降至正常範圍,推測可能因 colchicine 未依病人腎功能情形調整劑量或頻率而導致神經肌肉病變。探討本案例之藥物不良反應相關性,依據文獻資料與回顧用藥時序,以 Naranjo score 評估表評分為4分 (表五)15,此案例「可能」因使用 colchicine 引起神經肌肉病變,並導致病人住院,已通報至全國藥物不良反應通報中心。
表四 國外 Colchicine-induced myopathy 之案例報告1-3,9
表五 Naranjo score of colchicine15

伍、結論
雖然 colchicine 引起的神經肌肉病變並不常見,但相較於腎功能正常的病人,慢性腎臟病之透析病人,則存在較高的發生率。本案例報告旨在提醒醫療人員當透析病人使用 colchicine 時,建議調降劑量為0.3 mg,一週使用兩次,並留意因藥物蓄積可能產生之不常見、嚴重的不良反應,以確保用藥安全。此外,應提醒病人在用藥期間若出現近端肌肉疼痛或無力等症狀,宜盡早就醫。
Colchicine-Induced Myopathy: A Case Report
Ning-Yao Yen1, Ya-Fang Cheng1, Tzu-Cheng Tsai1,2
Department of Pharmacy, Chang Gung Memorial Hospital, Linkou1
Department of Long Term Care, Hsin Sheng College of Medical Care and Management2
Abstract
Colchicine has been used for the treatment of gout for centuries. The main side effect is gastrointestinal intolerance. The patients with chronic renal failure have higher risk of developing neuromyopathy. This case is a 54-year-old male with end-stage renal disease under peritoneal dialysis. Muscle weakness developed after acute gout therapy with colchicine 0.5 mg QD for 1 month. Laboratory studies showed elevated creatine kinase level (1460 U/L). Electromyography and nerve conduction velocity test results were abnormal. A series of examinations were done to rule out possible causes and discontinue colchicine due to suspicion of drug-induced myopathy. The muscle weakness gradually improved and CK level normalized after withdrawal of colchicine. We report this case is to remind the medical staff about the importance of colchicine dose adjustment, which was suggested 0.3 mg BIW in the dialysis population. Also, be aware of the uncommon but serious complications..
參考資料:
1. Kellie HB: Colchicine-Induced Rhabdomyolysis. Ann Pharmacother 2002;36:824-6.
2. Altiparmak MR, Pamuk ÖN, Pamuk GE, et al: Colchicine neuromyopathy: A report of six cases. Clin Exp Rheumatol. 2002;20(4 Suppl 26):S13-6.
3. Wilbur K, Makowsky M: Colchicine myotoxicity: case reports and literature review. Pharmacotherapy 2004;24(12):1784-1792.
4. Carvedilol: Drug information. In: UpToDate, Post TW (Ed), UpToDate,Waltham, MA. (Accessed on November 25, 2018.)
5. Amlodipine: Drug information. In: UpToDate, Post TW (Ed), UpToDate,Waltham, MA. (Accessed on November 25, 2018.)
6. Olmesartan. In: IBM Micromedex® DRUGDEX® (electronic version). IBM Watson Health, Greenwood Village, Colorado, USA. Available at: https://www.micromedexsolutions.com/ (Accessed on November 25, 2018.)
7. Febuxostat. In: IBM Micromedex® DRUGDEX® (electronic version). IBM Watson Health, Greenwood Village, Colorado, USA. Available at: https://www.micromedexsolutions.com/ (Accessed on November 25, 2018.)
8. Fernandez C, Figarella-Branger D, Alla P, et al: Colchicine myopathy: a vacuolar myopathy with selective type I muscle fiber involvement. An immunohistochemical and electron microscopic study of two cases. Acta Neuropathol 2002;103 :100-106.
9. Choi SSL, Chan KF, Ng HK, et al: Colchicine-induced myopathy and neuropathy. HKMJ 1999;5:204-7
10. Marc LM: Drug-induced myopathies. Post TW, ed. UpToDate. Waltham, MA: UpToDate Inc. http://www.uptodate.com (Accessed on October 04, 2017.)
11. Adam M, Mitnick HJ, Michael HP, et al: Drug-Induced Myopathies. Bull NYU Hosp Jt Dis. 2009;67(4):358-69.
12. Kayser C, Zeki O, Mukerrem S, et al: Case report: Colchicine-induced myopathy with myotonia in a patient with chronic renal failure. Clinical Neurology and Neurosurgery 2003;105:274-276
13. Colchicine: Drug information. In: UpToDate, Post TW (Ed), UpToDate,Waltham, MA. (Accessed on November 25, 2018.)
14. Vargas-Santos AB, Neogi T: Management of Gout and Hyperuricemia in CKD. Am J Kidney Dis. 2017;70(3):422-439.
15. Naranjo CA et al: A method for estimating the probability of adverse drug reactions. Clin Pharmacol Ther 1981; 30: 239245.
通訊作者:顏寧瑤/通訊地址:桃園市龜山區復興街5號
服務單位:林口長庚紀念醫院藥劑部藥師/聯絡電話:(O) 03-3281200 ext 3543

