偏頭痛治療新藥 Erenumab
中山醫學大學附設醫院藥劑科藥師 黃雅惠、吳俊男
中山醫學大學藥理學科副教授 李建瑩
摘要
偏頭痛 (Migraine) 是一種慢性的神經系統疾病,其典型特徵是持續4-72小時的嚴重單側反復性頭痛發作,伴有噁心、嘔吐、畏光和對聲音恐懼。由於傳統的預防性治療所引起的副作用使其治療受到限制,因此,我們需要有更具療效和安全性的新型治療來預防偏頭痛。近年來,研究開發針對 CGRP (Calcitonin gene-related peptide, 降鈣素基因相關肽) 和 CGRP 受體的單株抗體,用於治療偏頭痛有不錯的療效,而美國 FDA 於2018年核准第一個用於預防偏頭痛的 CGRP 受體單株抗體 erenumab。本文將綜合敘述 erenumab 的藥理學、安全性、臨床試驗和適應症。
關鍵字:migraine、erenumab、CGRP、CGRP receptor、calcitonin gene-related peptide
壹、前言
偏頭痛是一種常見且複雜的神經疼痛疾病。約有10-15%的成年人都有此困擾。偏頭痛在女性 (14.4%) 中比男性 (4.5%) 更加常見1,男女比例約為1:2~3。此反覆發生的頭痛,每次疼痛發作可持續4-72小時,特徵為單側、搏動性、頭痛程度為中至重度,會因日常活動會加劇頭痛,時常伴隨噁心或嘔吐、畏光及怕吵1。根據每月頭痛發作的天數來作區分,可分為陣發性 (episodic) 和慢性 (chronic) 偏頭痛。陣發性偏頭痛定義為每月 < 15天的頭痛發作。如果頭痛發作的頻率每月 ≥ 15天,持續3個月以上,其中有大於8天符合偏頭痛診斷,則陣發性偏頭痛可能會發展為慢性偏頭痛。
根據發作的頻率,藥物也區分為頭痛發作時使用和預防性使用。急性偏頭痛治療目標為停止頭痛或至少停止頭痛進展,常使用的治療藥物有非類固醇消炎止痛藥 (NSAIDs)、麥角鹼衍生物 (如 ergotamine, dihydroergotamine) 和 triptans 類藥物 (如 sumatriptan, rizatriptan)。預防性藥物的治療目標在於降低急性發作的次數、增加急性緩解藥物使用之有效性、減少因偏頭痛所引起的不適感、及喪失工作能力所造成之損失,其藥物可分為乙型阻斷劑 (β-blockers, 如 propranolol)、抗癲癇藥物 (antiepileptics, 如 valproate、topiramate)、三環抗憂鬱劑 (tricyclic antidepressants, 如 amitriptyline)、鈣離子阻斷劑 (Calcium channel blocker, 如 flunarizine) 及其他類 (如肉毒桿菌素, onabutolinumtoxinA)1,2。但這些療法目前存在副作用大、療效不足和患者依從性差等方面的問題,部分患者因副作用而被迫停止治療。
最早於1985年 Edvinsson 提出降鈣素基因相關肽 (Calcitonin gene-related peptide, CGRP) 參與偏頭痛的發病機制。近年來,陸續有大型臨床試驗證實 CGRP 單株抗體之療效。本文將綜合論述 erenumab (Aimovig) 作用機轉、藥效學和藥代動力學。
貳、CGRP 及其受體2
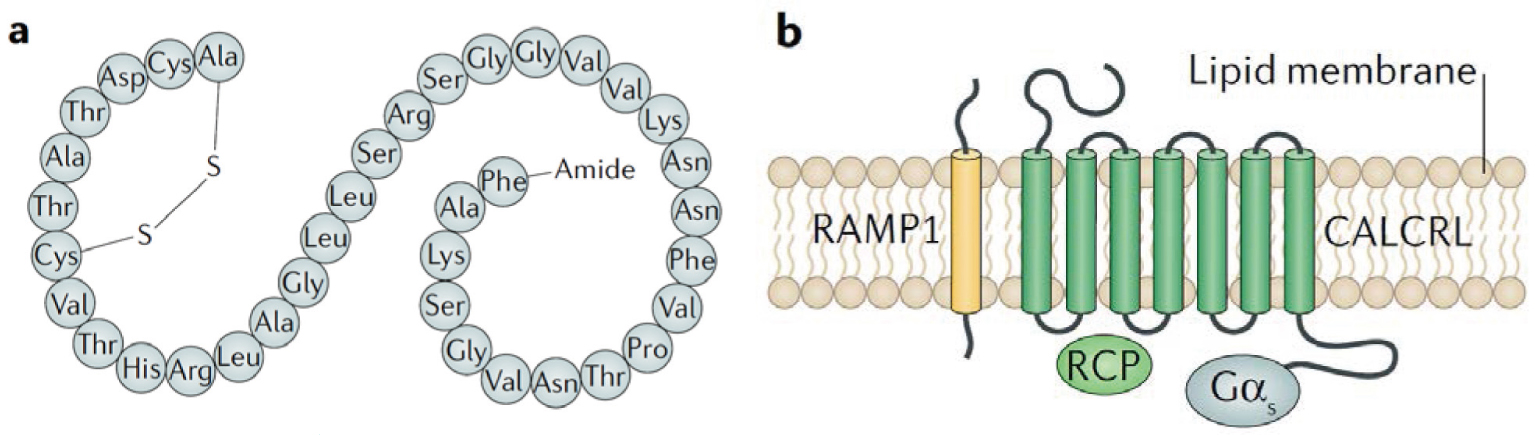
CGRP 是一種神經胜肽 (neuropeptide),於1982年由 Amara 和 Rosenfold 等人首次發現,結構是由37個胺基酸組成,目前有α和β兩種亞型,它們有相似的結構和生物活性,且由單獨的基因合成。α-CGRP (圖一,a)主要存在中樞和周圍感覺神經系統內,其中三叉神經節和背根神經節是其合成及釋放的主要場所;而 β-CGRP 主要存在於腸神經系統中。
CGRP 受體 (CGRP receptor) 是由4個部分組成的複合物 (complex)(圖一, b3),每個配體都有其特異性接合位點和功能性,分別為一、降鈣素受體樣受體 (calcitonin receptor-like receptor, CALCRL):由7個跨膜蛋白複合體所組成;二、受體活性修飾蛋白1 (receptor activity-modifying protein 1, RAMP1):現在已知 RAMP 可分為 RAMP1、RAMP2和 RAMP32,是一小分子單跨膜蛋白 (single transmembrane-spanning proteins),與 CALCRL 形成 CGRP 特異性配體結合位點,其中以 RAMP1為 CGRP 作用之標的;三、受體成分蛋白 (receptor coupling protein, RCP):是位於胞膜內小分子多肽,介導 CALCRL 下游信號傳遞;四、Gs-protein:一樣位於胞膜內,含有 Gαs 亞基,負責傳遞胞內訊息活化 adenylyl cyclase,然後透過 cyclic AMP 活化 protein kinase A (PKA),導致血管擴張 (vasodilation)。
圖一 α-CGRP 和 CGRP receptor complex
所以,當 RAMP1與 CALCRL 結合形成異二聚體 (heterodimer) 時,可產生 CGRP 接合位點,形成對 CGRP 具有最高親和力的功能性受體2,而 RCP 與 Gs-protein 皆位於膜內參與下游之訊息傳遞。CGRP 與特異性的 CGRP 受體結合後造成強力血管舒張作用,亦參與痛覺訊息傳導。因此,在偏頭痛的病理生理中扮演重要角色。
參、Erenumab 用於偏頭痛的治療
Erenumab (Aimovig) 是全人類基因重組的單株抗體 (fully human mAb),對人體內的CGRP受體具有高度選擇性2,可與 CGRP 受體結合而拮抗 CGRP 受體的功能,使釋放出來的 CGRP 無法順利與 CGRP 受體結合,阻斷引起偏頭痛的訊息傳遞途徑,來預防偏頭痛的發作。Erenumab 在2018年5月17日被美國食品藥物管理局 (FDA) 核准上市,是第一個上市的 CGRP 受體抑制劑。
一、適應症和用法劑量4
美國 FDA 核准適應症是用於成人偏頭痛的預防性治療,建議劑量是每月一次皮下注射70 mg,少部分患者則是需要每月140 mg 才可以達到治療效果。皮下注射後,約4-6天後會達到了 erenumab 的血中尖峰濃度,其有效半衰期為28天,因此建議每月注射一次。
二、臨床研究及安全性
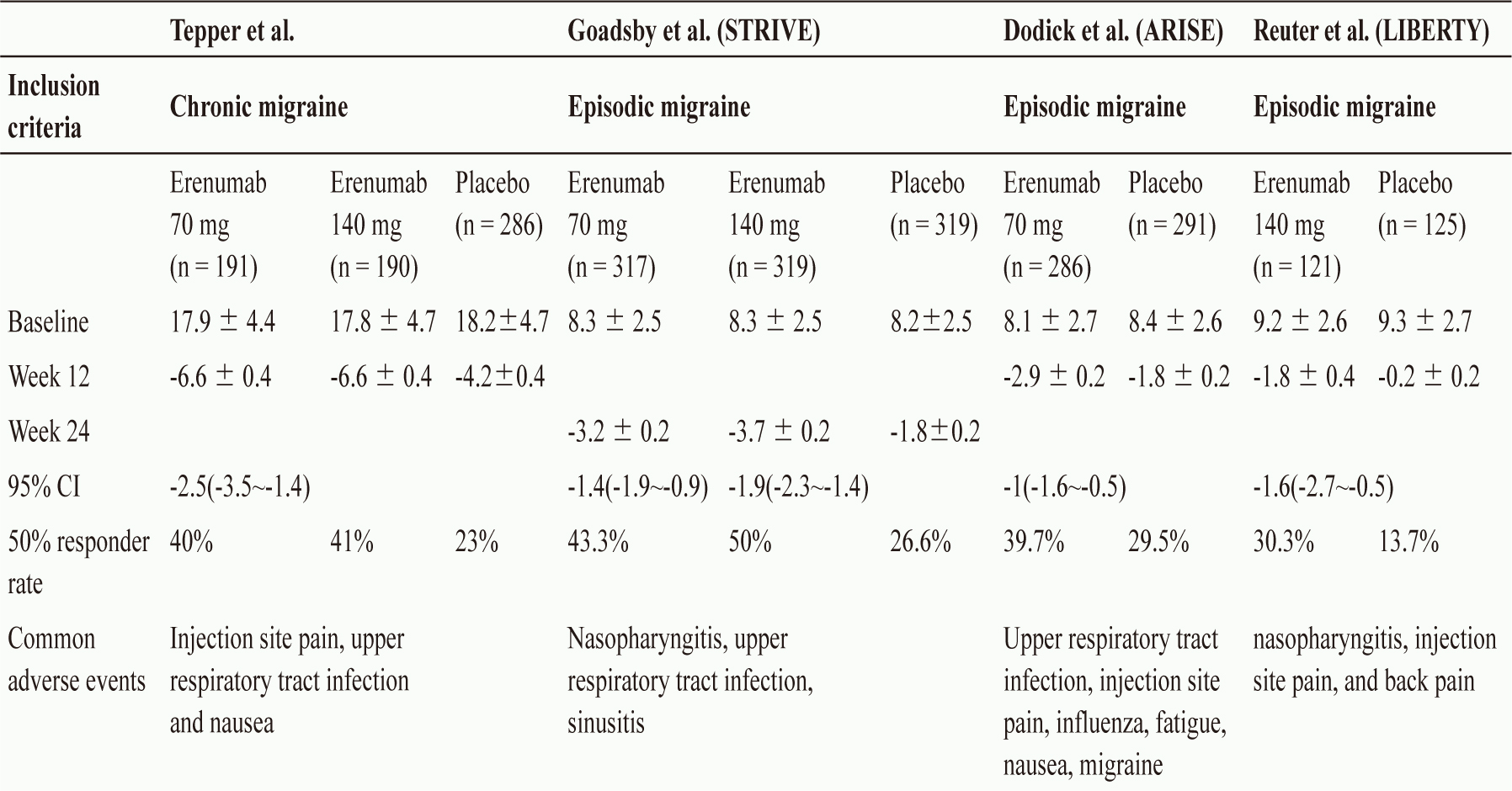
FDA 批准該產品上市是基於三項臨床試驗在偏頭痛中的療效和安全性的結果 (表一)。
表一 Erenumab 治療偏頭痛的臨床試驗
第一個是第Ⅱ期試驗屬隨機、雙盲、跨國多中心、安慰劑對照試驗 (NCT02066415)4,5,收納667位慢性偏頭痛患者,隨機分成3組,每四週給予 erenumab 70 mg (191位)、erenumab 140 mg (190位) 和安慰劑 (286位),持續12週的治療。三組的基線皆分別為每月平均偏頭痛天數為17.9天、17.8天和18.2天。70 mg組患者每月偏頭痛發作天數相比基線下降6.6天,140 mg組下降6.6天,而安慰劑組僅下降4.2天 (difference -2.5, 95% CI -3.5 to -1.4, p < 0.0001)。此外,兩組治療組達每月偏頭痛發生天數減少50%之比率 ( ≥ 50% responder rate)分別為40%和41%,安慰劑組則為24%(p < 0.001)。最常見不良事件是注射部位疼痛、上呼吸道感染和噁心。治療組與安慰劑組的不良事件發生率相似。
第二個是第Ⅲ期試驗,名稱 STRIVE (研究 erenumab 在陣發性偏頭痛患者的預防療效和安全性),屬隨機、雙盲、全球性多中心、安慰劑對照試驗 (NCT02456740)4,6,收納955位陣發性偏頭痛患者以1:1:1的比例隨機分組,每四週給予 erenumab 70 mg (317位)、erenumab 140 mg (319位) 和安慰劑 (319位),持續24週的治療。三組的基線皆為每月平均偏頭痛天數為8.3天。70 mg組患者每月偏頭痛發作天數相比基線下降3.2天,140 mg組下降3.7天,而安慰劑組僅下降1.8天( P < 0.0001)。此外,兩組治療組達每月偏頭痛發生天數減少50%之比率 (≥ 50% responder rate) 分別為43.3%和50%,安慰劑組則為26.6%(P < 0.001)。最常見的不良事件是鼻咽炎、上呼吸道感染和鼻竇炎。治療組與安慰劑組的不良事件發生率相似。
第三個是第Ⅲ期試驗,名稱 ARISE (研究 erenumab 對於偏頭痛患者的預防性治療之療效與安全性),屬隨機、雙盲、全球性多中心、安慰劑對照試驗 (NCT02483585)4,7,收納577位陣發性偏頭痛患者,隨機分成2組,每四週給予 erenumab 70 mg (286位) 和安慰劑 (291位),持續12週的治療,兩組的基線皆分別為每月平均偏頭痛天數為8.1天和8.4天。70 mg組患者每月偏頭痛發作天數相比基線下降2.9天,而安慰劑組僅下降1.8天 (P < 0.0001)。使用70 mg 的治療組達每月偏頭痛發生天數減少50%之比率 ( ≥ 50% responder rate)為39.7%,安慰劑組則為29.5%(P < 0.001)。最常見不良事件兩組相似,包括上呼吸道感染、注射部位疼痛、鼻咽炎、流感、疲勞、噁心和鼻竇炎。
另一項是2018年11月刊登在Lancet,名稱為 LIBERTY 試驗,屬隨機、雙盲、全球性多中心、安慰劑對照試驗 (NCT03096834)2,8,收納246位陣發性偏頭痛患者,隨機1:1分成2組,每四週給予 erenumab 70 mg (121位) 和安慰劑 (125位),持續治療12週。參加此試驗的患者是以前對2至4種偏頭痛預防性藥物治療效果不佳或是不能忍受藥物副作用,其中有95位 (39%) 曾嘗試過兩種預防療法失敗,有93位 (38%) 曾嘗試過三種失敗,56位 (23%)嘗試了四種失敗。兩組的基線皆分別為每月平均偏頭痛天數為9.2天和9.3天。結果顯示,在第12週接受 erenumab 治療的患者中有36位 (30.3%) 平均每月偏頭痛天數比基線減少50%或更多,相比之下安慰劑組只有17位 (13.7%) 患者 (OR = 2.7,95%CI:1.4-5.2,P = 0.002)。此研究結果顯示,erenumab 可有效改善先前多種預防療法都無效的難治性偏頭痛,降低偏頭痛的發作頻率。Erenumab 組報告的不良事件與安慰劑相似,最常見治療引起的不良事件是注射部位疼痛、鼻咽炎和背痛。
三、不良反應與注意事項
關於安全性方面,erenumab 在臨床試驗上常見的副作用 (發生率 ≥ 3%且多於安慰劑)有:注射部位反應 (5-6%) 和便秘 (1-3%)4,9。從一項統合分析 (meta-analysis) 報告中10,erenumab 與安慰劑組中最常見不良事件的發生率如下:注射部位疼痛 (3.5% vs 2.3%)、上呼吸道感染 (4.7% vs 3.3%)、鼻咽炎 (7.0% vs 7.1%)、疲勞 (2.6% vs 2.1%)、噁心 (2.4% vs 2.7%)、鼻竇炎 (2.6% vs 2.1%)和便秘 (2.2% vs 1.2%)。關於對孕婦或胎兒的影響,目前沒有相關研究資料可以確認 erenumab 是否存有不良發育影響,所以不建議使用。用於兒童患者 (18歲以下) 的安全性與療效尚未確立4。
肆、總結
Erenumab 是美國 FDA 核准的 CGRP 受體拮抗劑,是一種新型的偏頭痛預防藥物,是十多年來繼 triptans 類藥物後第一種為偏頭痛患者提供的新療法,並已被證明是一種有效的預防性治療藥物。Erenumab 每月一次的皮下給藥,適用於預防陣發性和慢性偏頭痛的成年患者,在第Ⅱ和Ⅲ臨床試驗中已經充分證明了 erenumab 在預防發作性和慢性偏頭痛中的療效。目前,在美國 Erenumab (70或140 mg) 定價是每支575美元,每年所需藥價約6900美元,比起目前市場上現有的傳統療法貴上許多,但如果將患者因偏頭痛產生而導致勞動力降低所帶來的經濟損失,及生活品質的降低,或許使用 erenumab 可能是一種經濟有效的治療方法,也同時希望有更多同類藥物的上市,在藥品競爭下,可望再調降藥物的售價。未來,希望此藥物的上市後,可以顯著降低全球在偏頭痛的醫療保健支出和與頭痛相關的疾病。
New Drugs for the Treatment of Migraine: Erenumab
Ya-Hui Huang1, Chun-Nan Wu1, Chien-Ying Lee2
Department of Pharmacy, Chung-Shan Medical
University Hospital1
Department of Pharmacology, Chung-Shan Medical
University2
Abstract
Migraine is a chronic neurological disease with nausea, vomiting, photophobia, and phonophobia. Migraine is typically characterised by recurrent attacks of severe, unilateral, pulsating headaches lasting 4-72 h. Its management is limited due to side effects posed by current preventive therapies. Novel therapeutic options with improved efficacy and safety profiles are needed for the prophylaxis of migraine. In recent years, research has been dedicated to the development of monoclonal antibodies against calcitonin gene-related peptide(CGRP) and CGRP receptors for the treatment of migraine. Erenumab is the first fully human monoclonal antibody directed against the CGRP receptor to be FDA-approved for the prevention of migraine. This paper provides a review of erenumab in the pharmacology, safety, clinical trials and indications.
參考資料:
1. 台灣頭痛學會,偏頭痛急性發作和預防性藥物治療準則_2017修訂
2. Jain S, Yuan H, Spare N, et al: Erenumab in the treatment of migraine. Pain Manag. 2018; 8(6):415-426.
3. Edvinsson L, Haanes KA, Warfvinge K, et al: CGRP as the target of new migraine therapies - successful translation from bench to clinic. 2018; Nat Rev Neurol.14(6):338-350.
4. 藥品仿單(Package-Insert)
5. Tepper S, Ashina M, Reuter U et al: Safety and efficacy of erenumab for preventive treatment of chronic migraine: a randomised, double-blind, placebo-controlled Phase II trial. 2017; Lancet Neurol. 16(6), 425-434.
6. Goadsby PJ, Reuter U, Hallstrom Y et al: A controlled trial of erenumab for episodic migraine. 2017; N. Engl. J. Med. 377(22), 2123-2132.
7. Dodick DW, Ashina M, Brandes JL et al: ARISE: a Phase III randomized trial of erenumab for episodic migraine. 2018; Cephalalgia 38(6), 1026-1037.
8. Reuter U, Goadsby PJ, Lanteri-Minet M et al; Efficacy and tolerability of erenumab in patients with episodic migraine in whom two-to-four previous preventive treatments were unsuccessful: a randomised, double-blind, placebo-controlled, phase 3b study. 2018; Lancet ;392:2280-2287.
9. Micromedex®
10. Lattanzi S, Brigo F, Trinka E et al: Erenumab for Preventive Treatment of Migraine: A Systematic Review and Meta-Analysis of Efficacy and Safety. 2019; Drugs. ; 79(4):417-431.
通訊作者:李建瑩/通訊地址:台中市南區建國北路一段110號
服務單位:中山醫學大學藥理學科副教授/聯絡電話:(O) 04-24730022 ext 11664