暴露愛滋病毒前預防性投藥簡介
蕭如君1、李建瑩2
1中山醫學大學附設醫院藥劑科、2中山醫學大學藥理學科
摘要
目前全球約有3,790萬人感染愛滋病,每年約有100萬人死於愛滋病,部分高風險族群感染愛滋病毒的人數仍持續上升。HIV (Human immunodeficiency virus) 感染的盛行率實不容小覷,正確穩定使用PrEP (Pre-exposure prophylaxis,暴露愛滋病毒前預防性投藥)已被證實在不同族群可有效預防愛滋病毒感染。世界衛生組織(World Health Organization, WHO)強烈建議將PrEP作為全球愛滋防治的重要措施之一,2005年起台灣政府開始正視愛滋防治問題,2016年底推動PrEP投藥計畫與現行愛滋病預防措施併行,以期達到愛滋傳染防治之最大成效。
關鍵字: 暴露愛滋病毒前預防性投藥、人類免疫缺乏病毒、Pre-exposure prophylaxis、PrEP、Human immunodeficiency virus
壹、前言
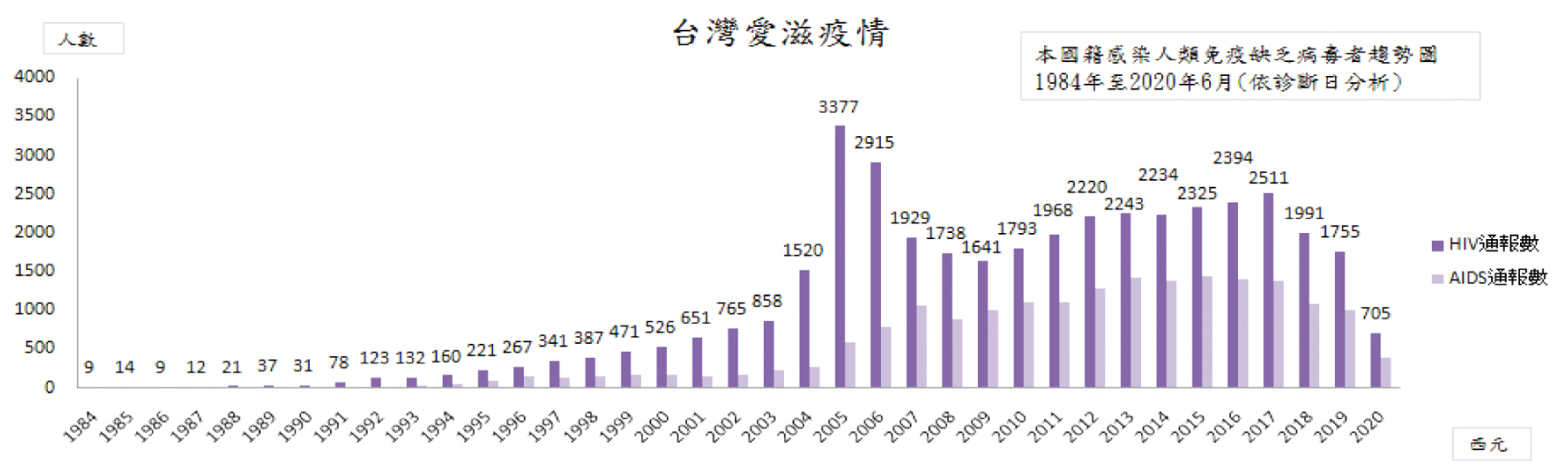
根據聯合國愛滋病組織UNAIDS (Joint United Nations Program on HIV/AIDS)估計,目前全球約有3,790萬人感染愛滋病,每年約有100萬人死於愛滋病,現為全球皆須重視的國際性問題1。台灣每年新增人類免疫缺乏病毒(Human immunodeficiency virus, HIV)約1600~2200人(2007~2017年),感染人數統計於2004~2005年有一波高峰流行,評估主體原因在於靜脈藥癮者(injection drug user, IDU)共用針頭所致。衛生署疾病管制局擬定防治愛滋與毒品的策略,自2005年8月起積極推行第一波減害計畫,提倡清潔針具、不共用針頭、美沙冬替代療法,以及衛教諮商與轉介等措施,此舉讓注射藥物者感染愛滋病毒的疫情獲得改善。統計台灣新增HIV感染數的上升,同性間不安全性行為是愛滋病毒最主要傳染途徑(圖一2)。2016年11月至2017年底,政府再施行第二波減害計畫,推動「愛滋病毒篩檢與暴露愛滋病毒前預防性投藥(Pre-exposure prophylaxis, PrEP)前驅計畫」。HIV感染的盛行率實不容小覷,部分高風險族群感染愛滋病毒的人數仍持續上升。PrEP的效力取決於服藥順從性,正確穩定地使用PrEP已被研究報告證實,在不同族群可有效預防愛滋病毒感染。世界衛生組織(World Health Organization, WHO)強烈建議將PrEP作為全球愛滋防治的重要措施之一3,台灣政府正視愛滋防治問題,推動PrEP投藥計畫與現行愛滋病預防措施(安全性行為、正確使用保險套等措施)併行,無疑能更有效地遏止HIV感染流行。
圖一 台灣愛滋病例趨勢圖2
貳、PrEP用藥相關的研究
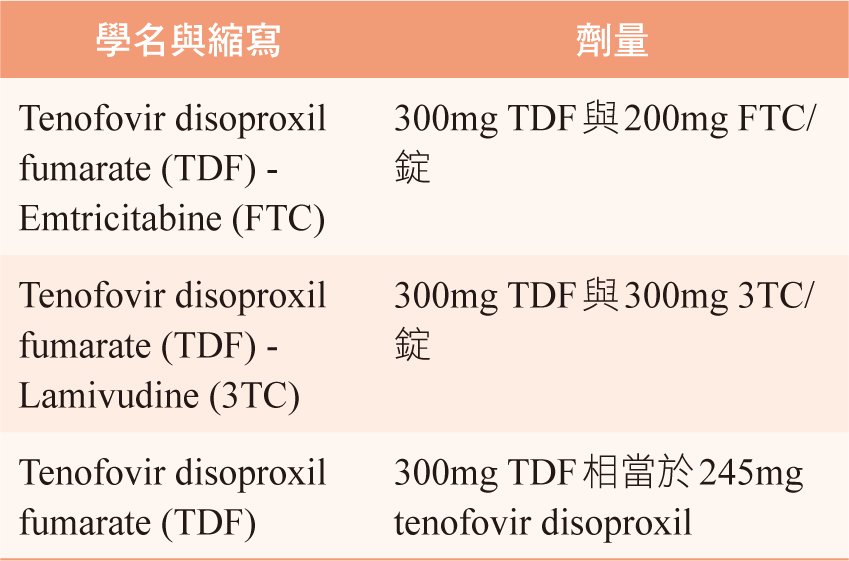
PrEP旨在與潛在愛滋病毒感染者有體液接觸前,先投予抗反轉錄病毒藥物於未受愛滋病毒感染者,以預防被感染,是全面預防HIV感染的方法之一4。WHO主張治療即最好的預防3,PrEP建議用藥如表一。用藥建議FTC (emtricitabine)與3TC (lamivudine)不宜一起使用,兩者為非常類似的化合物,同時間併用並無附加的好處5。2012年7月FDA正式核准TDF (tenofovir) 300mg合併FTC (emtricitabine) 200mg的固定劑量複方製劑(TDF-FTC)為PrEP首選用藥,truvada®(TDF-FTC)是台灣目前PrEP唯一核准用藥,若感染愛滋病毒之高風險者其肌酸酐清除率(creatinine clearance) < 60mL/min則不建議進行PrEP。TDF常見副作用為頭痛、腹瀉、無力、腎功能受損,乳酸代謝性中毒及骨密度流失。FTC常見副作用包括頭痛、噁心、腹瀉、無力、皮膚色素沉澱及乳酸代謝性中毒。PrEP建議適用對象於HIV高感染風險的男男間性行為者與跨性別女性、異性戀血清相異伴侶中的陰性伴侶、注射藥物者、高風險異性戀男性與女性者6。研究證實PrEP用於預防HIV感染是非常有效的工具,據iPrEx(2010年第一個大型臨床試驗,PrEP Initiative)研究中,收納2499位>18歲HIV高感染風險男男性行為與跨性別女性者,口服Truvada組相較口服安慰劑組,減少男男性行為者44 % (95 % CI: 15-63, p=0.005)感染HIV的機率7。於Partners PrEP study team研究中,收納異性戀的血清相異伴侶(heterosexual, serodiscordant couples),分成3組:一、口服TDF組(1584人) 二、口服TDF-FTC組(1579人) 三、口服安慰劑組(1584人),研究結果發現,口服TDF組減少67 % (95% CI: 44-81, p<0.001)感染HIV的機率,口服TDF-FTC組減少75 % (95 % CI: 55-87, p<0.001)感染HIV的機率8。在PROUD與IPERGAY study Group研究結果發現,可減少86 %感染HIV的機率9,10。使用於確定未受愛滋病毒感染者是非常重要的前提,因PrEP只使用2種核苷酸反轉錄酶抑制劑(nucleoside reverse transcriptase inhibitors, NRTI)藥物,若用於已感染HIV者,可能因產生抗藥性導致其HIV治療失敗11。
表一 PrEP建議用藥5
另有一大型DISCOVER study Group臨床試驗研究其他藥物選擇,試驗收納5387位參與者,研究將TDF (tenofovir disoproxil fumarate)置換成TAF (tenofovir alafenamide),TAF在細胞內濃度是TDF 3~5倍,理論上預防效果更好,TAF血中濃度只有TDF 1/10,對腎臟及骨密度的副作用相對降低。研究目前進行至phase III階段,初步結果可知同樣口服FTC-TAF相較於FTC-TDF(1顆/天)在骨密度及腎功能的相對安全性具統計學上意義12。
愛滋病抗病毒製劑需感染科醫師或愛滋病治療專家開立,在使用PrEP之前,應遵循投藥流程(表二)。經醫師謹慎評估使用及定期追蹤,遵循醫囑停用時機及注意事項,方能確保PrEP用藥的安全及有效性6。
表二 PrEP使用流程6
參、PrEP服藥方式6
TDF (tenofovir) 300mg合併FTC (emtricitabine) 200mg固定劑量複方製劑(TDF-FTC, truvada®)是台灣目前PrEP唯一核准用藥。根據臺灣愛滋病學會所制訂第二版暴露前口服預防性投藥使用指引中提出,投藥實務應依據使用者性行為模式與頻率給予適當的PrEP 服藥方式建議。
一、每日使用(Daily use):一天一顆
請使用者在固定時間點每日服用一顆,體內藥物濃度非常穩定。臨床研究中藥物濃度與PrEP保護力密切相關,越穩定服藥,預防效果越好。
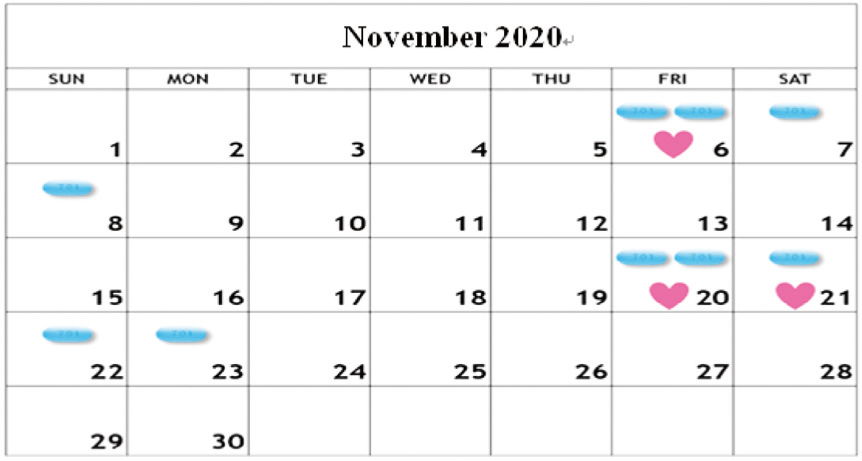
二、依需求使用(On-demand use):每次性行為至少服用4顆(前2後1+1,6~8, Nov.,如圖二)
(一) 單次性行為:使用者在可能發生不安全性行為前2至24小時服用2顆,服藥後的24小時與48小時,各服用1顆。
(二) 連續性行為:使用者在可能發生不安全性行為的前2至24小時服用兩顆後,服藥後每隔24小時服藥一顆,直到最後一次性行為後兩日為止。第2日起的服藥時刻是依照首次服藥日之時刻而定(也就是性行為前那一次的服藥時刻),而非指性行為發生的時刻。
(三) 最後一次服藥到當次性行為時間間隔小於7天:使用者在最後一次服藥距離當次性行為時間間隔若小於7天,當次性行為前2至24小時僅需服用一顆,並在服藥後的24、48小時各服用一顆,完成此次依需求使用暴露前預防性投藥(20~23, Nov.,如圖二)。
圖二 依需求使用PrEP示意圖
肆、PrEP藥物濃度於不同組織有異
口服TDF-FTC發揮保護效果的時間因細胞型態及組織細胞依賴藥物動力學的情況會有所差異,根據研究指出,於直腸組織中所測得的TDF藥物濃度>10倍陰道/子宮頸組織的濃度,藥物進入直腸濃度遠遠高於陰道濃度,因此預估肛交接受方每天持續服用1顆truvada®達7天之保護效果就很好,當停止投予PrEP後,雖然細胞內藥物濃度仍會維持好幾天,但建議在最後一次暴露風險後應持續再服用4週最為理想。而估計女性陰道/子宮頸組織的保護作用,則至少須持續每日服用21天,始可達到最大濃度,方足以確保女性免受愛滋感染13,14。
伍、台灣PrEP推動現況
台灣執行國家性計畫,推動暴露愛滋病毒前預防性投藥計畫,於2016年11月至2017年底推動第一波試辦計畫(前驅計畫),補助預防性藥物105顆,但歸納有「藥物太貴」與「宣導不足」之原因導致成效不彰。2018~2019年招募全國38家醫療院所提供服務。經參考他國成功經驗與檢討前驅計畫和2018~2019年計畫的推動經驗,2020年規劃持續將PrEP融入至整體愛滋防治策略,推動第二波公費計畫,補助對象為:年輕高風險族群(<30歲)或經衛生局認定為本國籍愛滋感染者之配偶或性伴侶,且愛滋檢驗為陰性及高風險指標達≧30分者。開立藥物Truvada®處方箋時,執行機構每次須開立1個月30顆藥物,每名補助對象至多補助360顆Truvada®。
另外藥廠有補助PAP(Patient Assistance Program)計畫,目標在與疾管署公費計畫併行,讓有暴露風險的民眾能在降低藥價負擔下,持續使用truvada®(TDF/FTC),以有效預防感染。PAP計畫執行時間至2020年12月31日止,計畫收納對象須符合:
一、HIV未感染者
二、醫師診斷具感染風險者
三、以下條件擇一:
(一)18~34歲
(二)月收入<36,600元
符合PAP計畫對象者經專業醫療人員完整諮詢檢測後,於醫院購買一瓶truvada®,廠商提供後面兩瓶,由藥師配送藥物,並提供諮詢服務。WHO於2015年規劃出愛滋病防治策略三零(零感染、零死亡、零歧視)願景,在階段目標上,希望在2020年達到90-90-90目標(90%知道自己感染、90%感染者有服藥及90%服藥者病毒量受到控制)。聯合國表示,2018年感染愛滋病毒死亡的人數降至約77萬,比2010年減少約33%,顯見在政策的推動下確具成效,降低因感染愛滋後續健保所需付出之醫療資源成本。
陸、結論
PrEP 策略已是國際趨勢,全球自推動PrEP策略開始,各國新診斷之愛滋感染人數普遍下降。台灣政府重視HIV感染流行之國際性問題,積極推動PrEP投藥計畫,絕非鼓勵愛滋高感染風險族群間的無套性行為。為杜絕愛滋病繼續擴大,於現行各種預防愛滋病傳染措施中,同時加入PrEP措施,以期達到愛滋傳染防治之最大成效,成功節省後續醫療費用及社會成本的支出。
Introduction of the Pre-exposure prophylaxis (PrEP)
Ju-Chun Shiao1, Chien-Ying Lee2
1Department of Pharmacy, Chung Shan Medical
University Hospital
2Department of Pharmacology, Chung Shan Medical
University
Abstract
Approximately 37.9 million people are infected with AIDS in the whole world nowadays and one million people died from AIDS every year. Some specific populations at high HIV infection risk, such as complex sexual partners, are increasing continuously. Therefore, the prevalence rate of HIV (human immunodeficiency virus) infection should not be underestimated and should be committed to reducing. Increasing evidences revealed stable using PrEP (Pre-exposure prophylaxis, preventative administration before exposing to the HIV virus) correctly was able to prevent the HIV infection in different groups. World Health Organization has highly recommended PrEP should be used as one of the principal measures for preventing HIV infection in the whole world. Dealing with the issue of HIV infection, the health authority in Taiwan should promote PrEP drug administration plan and combine with effective AIDS-preventive-measures currently. In this way, the efficacy of AIDS prevention could be achieved maximally.
參考資料:
1. UNAIDS The Joint United Nations Programme on HIV/AIDS. https://www.unaids.org/en/resources/factsheet-2020.
2. 衛生福利部疾病管制署: https://www.cdc.gov.tw
3. WHO. Global HIV/AIDS response: epidemic update and health sector progress towards universal access: progress report 2011. Geneva: UNAIDS, UNICEF; 2011.
4. Tan DH, Hull MW, Yoong D et al : Canadian quideline on HIV pre-exposure prophylaxis and nonoccupational postexposure prophylaxis. Canadian Medical Association journal 2017;189 (47) : 1448-58.
5. WHO Model List of Essential Medicines, 20th List (March 2017). Geneva: World Health Organization; 2017 (http://www.who.int/medicines/publications/essentialmedicines/20th_ EML2017.pdf?ua=1).
6. Guideline for the Use of Pre-Exposure Prophylaxis (PrEP) in Taiwan. Taiwan AIDS Society (第二版) (March 2018).
7. Grant RM, Lama JR, Anderson PL et al : Preexposure Chemoprophylaxis for HIV Prevention in Men Who Have Sex with Men. New England Journal of Medicine 2010; 363(27) : 2587-99.
8. Baeten JM, Donnell D, Ndase P et al : Antiretroviral Prophylaxis for HIV Prevention in Heterosexual Men and Women. New England Journal of Medicine. 2012; 367(5) : 399-410.
9. McCormack S, Dunn DT, Desai M et al: Pre-exposure prophylaxis to prevent the acquisition of HIV-1 infection (PROUD): effectiveness results from the pilot phase of a pragmatic open-label randomised trial.Lancet 2016;387(10013): 53-60.
10. Molina JM,Capitant C,Spire B et al:On-Demand Preexposure Prophylaxis in Men at High Risk for HIV-1 Infection.New England Journal of Medicine. 2015; 373(23) : 2237-46.
11. Hall HI, Song R, Rhodes P et al: Estimation of HIV incidence in the United States. Jama 2008;300:520-9.
12. Mayer KH,Molina JM,Thompson MA et al: Emtricitabine and tenofovir alafenamide vs emtricitabine and tenofovir disoproxil fumarate for HIV pre-exposure prophylaxis (DISCOVER): primary results from a randomised, double-blind, multicentre, active-controlled, phase 3, non-inferiority trial. Lancet 2021;396(10246): 239-54.
13. Seifert SM, Chen X, Meditz AL et al : Intracellular Tenofovir and Emtricitabine Anabolites in Genital, Rectal, and Blood Compartments from First Dose to Steady State. AIDS RESEARCH AND HUMAN RETROVIRUSES 2016;32 : 981-91.
14. Seifert SM, Glidden DV, Meditz AL et al: Dose response for starting and stopping HIV preexposure prophylaxis for men who have sex with men.Clin Infect Dis 2015;60(5) : 804-10.
通訊作者:李建瑩/通訊地址:台中市南區建國北路一段110號
服務單位:中山醫學大學藥理學科/聯絡電話:(O) 04-24739595 ext 11664