化粧品衛生安全管理法藥師角色變革
羅宏丞1、陳俞沛2、王四切1
1嘉南藥理大學藥學系、2衛生福利部臺南醫院中醫科
摘要
因應全球化市場發展並與國際接軌,透過法規協和降低我國化粧品產業面對國際市場之法規障礙,提升我國化粧品產業之國際競爭力,保護消費者使用安全並兼顧產業發展。
「化粧品衛生安全管理法」自108年7月1日起施行以來,多項子法及法規命令均已完備,如化粧品產品登錄辦法、化粧品產品資訊檔案管理辦法、製造場所須符合優良製造準則等,尤其與藥師角色密切相關的化粧品專業技術人員及化粧品安全資料簽署人員等相關法規,大部分的藥師還是一知半解,甚至誤以為原本唯一的「含藥化粧品」監製角色也因修改為「特定用途化粧品」後,將會被其他化粧品專業技術人員所取代。實際上在新法中,藥師除了保留原有的「特定用途化粧品」監製外,更可擴大擔任化粧品專業技術人員為所有種類的化粧品監製,或成為化粧品安全資料簽署人員,為每一個上市販售的化粧品執行化粧品安全評估及簽署,可以專任聘僱或獨立執業兼任。藥師在化粧品產業的角色已經從含藥化粧品監製的小角色,擴張為涵蓋整個化粧品產業的重要角色。
關鍵字: 化粧品衛生安全管理法、化粧品安全資料評估及簽署、建立產品資訊檔案、Cosmetic Hygiene and Safety Act、Safety Assessment、Product Information File
壹、前言
我國「化粧品衛生管理條例」自61年12月28日公佈實施以來已經有47年的「悠久歷史」,有諸多內容早已不符時宜,修正案經總統於107年5月2 日頒布,法律名稱修正為「化粧品衛生安全管理法」,並自108年7月1日起施行,將促使我國化粧品管理邁入新紀元,精進政府管理行政效能,並建構更具安全性及品質優質之化粧品使用環境。不僅如此,同時主管機關公告多項新訂及修正的子法及法規命令施行。
此次化粧品管理規範大幅變動,影響所有化粧品業者及相關從業人員。未來只要是依法設立的公司或商號、工廠及其他或製造輸入化粧品之團體或法人,都需上網完成產品登錄(Notification, NTF)、化粧品安全資料評估及簽署(Safety Assessment, SA)、建立產品資訊檔案(Product Information File, PIF),製造場所都須符合優良製造準則GMP (Good Manufacturing Practice)。為減緩對化粧品產業的衝擊,讓業者們有時間因應準備,重大新規範都設有緩衝時間,並依據產品類型分階段施行,不論是輸入、製造或販售的化粧品業者,都必須提前做好因應及準備。
貳、重大變革
台灣舊的化粧品規範偏向事前審查,從最早期所有一般化粧品的上市前審查,之後改為只有含藥化粧品須上市前查驗登記,甚至廣告內容也須刊登前審查,原本在106年1月6日前,「化粧品衛生管理條例」第24條第2、3項規定化粧品廣告須事前申請衛署粧廣字號許可始得登載或宣播,但本條規定經司法院大法官釋字第744號解釋違憲並於106年1月6日起失效,因此目前所有化粧品廣告已不須再事前申請許可。
在國際間,對化粧品的管理多採上市後監督(post-market surveillance),因此產品登錄(NTF)、產品資訊檔案(PIF)及優良製造規範(GMP)等新興管理制度,在東協、歐盟已行之有年,為接軌國際,提升國際競爭力,建構更安全及良好品質的化粧品環境,本次重大變革包含:
一、新增化粧品定義,將非藥用牙膏、漱口水納入化粧品管理。
二、修改「含藥化粧品」名稱為「特定用途化粧品」,分階段以產品登錄和產品資訊檔案(PIF)制度取代上市前查驗登記制度。
三、增訂化粧品上市前線上登錄制度,須在產品供應、販賣、贈送、公開陳列或提供消費者試用前完成登錄。
四、增訂產品資訊檔案(PIF),並須由化粧品安全資料人員(SA)評估簽署確認產品安全。
五、增訂製造及包裝場所須符合化粧品優良製造準則(GMP),確保產品生產品質。
六、增訂化粧品專業技術人員駐廠監製,確保產品製程均受專業監督管理。
七、廢除刑罰,提高行政罰鍰,新增化粧品檢舉獎勵辦法的吹哨子條款,全民一同監督不法。
八、增訂主動通報、邊境查驗及得要求刊登更正廣告及下架產品等規範。
本次修法並將「含藥化粧品」名稱,修改為「特定用途化粧品」。將其明確定義為具有防曬、染髮、燙髮、止汗制臭、牙齒美白或其他用途之化粧品,除衛生福利部另有規定者外,其含有之特定用途成分應符合「特定用途化粧品成分名稱及使用限制表」之規定。以往輸入特定用途化粧品無論數量、用途皆須向衛生福利部食品藥物管理署申請輸入許可證,此次修法後,如屬個人自用且符合一定數量(每種至多12瓶/盒/罐/包/袋,合計不得超過36瓶/盒/罐/包/袋),得以免證代碼DHM99999999507通關6。
參、新舊法修訂重點及產品責任人(RP)
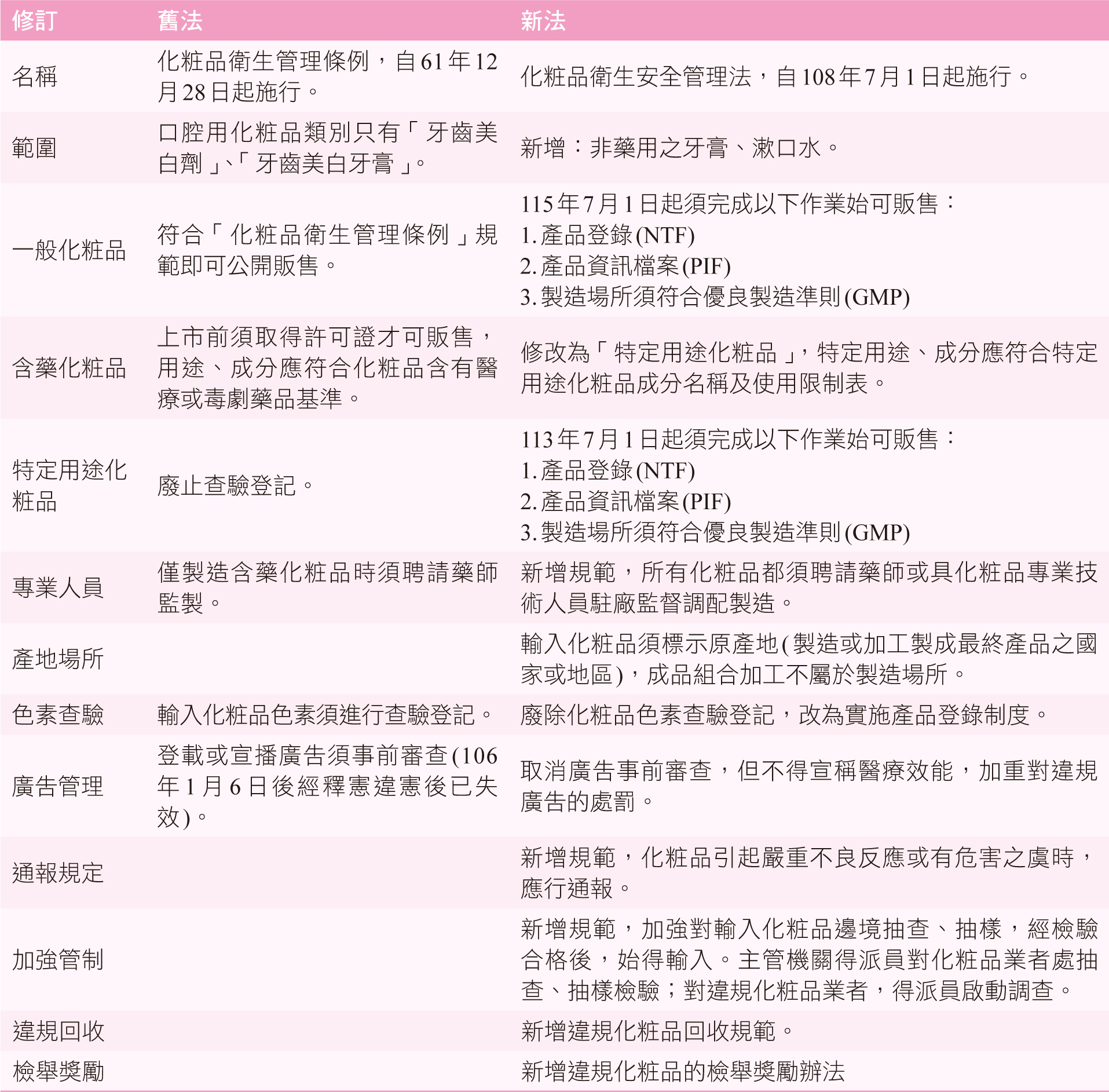
製造者或輸入者為化粧品產品登錄、化粧品產品資訊檔案(PIF)與回收作業的產品責任人 RP (Responsible Person),受託製造者之OEM (原廠委託製造, Original Equipment Manufacturer)、ODM (原廠委託設計加工, Original Designing & Manufacturing)等代工廠不屬於此項義務人,此點與舊法產品製造者是完全義務人精神上有很大的變革(表一)。
表一 新舊法主要的變革7
肆、 化粧品專業技術人員的資格及訓練要求4
新法規定所有化粧品都須聘請藥師或具化粧品專業技術人員駐廠監督調配製造。
一、主要職責
(一)化粧品調配、製造之駐廠監督。
(二)化粧品製造場所、設施、設備維護之檢查及指導。
(三)符合化粧品優良製造準則作業計畫之擬訂及執行之監督。
二、對學經歷的要求
主要有三種,其中化粧品製造相關業務,係指在化粧品製造工廠,從事生產、調配、加工或其他與製造相關之業務:
(一) 正科班
國內外公、 私立專科以上學校化粧品、藥學相關科、系、所或學位學程畢業,領有畢業證書者。
(二) 科班加三年相關業務經歷
國內外公、私立專科以上學校化學、化工相關科、系、所或學位學程畢業,領有畢業證書,並從事化粧品製造相關業務三年以上者。
(三) 同等學歷加五年相關業務
國內外公、私立專科以上學校畢業,領有畢業證書。並從事化粧品製造相關業務五年以上者。
三、化粧品專業技術人員的訓練
包括職前訓練,主管機關或其認可機構舉辦以下訓練二十四小時以上,並領有證明文件。
(一)化粧品衛生安全法令
(二)化粧品製造相關職業倫理
(三)專技人員職責之範圍及內容
(四)其他與化粧品製造相關課程
四、 在職訓練
從業期間,每年至少應接受主管機關或其認可之機構舉辦之化粧品製造及優良製造準則複訓八小時。
伍、化粧品安全資料簽署人員的資格及訓練要求3
新法規定,特定用途化粧品自113年7月1日起、一般化粧品自115年7月1日起須完成以下作業始可販售:
一、產品登錄(NTF)
二、產品資訊檔案(PIF)
三、製造場所須符合優良製造準則(GMP)
其中的產品資訊檔案(PIF)的第十六項「產品安全資料」是一個非常重要的環節,將會由訓練及考試認證通過的安全資料簽署人員(Safety Assessor, SA)負責評估與簽署才算完成PIF的登記。
一、化粧品安全資料簽署人員(SA)的資格
(一)學歷:國內、外大學醫學系、藥學系、毒理學、化粧品學及其相關系、所畢業。
(二)訓練:並曾接受由國內、外大學或中央主管機關所開設化粧品安全性評估 54 小時訓練課程者。
(三)複訓:每年接受8小時以上繼續教育。
二、 化粧品安全資料簽署人員(SA)訓練內容
(一)化粧品管理法規
至少4小時,包含我國化粧品衛生管理規範,國際間化粧品管理規範,我國化粧品產品資訊檔案制度。
(二)化粧品成分之應用及風險
至少8小時,包含美白、防曬、止汗、制臭、染髮、燙髮與其他成分之作用原理與安全性及化粧品常見不良反應或違規案例。
(三)化粧品安全評估方法
至少36小時,包含皮膚生理解剖學、化粧品經皮吸收能力、化粧品皮膚刺激、光老化與光敏感之機轉與臨床症狀、奈米安全性評估、天然物化粧品安全性評估、化粧品風險評估、毒理評估方法(皮膚刺激性、皮膚敏感性、皮膚腐蝕性、眼睛刺激性及基因毒性與致突變性測試)、系統性毒性與安全臨界值、動物試驗替代性方法。
(四)產品安全性評估結論製作
至少6小時。
第一階段考試通過後才能參加實作。
陸、化粧品產品資訊檔 (PIF)3
新法明定製造及輸入化粧品業者應於產品販賣、贈送或提供消費者試用前,建立完整之產品資訊檔案,以確保上市化粧品產品品質、安全及功能之資料完備。其主要的目的為:
一、一般化粧品免經上市前審查,產品品質、安全性與效能性資料難以追溯。
二、參酌歐盟等國家的管理模式,業者應負責其所承諾的產品品質及確保上市後消費者使用安全。
三、遇消費糾紛時,可提出應盡義務的科學證明,提高對消費者健康的保障。
四、與歐盟及東協法規同步,亦與日本、中國大陸等國家管理精神相似,可促進國產品拓展國際市場。
化粧品產品資訊檔(PIF)的規劃重點:
一、一個產品、一個批次紀錄、一個PIF檔。
二、無須事前提交審查(備查),只在必要時提供查核。
三、內容應依實際情況隨時更新或補充。
四、保存人為責任人RP (Responsible Person),即製造者、輸入者或品牌商;受託製造者之OEM、ODM等代工廠不屬於此項義務人。
五、保存時間自產品最後上市日之次日起至少保存五年。
六、保存地點為產品標籤、仿單或包裝上所標示之地址。
七、可以中文或英文書面或電子檔保存。
八、主管機關派員查核時,應於五日前通知。
化粧品產品資訊檔(PIF)並無規定的制式格式,但其內容至少須含以下十六項:
一、產品基本資料:名稱、類別、劑型、用途、製造廠名稱與地址及產品製造或輸入業者資訊。*
二、完成產品登錄之證明文件
三、全成分名稱及其個別量
四、產品標籤、仿單、外包裝或容器
五、製造場所符合化粧品優良製造準則之證明文件或聲明書
六、製造方法、流程
七、使用方法、部位、用量、頻率及族群
八、產品使用不良反應資料
九、產品及各別成分之物理及化學特性
十、成分之毒理資料
十一、產品安定性試驗報告**
十二、微生物檢測報告**
十三、防腐效能試驗報告**
十四、功能評估佐證資料
十五、與產品接觸之包裝材質資料
十六、產品安全資料:經安全資料簽署人員簽名並載明日期之安全性評估結論及建議。
* 化粧品分段製造者,製造廠名稱及地址應包括製程中所有製造商及其執行製程。
** 經安全資料簽署人員依產品屬性或特性評估,且於產品安全資料敘明理由者,得免建立之。
柒、化粧品衛生安全管理法實施時程表
建立化粧品產品資訊檔案 PIF 和符合化粧品優良製造準則 GMP,兩者在三階段的時程是相同的,應建立之化粧品種類及實施日期主要分三個重要階段:
第一階段:特定用途化粧品,113年7月1日起實施。
第二階段:嬰兒用、唇用、眼部用與非藥用牙膏、漱口水之一般化粧品,114年7月1日起實施。
第三階段:一般化粧品,115年7月1日起實施。
表二 新制化粧品衛生安全管理法重要時間點7
捌、結論
藉由本文全面地比較新舊化粧品法規變革及施行細則後,我們可以確切地瞭解到,藥師在新法中所扮演的角色及職責變得更多元且寬廣,從舊法含藥化粧品監製的唯一角色,轉變為多元的化粧品專業技術人員及化粧品安全資料簽署人員,肩負調配、製造之駐廠監督,製造場所、設施、設備維護之檢查及指導,化粧品優良製造準則作業計畫之擬訂及執行之監督,以及化粧品產品安全資料的安全性評估結論、建議與簽署等關鍵角色與職責。
The role of pharmacists in
Cosmetic Hygiene and Safety Act
Hung-Cheng Lo1, Yu-Pei Chen2, Tzu-Chueh Wang1
1Department of Pharmacy, Chia-Nan University of
Pharmacy and Science
2Director, Chinese Medicine, Tainan Hospital,
Ministry of Health and Welfare
Abstract
In response to the development of the global market and in line with international standards. It's time to reduce the legal barriers and step out to the international cosmetics market through legal harmony. Enhances the international competitiveness and protects consumer safety and takes into account the development of the industry as well. The new Law has been implemented since July 1, 2019. A number of regulatory commands have been completed, such as notification, PIF, GMP, etc. Most pharmacists still are a little confused to the new regulations and even mistakenly believe that the original only "role" has been taken away. In fact, in addition to retaining the original role, pharmacists can even expand his role in the new law. Safety assessment and signing can be a full-time employment or independent appointment. The role of pharmacists in the cosmetics industry has expanded from a small role in the supervision of medicated cosmetics to an important role covering the entire cosmetics industry.
參考資料:
1. 107年 - 110年衛生福利部新聞
2. 化粧品衛生安全管理法
3. 化粧品產品資訊檔案管理辦法
4. 化粧品專業技術人員資格及訓練辦法
5. 化粧品衛生管理條例暨相關法規彙編,衛生福利部食品藥物管理署,中華民國一○九年一月
6. 特定用途化妝品新制上路-財政部全球資訊網, 2020-01-02
7. 台美檢驗科技股份有限公司-焦點訊息-化粧品衛生安全管理法修法 Retrieved from 20210102 https://www.superlab.com.tw/cosmetic_hygiene_and_safety/
通訊作者:王四切/通訊地址:臺南市仁德區二仁路一段60號
服務單位:嘉南藥理大學藥學系/聯絡電話:(O) 06-2664911 ext 2226