帕金森氏症之神經精神症狀的藥物治療
鄒毅寰1、林昀珊2、陳敦凉3
1桃園長庚紀念醫院藥劑組、2林口長庚紀念醫院中醫藥劑部、3林口長庚紀念醫院藥劑科
摘要
隨著台灣逐漸邁向高齡化社會,神經退化性疾病如帕金森氏症是好發於老年人的疾病,相較於動作性症狀,非動作性之神經精神症狀 (non-motor neuropsychiatric symptoms) 通常於診斷出帕金森氏症之前早已發生,通常以憂鬱症、焦慮症的形式表現,本文針對帕金森氏症之非動作性神經精神症狀如憂鬱症 (depression)、木然症 (apathy)、焦慮症 (anxiety)、認知功能障礙 (cognitive impairment) 與失智症 (dementia),探討其藥物治療。
關鍵字: 帕金森氏症、非動作性神經精神症狀、藥物治療
壹、前言
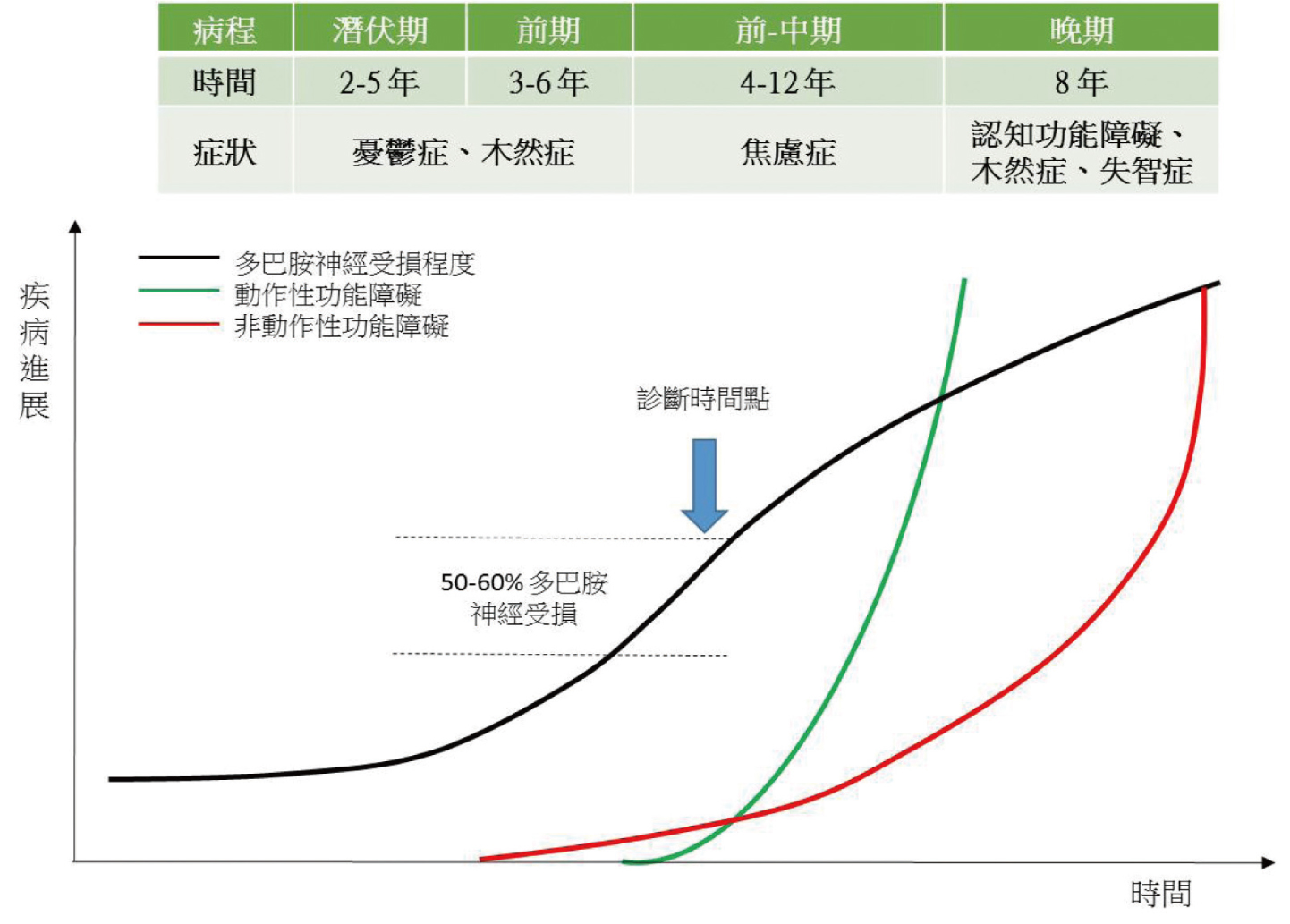
帕金森氏症為一慢性、進展性的神經退化性疾病,主要為動作相關症狀如動作遲緩 (bradykinesia)、運動減退 (hypokinesia),常伴隨休息肢體震顫 (rest tremor) 及僵硬 (rigidity) 等,這些動作症狀與帕金森氏症的診斷有密切關聯,而診斷出疾病時通常多巴胺神經已有 50-60% 受損1,故藥物治療主要以多巴胺類或抑制其代謝的藥物為主,以改善病人的動作障礙症狀。除此之外,疾病進展的同時還會遭遇各種非動作性神經精神疾患所苦。非動作性神經精神症狀會於動作症狀發生前的潛伏期存在數年之久,在整個帕金森氏症的疾病歷程中也會不斷進展,但非動作性神經精神症狀發生的順序、時間及症狀還是會因患者而異。憂鬱症發生於帕金森氏症的潛伏期、前期,焦慮症於前-中期,認知功能障礙與失智症通常於疾病後期發生,木然症可能與憂鬱症及失智症共存,但也可能獨立於兩者發生,目前已有發生於早期帕金森氏症的案例報告 (圖一) 1,故帕金森氏症患者除了需服用多巴胺類藥物來控制動作相關症狀,還需同時服用其他精神疾患的相關藥物控制情緒及認知功能。
圖一 帕金森氏症之動作與非動作症狀發生的時間軸
貳、神經精神症狀之藥物治療
以下主要針對帕金森氏症之非動作性症狀,憂鬱症、木然症、焦慮症、認知功能障礙及失智症作藥物治療的探討。
一、憂鬱症
憂鬱症好發於帕金森氏症患者,一項收納 116 位病患的小型研究指出 30% 的患者存在當前的死亡意念 (28%) 或自殺意念 (11%),4% 的患者有終身自殺的念頭2,所以帕金森氏症合併憂鬱症之治療顯得相當重要,但目前並無明確建議的第一線用藥,臨床醫師大多會以選擇性血清素再回收抑制劑 (selective serotonin reuptake inhibitor, SSRI)、血清素-正腎上腺素再回收抑制劑 (serotonin-norepinephrine reuptake inhibitor, SNRI) 為主,畢竟三環抗憂鬱劑 (tricyclic antidepressant, TCA) 有較多抗膽鹼 (anti-muscarinic) 的相關副作用如認知功能減退、低血壓、尿滯留等,故臨床上目前還是以 SSRI、SNRI 為主要考量。2012 年一項多中心的雙盲隨機對照臨床試驗 (randomized controlled trial, RCT) 將收納的 115 位病患分成三組:Paroxetine 組 (n=42;起始劑量 10 mg/日,最大劑量 40 mg/日)、Venlafaxine XR 組 (n=34;起始劑量 37.5 mg/日,最大劑量 225 mg/日) 及安慰劑 (Placebo;n=39),收納的憂鬱症患者需符合 DSM-IV 標準或漢氏憂鬱量表 (Hamilton Rating Scale for Depression, HAM-D) 的前 17 項評分之總分 >12 分的亞徵候憂鬱症 (subsyndromal depression)。所有患者經過 12 週的治療 (0-2 週的起始劑量,4-6 週作劑量調整及 6-12 週維持治療) 後再以 HAM-D 評估,結果 Paroxetine 組降低 HAM-D 6.2 分 (97.5% CI 2.2-10.3, p=0.0007),Venlafaxine XR 組降低 4.2 分 (97.5% CI 0.1-8.4, p=0.02),試驗結果顯示兩種藥物對於帕金森氏症合併憂鬱症的患者皆有效3,但 Paroxetine 仍列為「可能有效,證據不足」是由於 2008 年一項 RCT 收納 52 位帕金森氏症合併憂鬱症患者, 比較長效型 Paroxetine (n=18;起始劑量 12.5 mg/日,最大劑量 37.5 mg/日)、Nortriptyline (n=17;起始劑量 25 mg/日,最大劑量 75 mg/日) 及安慰劑 (n=17),經過 8 週的治療後以 HAM-D 的改變進行評估,結果顯示 Nortriptyline 與安慰劑相比有顯著差異 (p<0.002),而 Paroxetine 則沒有達到統計上差異 (p=0.165)4 。從上述的臨床試驗可以得知若 SSRI、SNRI 的療效不彰,仍可以選擇 TCA 治療。另外多巴胺受體致效劑 (dopamine agonist) Pramipexole 是目前確定臨床上治療帕金森症合併憂鬱症的有效藥物,其結果是根據 2010 年的一項 RCT,收案的323 位病患中有 296 位進入隨機分配,最後進入主要分析的有 287 位,經過 12 週的治療,Pramipexole (n=139;起始劑量 0.125 mg TID,每週調整劑量,最大劑量為 3 mg/日) 與安慰劑 (n=148) 相比可以顯著降低貝克憂鬱量表 (Beck Depression Inventory, BDI) 分數 (5.9 vs. 4.0;95% CI 0.5-3.4, p=0.01)5, 6。
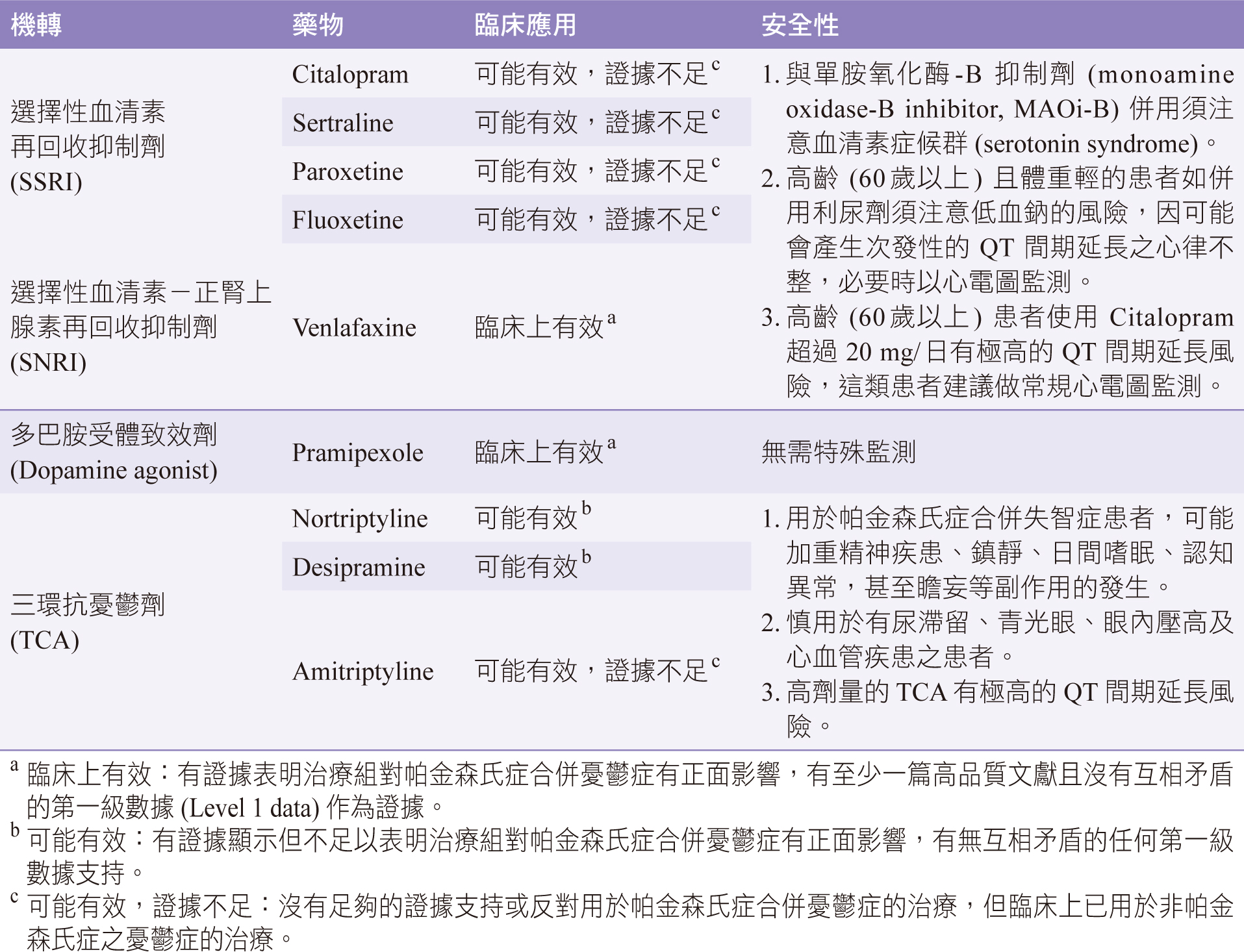
臨床上可用於治療帕金森氏症合併憂鬱症的藥物種類、機轉、臨床應用及安全性簡介 (表一)。
表一 治療帕金森氏症合併憂鬱症之藥物3, 4, 5, 6
二、木然症
60% 的帕金森氏症患者會出現木然症,且木然症可能會伴隨憂鬱症及失智症發生,在有些患者則是單獨表現1。在一項 30 位病患的小型多中心雙盲 RCT 針對非失智症及非憂鬱症型之帕金森氏症患者,結果顯示乙醯膽鹼酯酶抑制劑 (Acetylcholinesterase inhibitor, AchEi) Rivastigmine (n=16;劑量為 9.5 mg/日,耐受不佳可減少至 4.6 mg/日為期兩週) 6 個月的治療與安慰劑 (n=14) 相比可以顯著改善 Lille Apathy Rating Scale (LARS) 分數 (從基值 -11.5 至治療後 -20, p=0.031),但因此臨床試驗的樣本數少,臨床應用列為「可能有效」7。
臨床上可用於治療帕金森氏症合併木然症的藥物種類、機轉、臨床應用及安全性簡介 (表二)。
表二 治療帕金森氏症合併木然症之藥物5,7
三、焦慮症
焦慮症於帕金森氏症患者的盛行率差異巨大,大約為 6-55%8。焦慮症也常發生於多巴胺治療後產生藥效減退 (wearing-off) 的患者9,目前無針對帕金森氏症合併焦慮症所做的 RCT,但一篇統合性分析指出 TCA (Desipramine 與 Nortriptyline,合併之標準均差 SMD=1.43;95% CI 0.09-2.71)、SSRI 的 Citalopram (SMD=1.95;95% CI 0.05-1.89) 以焦慮症為次要結果是有效的10, 11。
另外,2010 年的一項 RCT 收納 69 位病患,55 位進入隨機分配,以狀態焦慮量表 (State Anxiety Inventory, STAI) 評估,結果顯示選擇性正腎上腺素再回收抑制劑 (selective norepinephrine reuptake inhibitor, NRI) Atomoxetine (n=28;起始劑量 40 mg/日,兩週後可增加至 80 mg/日或維持 40 mg/日) 於 8 週的治療相較於安慰劑 (n=27) 有減少 STAI 量表分數的趨勢 (自基值以來的平均組差異 -4.69;p=0.08),但沒有統計上的差異,故 Atomoxetine 於帕金森氏症合併焦慮症之治療仍缺乏證據12。
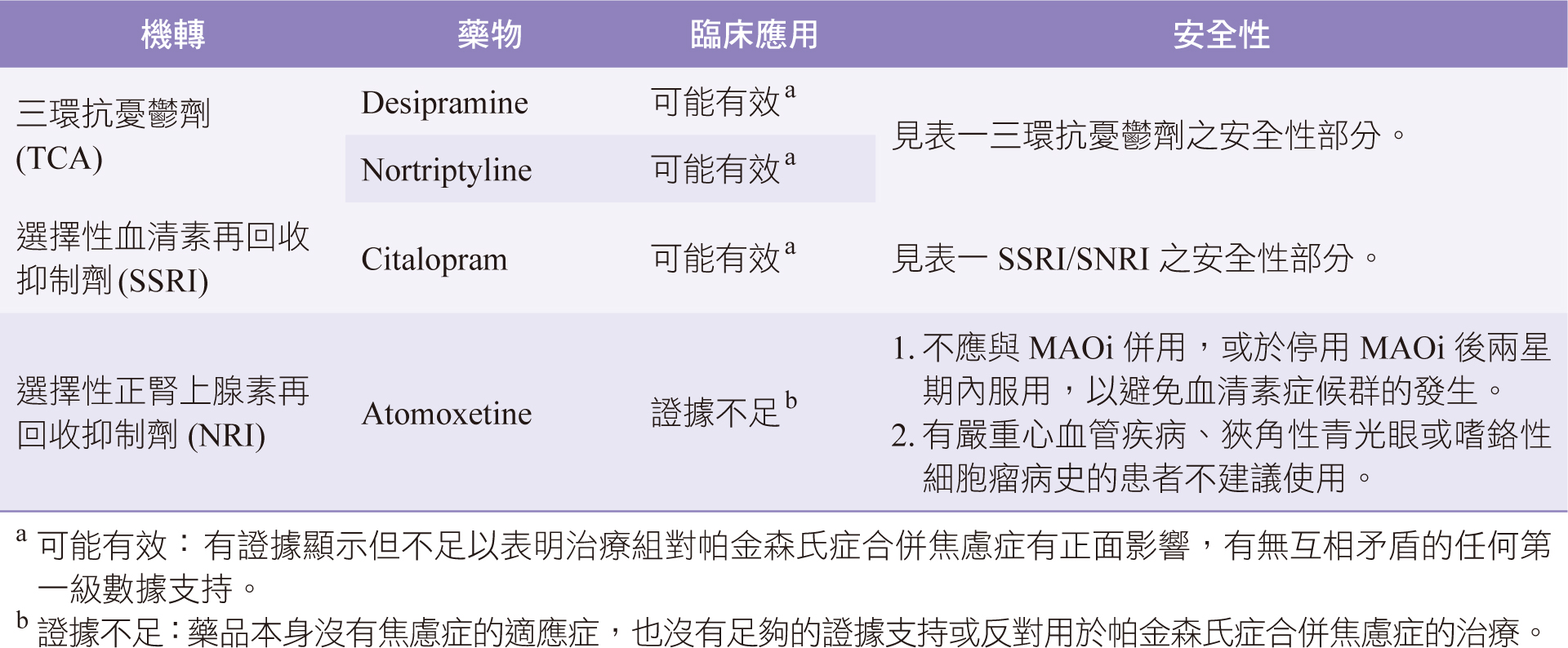
臨床上可用於治療帕金森氏症合併焦慮症的藥物種類、機轉、臨床應用及安全性簡介 (表三)。
表三 治療帕金森氏症合併焦慮症之藥物5, 10,11, 12, 13
四、認知功能障礙與失智症
認知功能障礙與失智症是帕金森氏症的特徵之一,在一項 2015 年澳洲的研究指出早期新診斷的帕金森氏症患者中,9% 患有認知功能異常14,隨著疾病的進展演變成失智症的比率逐漸上升,一項系統性回顧指出,帕金森氏症患者罹患失智症的比率為 24-31%15。
AChEi 類的 Rivastigmine、Donepezil、Galantamine與N-甲基-D-天冬胺酸 (N-methyl-D-aspartate, NMDA) 受體拮抗劑 Memantine 常用於失智症的治療。Rivastigmine 已有治療帕金森氏症相關的輕度至中度失智症的適應症,Donepezil 及 Galantamine 目前臨床上用於非帕金森氏症之失智症治療,對於帕金森氏症合併失智症的治療證據不足。另外,一篇 2015 年發表的統合性分析指出 AChEi 可以同時改善臨床總體評分表 (Clinical Global Impression, CGI) 與簡短智能測驗 (Mini-Mental State Examination, MMSE) 之分數,但 Memantine 能改善 CGI 卻無法改善 MMSE 評分16,故目前 Memantine 用於帕金森氏症合併失智症的治療為「可能有效,證據不足」。
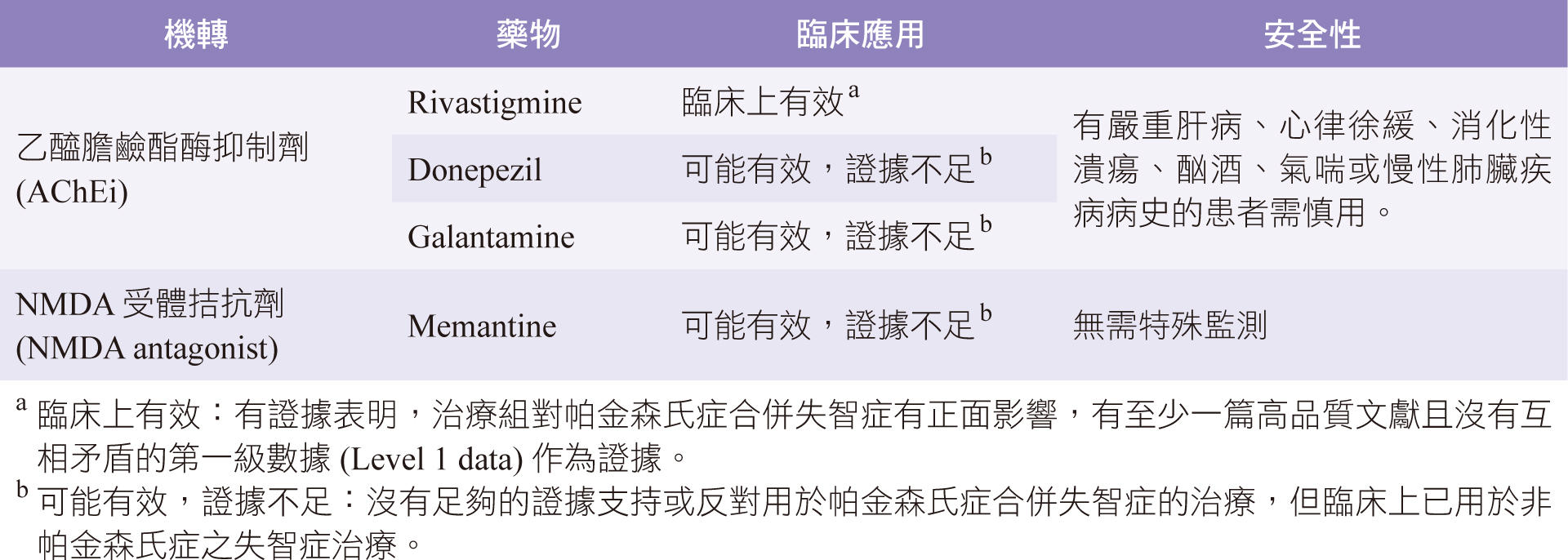
臨床上可用於治療帕金森氏症合併焦慮症的藥物種類、機轉、臨床應用及安全性簡介 (表四)。
表四 治療帕金森氏症合併失智症之藥物5, 16, 17, 18
參、結論
目前缺乏大型的隨機對照臨床試驗探討治療帕金森氏症之非動作性神經精神症狀的用藥,大多數用藥是根據非帕金森氏症族群所得到的結果,從 2011 年 1 月至2016 年 12 月間,僅有 66% 的發表能被視為高品質的隨機對照臨床試驗5,還有部分的症狀如焦慮症沒有臨床試驗佐證,所以目前認定為「臨床上有效」的藥物甚少,大多根據非帕金森氏症族群得到的結果僅能列為「可能有效」或「可能有效,證據不足」3。另外,非動作性症狀的神經傳遞物質與多巴胺較無直接關聯,故患者需同時服用多種調控神經傳遞物質的藥物以控制疾病的進展,多重用藥產生的藥物交互作用是必須多加注意的,例如 SSRI、SNRI 類藥品不得與 MAOi 類藥品併用,否則容易產生血清素症候群。使用 AchEi 的族群如有肝病、心律徐緩、消化性潰瘍、酗酒、氣喘或慢性肺臟疾病等病史必須慎用。
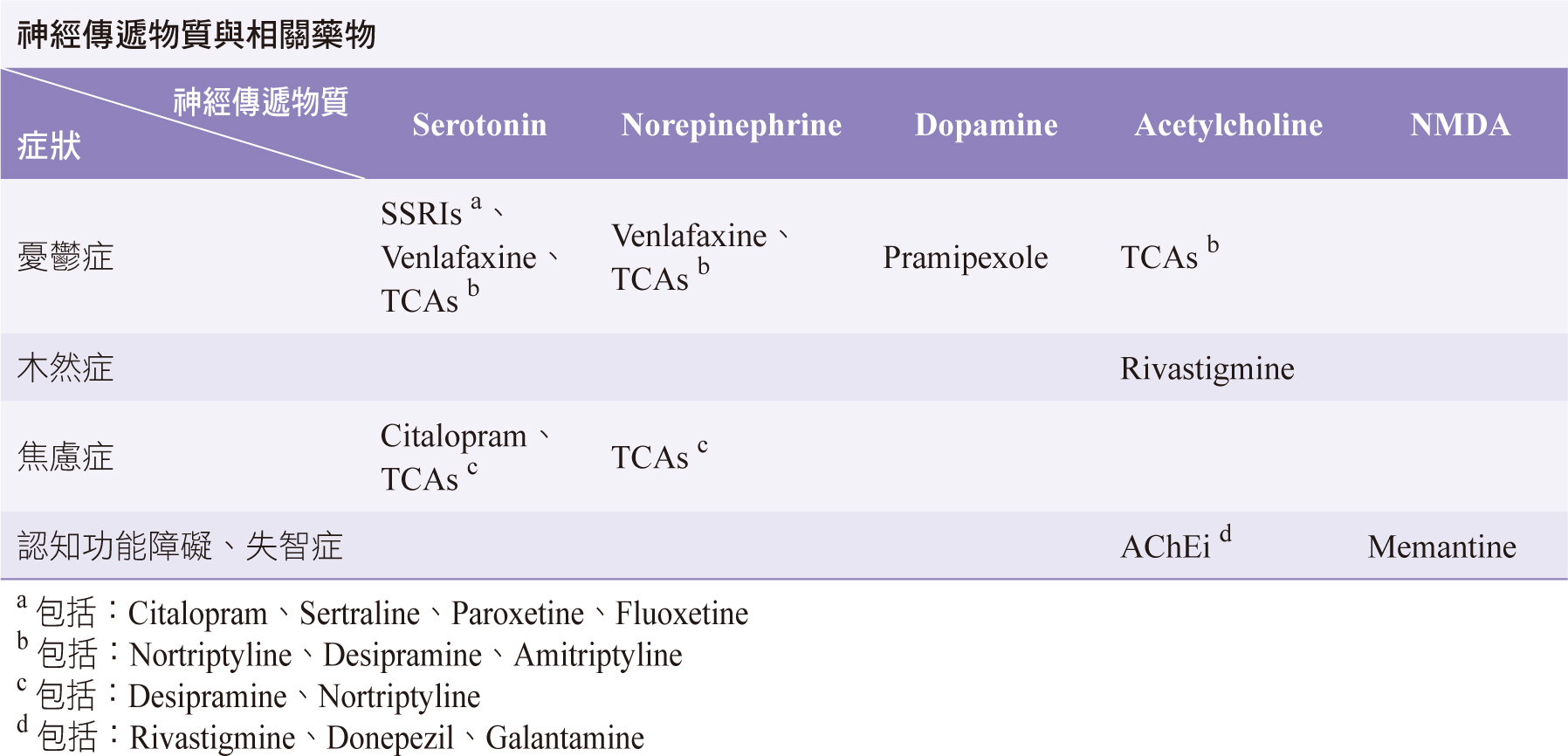
上整理帕金森氏症之非動作性神經精神症狀與牽涉的神經傳遞物質及對應的治療藥物 (表五)。
表五 帕金森氏症之神經精神症狀所關聯的神經傳遞物質與治療藥物5, 10, 11, 12, 13, 16, 17, 18
Pharmacotherapy of neuropsychiatric symptoms in Parkinson’s disease
I-Huan Tsou1, Yun-Shan Lin2, Tun-Liang Chen3
1Department of Pharmacy, Chang Gung Memorial
Hospital, Taoyuan
2Department of Chinese Pharmacy, Chang Gung
Memorial Hospital, Linkou
3Department of Pharmacy, Chang Gung Memorial
Hospital, Linkou
Abstract
Gradually moving towards an aging society in Taiwan, neurodegenerative disease such as Parkinson’s disease that is more common in the elderly. Compared with motor symptoms, non-motor neuropsychiatric symptoms usually occur before motor symptoms in the form of depression and anxiety. This article focuses on the pharmacotherapy of neuropsychiatric symptoms like depression, apathy, anxiety, cognitive impairment, and dementia in Parkinson’s disease.
參考資料:
1. Schapira AH, Chaudhuri KR, Jenner P: Non-motor features of Parkinson disease. Nat Rev Neurosci 2017;18(7):435-450.
2. Nazem S, Siderowf AD, Duda JE, et al: Suicidal and death ideation in Parkinson's disease. Mov Disord 2008;23(11):1573.
3. Richard IH, McDermott MP, Kurlan R, et al: A randomized, double-blind, placebo-controlled trial of antidepressants in Parkinson disease. Neurology 2012;78(16):1229-36.
4. Menza M, Dobkin R, Marin H, et al: A controlled trial of antidepressants in patients with Parkinson disease and depression. Neurology 2009;72(10):886-892.
5. Seppi K, Chaudhuri KR, Coelho M, et al: Update on treatments for nonmotor symptoms of Parkinson's disease-an evidence-based medicine review. Mov Disord 2019;34(2):180-198.
6. Barone P, Poewe W, Albrecht S, et al: Pramipexole for the treatment of depressive symptoms in patients with Parkinson's disease: a randomised, double-blind, placebo-controlled trial. Lancet Neurol 2010;9(6):573-80.
7. Devos D, Moreau C, Maltête D, et al: Rivastigmine in apathetic but dementia and depression-free patients with Parkinson's disease: a double-blind, placebo-controlled, randomised clinical trial. J Neurol Neurosurg Psychiatry 2014;85(6):668-674.
8. Broen MP, Narayen NE, Kuijf ML, et al: Prevalence of anxiety in Parkinson's disease: A systematic review and meta-analysis. Mov Disord 2016;31(8):1125-33.
9. van der Velden RMJ, Broen MPG, Kuijf ML, et al: Frequency of mood and anxiety fluctuations in Parkinson's disease patients with motor fluctuations: A systematic review. Mov Disord 2018;33(10):1521-1527.
10. Troeung L, Egan SJ and Gasson N: A meta-analysis of randomised placebo-controlled treatment trials for depression and anxiety in Parkinson's disease. PLoS One 2013;8(11):e79510.
11. Devos D, Dujardin K, Poirot I, et al: Comparison of desipramine and citalopram treatments for depression in Parkinson's disease: a double-blind, randomized, placebo-controlled study. Mov Disord 2008;23:850–857.
12. Weintraub D, Mavandadi S, Mamikonyan E, et al: Atomoxetine for depression and other neuropsychiatric symptoms in Parkinson disease. Neurology 2010;75(5):448-55.
13. 思銳膠囊仿單,取自 https://info.fda.gov.tw/MLMS/H0001D3.aspx?LicId=02024516
14. Weintraub D, Simuni T, Caspell-Garcia C, et al: Cognitive performance and neuropsychiatric symptoms in early, untreated Parkinson's disease. Mov Disord 2015;30(7):919-27.
15. Aarsland D, Zaccai J and Brayne C: A systematic review of prevalence studies of dementia in Parkinson's disease. Mov Disord 2005;20(10):1255-1263.
16. Wang HF, Yu JT, Tang SW, et al: Efficacy and safety of cholinesterase inhibitors and memantine in cognitive impairment in Parkinson's disease, Parkinson's disease dementia, and dementia with Lewy bodies: systematic review with meta-analysis and trial sequential analysis. J Neurol Neurosurg Psychiatry 2015;86(2):135-143.
17. Bonner LT and Peskind ER: Pharmacologic treatments of dementia. Med Clin North Am 2002;86(3):657–674.
18. 憶思能膠囊仿單,取自https://info.fda.gov.tw/MLMS/H0001D.aspx?Type=Lic&LicId=02022861
通訊作者:鄒毅寰/通訊地址:桃園市龜山區頂湖路123號
服務單位:桃園長庚紀念醫院藥劑組/聯絡電話:(O) 03-3196200 ext 2016