探討肝硬化病人用藥安全與策略擬定-從實證到應用
蘇建豪1、童郁琇1、蔡佳真1、王郁青1
1財團法人高雄長庚紀念醫院藥劑部
2財團法人高雄長庚紀念醫院中藥局
摘要
大部分藥品主要經由肝臟代謝和排除,當肝功能不全時可能導致藥品動力學和藥效學改變,肝硬化病人可能因為病態生理學改變,更易導致藥物不良反應,特別是肝毒性。然而,目前仍缺乏實證指引以提供肝硬化相關處置和治療的依據。因此,依照肝硬化藥品動力學和藥效學、疾病特徵以及目前實證知識進而發展病人的個別化治療將是非常重要的,藉此可避免副作用發生並給予病人適當處置。
關鍵字: 肝硬化、用藥安全、liver cirrhosis、drug safety
壹、前言
肝臟對於大部分藥品的吸收、分布與排除參數上扮演重要的角色,當肝功能不全時可能導致藥品動力學發生不等程度的改變,藥品的作用也可能更加敏感性。非肝硬化病人因活動病毒性肝炎或急性缺血性肝損傷而發生急性肝衰竭時,雖常伴隨血清轉胺酶(alanine aminotransferase, ALT)上升或發生瀰漫性肝壞死,但對於經肝代謝藥品的藥品動力學可能不會有巨大影響。然當發生不可逆損傷如肝硬化時,可能會因肝血流、蛋白質合成、肝酵素活性與膽道排除減少,進而提高藥物血中濃度1。
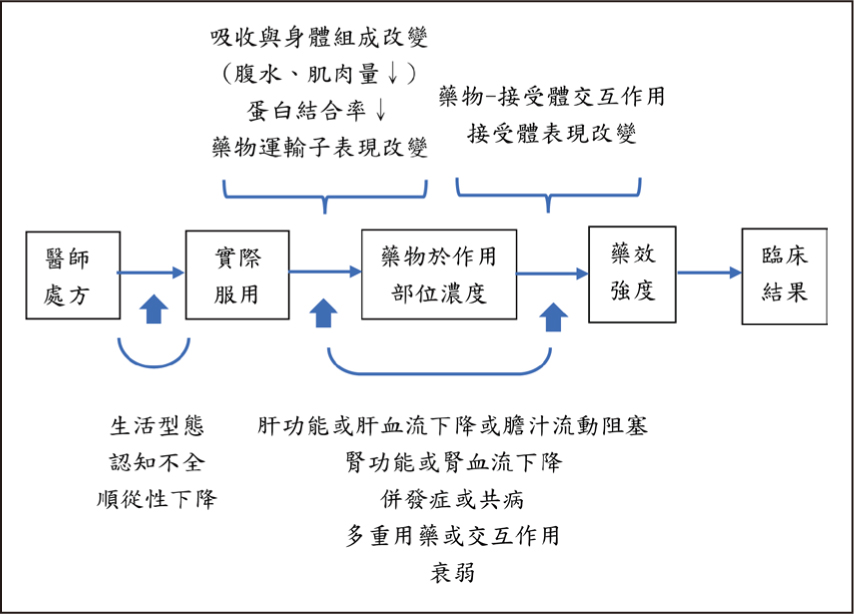
過去因無法精確定義出肝功能損傷程度對藥物排除的影響,也無指引可提供劑量調整依據,使得不適當藥物劑量使用成為門、住診肝硬化病人主要的用藥問題之一2,加上多重藥品使用、老化以及伴隨腎功能異常等因素(圖一)3,使得肝硬化病人於住院過程中有30%曾經歷藥物不良反應(adverse drug reaction, ADR),78.1%被認為為潛在可預防2。若肝硬化進展至嚴重失代償期肝硬化(decompensated cirrhosis),於門診追蹤後1年內有30.5%非計劃性入院認為與用藥有關,其中64.7%被認為是可預防2。
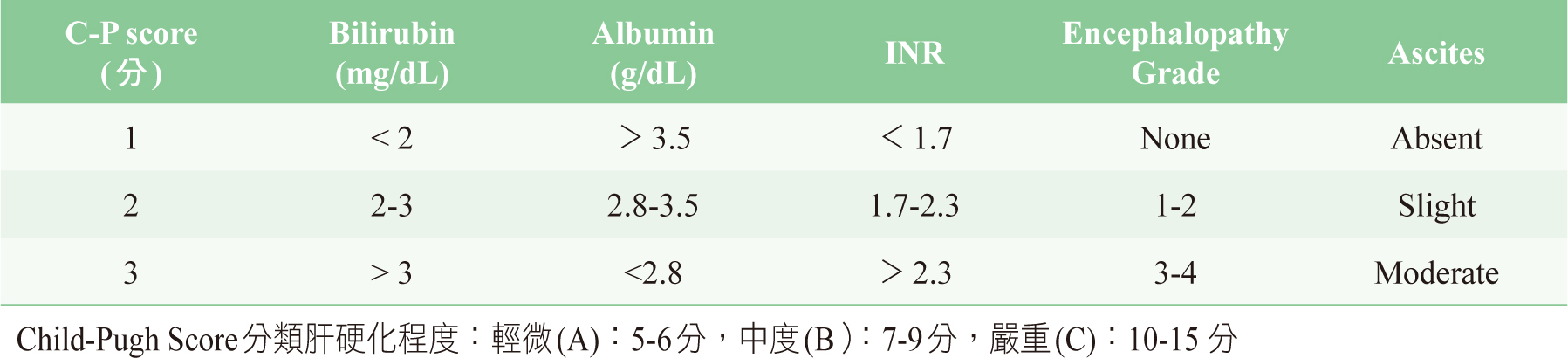
有鑑於此,美國FDA目前已建議當廠商進行新藥申請時,應使用Child-Pugh score(表一)作為肝損傷程度分類對於藥品動力學影響的依據,若能結合實證擬訂個別化用藥策略,將可成為提升肝硬化病人用藥安全的主要契機。
圖一 肝硬化病人藥品動力學與藥效學之改變5
表一 肝硬化之Child-Pugh Score 分數
貳、肝硬化病人藥品動力學改變
肝硬化病人對於藥品動力學影響最常導致藥品暴露量增加,而上升程度主要與藥品特性與病人特徵有關。
一、 藥品特性
藥物於肝臟的清除主要與肝血流、肝臟代謝藥品能力與未鍵結藥品比例有關。肝硬化病人可能因門靜脈高壓產生門靜脈系統分流或因而接受經頸靜脈肝內門體靜脈支架分流術(transjugular intrahepatic portal-systemic shunt, TIPS),當口服高肝臟抽提率(EH>0.7)之藥品時,因顯著降低首渡效應使藥品肝清除率下降(Flow-limited)。隨著肝硬化疾病進展,其肝細胞密度與肝酵素活性下降、血中白蛋白濃度下降以及bilirubin濃度上升,進而減少低肝抽提率藥品(EH<0.3)與高蛋白結合率(fu>70%)之肝清除率4,5。
二、病人特徵
一般來說,肝硬化病人大部分代謝酵素活性會下降25-50%,且隨嚴重度(Child-Pugh A cirrhosis:30-50%、Child-Pugh B cirrhosis:40-70%、Child-Pugh C cirrhosis:50-90%)而呈現差異性下降6。酒精性相較於C型肝炎肝硬化之病人,有較低alcohol dehydrogenase 1A/1B與UGT1A4之活性,而癌症與非酒精性脂肪肝相較於膽汁鬱積型之肝硬化病人,在某些肝臟代謝酵素與運輸子的表現也有較大的影響6,然而對藥物血中濃度改變的臨床意義尚不清楚5,其他如病人營養狀態與基因多型性都可能影響特定肝臟代謝酵素的表現5。
參、肝硬化病人藥品藥效學改變
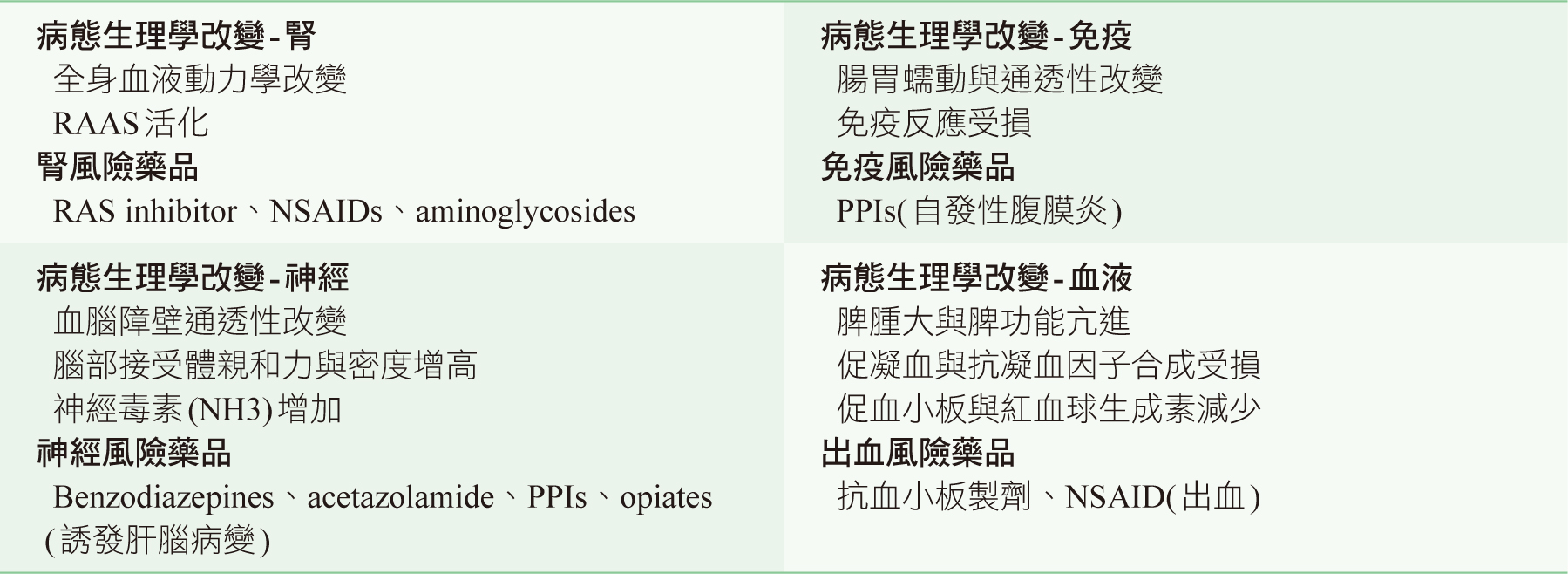
肝硬化病人可能因藥物進入作用部位或接受器數目與敏感度的改變,即使藥物血中濃度未顯著改變下,病人對藥物的反應可能與健康人有異。如肝硬化病人可能因腎元數目減少或利尿功能降低,使得對loop利尿劑反應降低5。此外,因肝硬化病人之腎臟、神經、免疫與血液等病態生理學改變,也可能會增加藥物不良反應發生風險(表二)。而慢性肝病包含肝硬化病人暴露於某些特定藥品如methotrexate, anti tuberculosis drugs與anti retroviral therapy時,可能會增加藥物誘發肝損傷發生風險2,7, B肝帶原病人及中草藥或健康食品誘發肝損傷則會顯著提高死亡風險8,9,肝硬化的存在則未呈現顯著差異。
表二 肝硬化病人病態生理學與藥效之改變5, 13-15
肆、應用實證發展肝硬化病人藥物調整策略
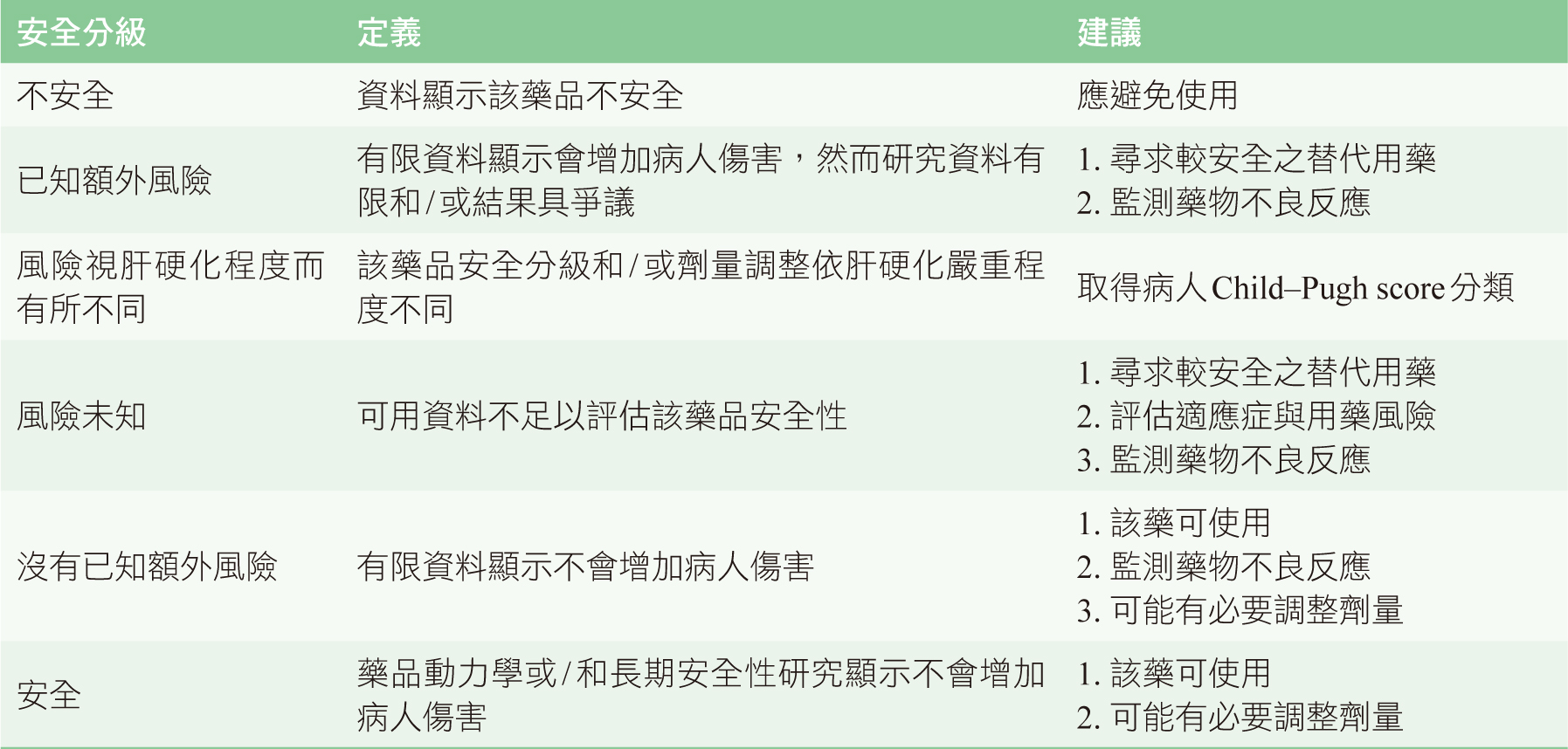
一般來說,ACEI或ARB於肝硬化病人相對耐受良好,然當併發腹水時,因可能誘發動脈低血壓與腎衰竭,應該避免使用(level:B1)10。此外,NSAIDs可能會惡化腹水、水腫與腎功能,並增加食道靜脈曲張(variceal bleeding)與潰瘍出血風險,diclofenac甚至有潛在肝毒性,使用上應謹慎小心(level:B1)10。Acetaminophen之使用劑量也不應該超過2-3 g/日(level:A1)。肝硬化病人PPIs可能會改變腸道菌叢,小腸細菌過度成長與細菌易位,可能會增加自發性腹膜炎與肝腦病變發生風險,長期使用也應謹慎小心(level:B1)10。Weersink等人於2018年分別依據肝硬化對病人藥品動力學的影響與藥物不良反應發生的類型、數目與是否中斷使用,進行文獻與藥品仿單系統性評估後,將常用藥品分為6個風險等級,同時提供標準定義與相對應動作(表三)11,內容包括用藥風險、肝硬化嚴重程度、劑量調整與替代用藥建議(表四)12,醫療人員可同時於網站(https://www.drugsinlivercirrhosis.org)免費查詢相關訊息,而目前也已整合於荷蘭醫師門診的臨床決策支援系統中使用。
表三 肝硬化用藥安全分級與建議11
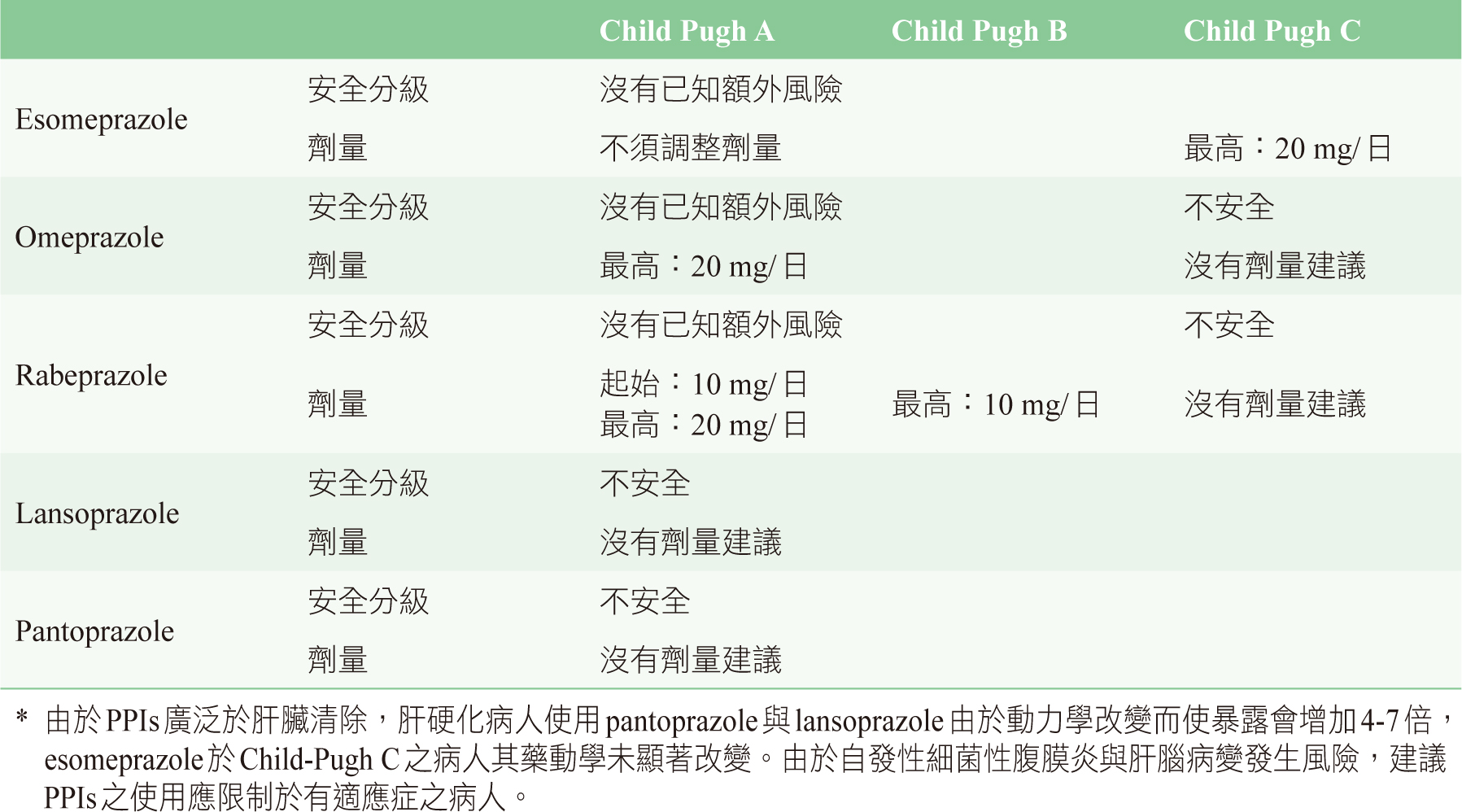
表四 安全性與劑量建議表(以Proton Pump Inhibitors (PPIs)為例)12
伍、結論
肝硬化對藥物動力學影響取決於藥物特性與病人特徵,因病態生理學的變化,可能對於相同濃度卻呈現不同的藥理與不良反應,故臨床上應評估藥品動力學改變、肝病嚴重程度、影響的代謝路徑、藥物給與途徑與劑量及組織對於藥理作用的反應,同時納入藥物於肝硬化病人用藥安全實證考量,以確保能安全且適當的使用藥品,提高病人用藥安全10。
An Evidence-Based Practice of Drugs Safety and Management Strategies in Patients with Liver Cirrhosis
Chien-Hao Su1, Yu-Hsiu Tung1, Chia-Chen Tsai2,
Yu-Chin Wang1
1Department of Pharmacy, Kaohsiung Chang Gung
Memorial Hospital
2Department of Chinese Medicine pharmacy, Kaohsiung Chang Gung Memorial Hospital
Abstract
Most drugs are primarily metabolized and excreted by liver. The presence of liver dysfunction can result in clinically pharmacokinetic (PK) and pharmacodynamic (PD) alternations of medicines. Patients with liver cirrhosis may have an increased susceptibility to adverse drug events particularly hepatotoxicity due to pathophysiological changes. However, the paucity of evidence-based guidelines for the management and treatment of liver cirrhosis, individualized therapy based on PK and PD of medicines, disease manifestation and current evidence-based knowledge with liver cirrhosis is very important. Furthermore, adverse drug reactions can be avoidable and patient care can be appropriately managed.
參考資料:
1. Diep U, Chudow M, Sunjic KM: Pharmacokinetic Changes in Liver Failure and Impact on Drug Therapy. AACN advanced critical care 2017;28:93-101.
2. Hayward KL, Weersink RA: Improving Medication-Related Outcomes in Chronic Liver Disease. Hepatology communications 2020;4:1562-77.
3. Cheema E, Al-Aryan A, Al-Hamid A: Medicine use and medicine-related problems in patients with liver cirrhosis: a systematic review of quantitative and qualitative studies. Eur J Clin Pharmacol 2019;75:1047-58.
4. Pena MA, Horga JF, Zapater P: Variations of pharmacokinetics of drugs in patients with cirrhosis. Expert review of clinical pharmacology 2016;9:441-58.
5. Weersink RA, Burger DM, Hayward KL, et al: Safe use of medication in patients with cirrhosis: pharmacokinetic and pharmacodynamic considerations. Expert opinion on drug metabolism & toxicology 2020;16:45-57.
6. El-Khateeb E, Achour B, Al-Majdoub ZM, et al: Non-uniformity of Changes in Drug-Metabolizing Enzymes and Transporters in Liver Cirrhosis: Implications for Drug Dosage Adjustment. Mol Pharm 2021;18:3563-77.
7. Teschke R, Danan G: Drug-induced liver injury: Is chronic liver disease a risk factor and a clinical issue? Expert opinion on drug metabolism & toxicology 2017;13:425-38.
8. Huang YS, Chang TT, Peng CY, et al: Herbal and dietary supplement-induced liver injury in Taiwan: comparison with conventional drug-induced liver injury. Hepatology international 2021.
9. Huang YS, Tseng SY, Chen WW, et al: Clinical characteristics and outcomes of drug-induced liver injury in Taiwan with an emphasis on the impact of chronic hepatitis B infection. Journal of the Chinese Medical Association : JCMA 2021.
10. KASL clinical practice guidelines for liver cirrhosis: Ascites and related complications. Clinical and molecular hepatology 2018;24:230-77.
11. Weersink RA, Bouma M, Burger DM, et al: Evidence-Based Recommendations to Improve the Safe Use of Drugs in Patients with Liver Cirrhosis. Drug safety 2018;41:603-13.
12. https://www.geneesmiddelenbijlevercirrose.nl/zorgverleners/geneesmiddelen/protonpo mpremmers/
13. Tapper EB, Henderson JB, Parikh ND, et al: Incidence of and Risk Factors for Hepatic Encephalopathy in a Population-Based Cohort of Americans With Cirrhosis. Hepatology communications 2019;3:1510-9.
14. Lieber SR, Jiang Y, Moon A, et al: Antiplatelet Medications Are Associated With Bleeding and Decompensation Events Among Patients With Cirrhosis. Journal of clinical gastroenterology 2021.
15. Alhumaid S, Al Mutair A, Al Alawi Z, et al: Proton pump inhibitors use and risk of developing spontaneous bacterial peritonitis in cirrhotic patients: A systematic review and meta-analysis. Gut pathogens 2021;13:17.
通訊作者:蘇建豪/通訊地址:高雄市鳥松區大埤路123號
服務單位:財團法人高雄長庚紀念醫院藥劑部/聯絡電話:(O) 07-7317123 ext 6134