胃食道逆流治療藥物之新發展
廖文聰1、蔡敏鈴2
1中山醫學大學附設醫院
2中山醫學大學
摘要
飲食習慣加上生活壓力致使胃食道逆流及胃潰瘍的發生率增加,目前的治療方法朝向降低胃酸的分泌來改善症狀。除了早期的鋁鎂制酸劑、H2受體拮抗劑及質子幫浦抑制劑之外,vonoprazan是一種鉀離子競爭性酸抑製劑(Potassium-competitive acid blockers (P-CABs)),研究證實具有不劣於質子幫浦抑制劑的療效,且作用時間快,持續時間長,也不會競爭性抑制肝臟酵素cytochrome P450 (CYP)2C19 的代謝造成某些藥物交互作用,可做為胃酸過多等相關疾病治療的新選擇。
關鍵字: PCAB、vonoprazan、胃潰瘍、鉀離子競爭性酸抑製劑、胃食道逆流
壹、前言
人類胃中的壁細胞(parietal cell)可經由多項機制而促進胃酸的分泌。胃酸可以殺菌也可以活化胃蛋白酶來幫助消化。當胃酸分泌失衡或是食道和胃之間的賁門括約肌鬆弛,則易造成胃潰瘍和十二指腸潰瘍及胃食道逆流(gastroesophageal reflux disease, GERD)等疾病。現今的治療方法仍以降低胃中酸度為主軸,藥物也從酸鹼中和制酸劑進展到H2受體拮抗劑(histamine H2 receptor antagonist )、質子幫浦抑制劑(proton pump也叫H+/K+ ATPase inhibitor, PPIs)及於2015年始從日本上市的鉀離子競爭性酸抑制劑(Potassium-competitive acid blockers (P-CABs))vonoprazan,經由和鉀離子競爭進而阻斷質子幫浦來達到減少胃酸的分泌1。
貳、胃食道逆流疾病簡介
一、流行病學
西方人中GERD大約佔了10%到20%的人口,其中又以60至70歲的成年人占大多數2。台灣於西元1995 年統計盛行率約為 5%,2018年則提升為20%4。飲食習慣的改變及不良的生活作息再加上人口老化多重用藥的影響皆是造成GERD盛行率上升的原因3。
二、症狀
GERD的患者口腔經常會有酸味,因胃酸逆流所以常出現心灼熱感或胸痛而誤以為是心臟疾病。 胃酸反覆侵蝕食道除了造成食道發炎潰瘍之外也會造成食道狹窄或遠端食道發生腸化生(intestinal metaplasia)讓上皮細胞從鱗狀上皮變為腸柱狀上皮而成為巴雷氏食道(Barrett's esophagus),巴雷氏食道在未來演變為食道腺癌的機率會增加。此外,有些患者還會有食慾不振、貧血、吞嚥困難、喉嚨異物感、聲音沙啞、睡眠障礙等症狀3,4。GERD的嚴重度分級如表一4。另外依患者食道黏膜受損狀態分成三種類型如表二5。
表一 胃食道逆流的嚴重度分級4
表二 GERD依症狀分類類型5
三、GERD致病機轉
可略分為三種:(一)胃和食道間壓力差增加及下食道括約肌(lower esophageal sphincter,LES)的收縮力減低導致收縮功能失常而無法緊密關閉,或是下食道括約肌鬆弛頻率增加,導致胃酸逆流至食道。(二)食道蠕動及唾液分泌障礙或黏膜防禦機能受損而讓胃酸產生逆流。(三)胃排空遲滯導致胃內消化物滯留,增加逆流風險。而慢性阻塞性肺病、體重過重、尼古丁和造成 LES 收縮力下降的某些藥物,例如鈣離子阻斷劑、賀爾蒙、benzodiazepines類藥物都可能使胃食道逆流的發生機率上升4,5。
參、胃酸分泌與質子幫浦的關係
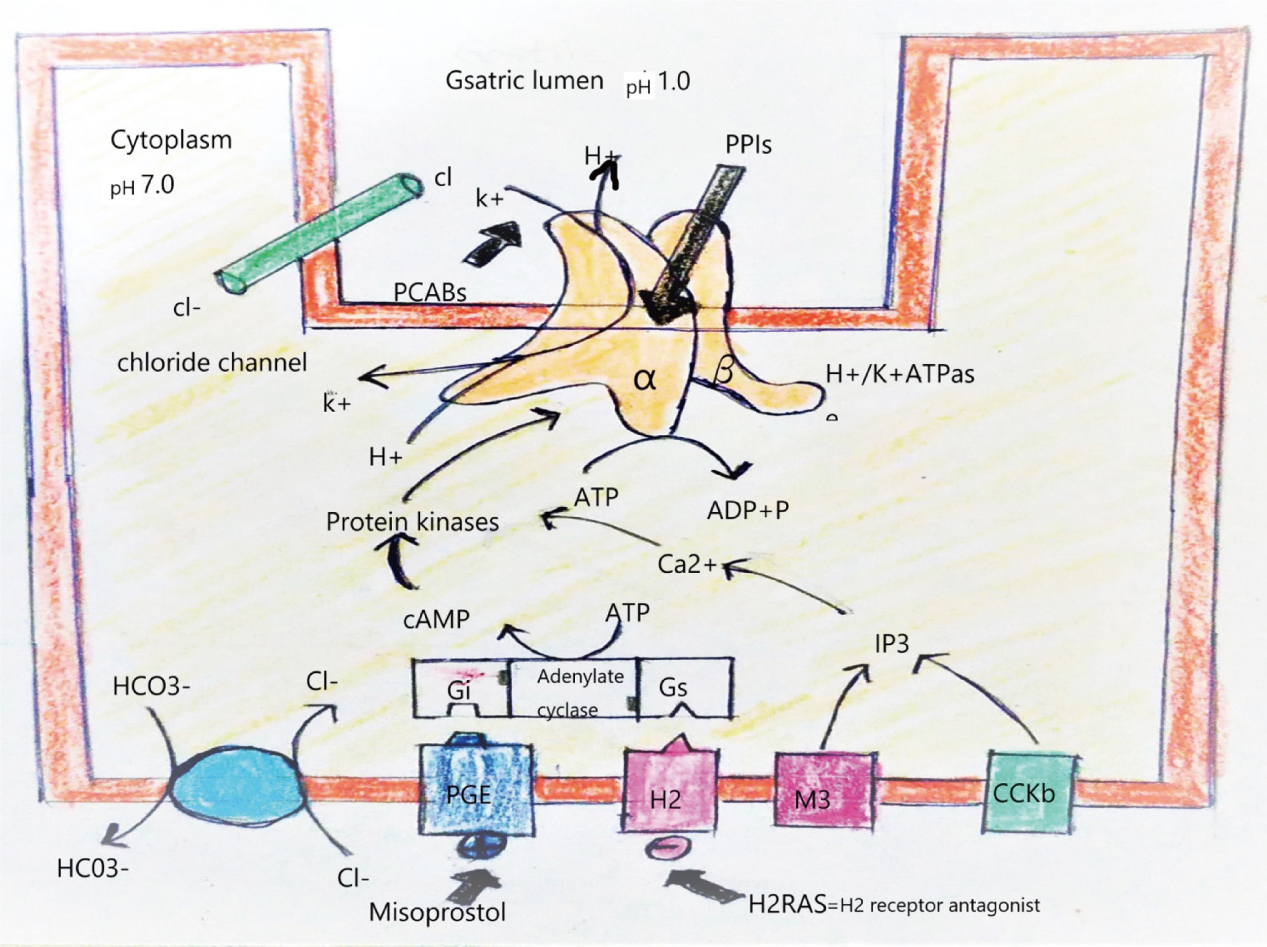
在胃的壁細胞內二氧化碳和水通過碳酸酐酶形成碳酸,碳酸解離產出H+離子和HCO3-離子,HCO3-離子在細胞基底側與Cl-離子交換使Cl-離子進入到壁細胞中。質子幫浦的α和β亞基在高基氏體(Golgi)中生成和組裝並在非進食時儲存在管泡中。進食後,壁細胞基底外側的乙醯膽鹼(acetylcholine)透過迷走神經和腸神經系統的副交感神經活動刺激M3乙醯膽鹼受體( M3 receptors),而胃泌素(gastrin)刺激膽囊收縮素B受體(CCK2 receptors),並透過三磷酸肌醇 (IP3) 刺激 Ca2+離子產出,Ca2+離子可促進胃竇部釋放胃泌素也可參與壁細胞的胃酸分泌作用。組織胺刺激H2 受體後透過G蛋白(Gs)刺激腺苷酸環化酶產生環狀AMP (cAMP),而前列腺素E(prostaglandin E)會產生一種抑制性G蛋白(Gi)來阻斷這種作用。Ca2+和cAMP 濃度升高導致蛋白激酶 A(protein kinase A)升高,蛋白激酶A可將參與質子幫浦從細胞質轉運至細胞膜的蛋白質磷酸化,增加壁細胞活化期間質子幫浦在分泌小管(secretory canaliculus)腔側的數量,並在去活化期間將其移除。質子幫浦可轉運 H+離子穿過小管膜以換取K+離子進入小管中,同時伴隨著Cl-離子的被動運輸穿過頂膜,最終形成 HCl 並保持電化學中性。質子幫浦的α亞基有10個跨膜結構域,排列成允許排出H+離子以換取K+離子進入的管道其上並有ATP 的結合位點,以提供此活動過程所需的能量。β亞基是單個跨膜結構域,推測是用來使質子幫浦插入和定位在分泌小管膜內,並確保H+離子的單向流動。PPI 和PCAB會阻止酸生產的最後一步。 PPI 透過與位於α亞基的跨膜結構域4和5上的半胱氨酸(cysteine)部分發生不可逆的共價結合,PCAB透過與小管中 K+離子的可逆性離子競爭作用來抑制H+離子的分泌,如圖一6。
圖一 胃酸分泌與質子幫浦及PCABs作用示意圖6。
肆、GERD的藥物治療
NERD患者經24小時食道酸鹼值檢查呈陽性反應則建議先服用PPI 4-8 週。EE患者同樣先服用 PPI 治療4-8週,之後視病患情況可採用降階(step down)療法,例如使用半劑量的PPI或H2受體拮抗劑、促胃腸蠕動藥或 鋁鎂制酸劑。也可用間歇(intermittent)療法,短期治療約2-3週後停藥,再視症狀恢復短期連續治療。或是用需求(on demand therapy)療法,病人出現GERD 症狀即服用一顆 PPI,症狀未改善者則持續(maintenance therapy)治療,無症狀者則停藥。逆流性食道炎患者如果以 PPI 治療無效,可以考慮加倍劑量 ,若加倍劑量治療仍然無效,則視臨床狀況決定後續檢查及治療。經 PPI 治療有效,停藥後症狀再度復發則建議回復 PPI 治療 4-8 週。Barrett 氏食道患者則依個案決定治療及追蹤方法7。
伍、GERD治療藥物簡介
一、 鋁鎂制酸劑(Antacids) 及海藻酸(Alginic acid)
氫氧化鋁中和胃中的鹽酸鹽形成 Al (Cl)3 和 H2O,導致胃 pH 值升高和胃蛋白酶活性受到抑制。 鎂鹽也具有相似的藥理作用。 海藻酸是一種天然多醣聚合物,在與胃酸接觸數分鐘內沉澱成 pH 值接近中性的低密度粘性凝膠。 pH值的變化觸發配方中的碳酸氫鈉釋放二氧化碳,二氧化碳被困在藻酸鹽凝膠中,使其可在胃中的食物表面形成高pH值的泡沫保護層,防止胃酸逆流至食道黏膜,兩者與食物一起服用藥效較佳8。
二、H2受體拮抗劑
作用在胃壁細胞上的H2受體進而減少胃酸分泌,與食物併服並不影響吸收,但若與制酸劑併服則可能減少一到二成的吸收,建議間隔一至二小時。患者若長期服用會因壁細胞內 cAMP濃度由其他途徑上升因此產生耐受性(tolerance)而失效。停藥後會因H2受體向上調節(up regulation)而引起胃酸反彈。其抑制夜間胃酸分泌效果較好乃因夜間組織胺分泌較多,若治療白天因進食而引起的胃酸分泌過多則表現適中。一般的處方劑量約可以減少五成的胃酸分泌達10 小時,所以一天需服用兩次較佳8,9。
三、質子幫浦抑制劑
PPIs基本化學構造是benzimidazole及pyridine環,屬於前驅藥物(prodrug),藥物本身為弱鹼性容易被胃酸破壞因此多製成腸溶劑型。具親脂性可以快速的通過胃的壁細胞膜進入且聚集在高度酸性的分泌小管。benzimidazole及pyridine環上的N與氫離子結合成為Sulphonamide才成為活性藥物,可與被高濃度酸激發而移至分泌小管膜上的質子幫浦之α亞基之半胱氨酸(Cysteine)以雙硫共價鍵結合,進而不可逆地破壞具有活動性的質子幫浦減少胃酸分泌9。PPIs 抗胃酸分泌的功效取決於壁細胞管狀空間中活化的質子幫浦數量。大多數的 PPIs應該於餐前 30-60 分鐘服用以便有時間全身吸收。PPIs的血漿半衰期大約只有 1-2 小時作用持續時間很短,且壁細胞酸分泌處最多只能同時容納75%數量的質子幫浦,因此若在PPIs血漿半衰期過後繼續進食,可能就會失去抑制胃酸分泌的能力,通常服用3-5天後達到藥效穩定。某些PPIs會競爭性抑制肝臟酵素CYP2C19的代謝,尤其對CYP2C19藥物遺傳學多態性(pharmacogenetic polymorphism)患者,常會導致這類患者服用clopidogrel 時無法完全代謝成活性型6。
四、鉀離子競爭性酸抑製劑
位於壁細胞分泌小管處的質子幫浦呈現E1 構象,對細胞質內的H+具有高親和力,當與 H+ 結合後,質子幫浦經由ATP驅動發生三向構象而成為磷酸化的E2構象(E2P), E2P對分泌小管腔外的K+ 離子具有高親和力,它和K+ 離子結合後會去磷酸化而回復成E1 構象並將K+ 離子運回細胞質內,如此循環的重複讓酸不斷分泌。它們作用於質子幫浦無論其是否處於活化或不活化狀態10。vonoprazan是一種PCAB,這類藥品還有 revaprazan、 tegoprazan、fexuprazan,PCAB與質子幫浦結合後,由於其分子較大,因此阻礙了 K+離子的結合位點,而不是直接佔據K+離子結合位點,藉由和 K+離子的可逆性離子競爭作用來抑制H+離子的分泌。目前台灣只核准vonoprazan使用,可用來治療糜爛性食道炎、胃潰瘍或十二指腸潰瘍或與其他抗生素併用治療幽門螺旋桿菌引起的感染。通常成人每日一次口服一顆 20 mg。vonoprazan因為pKa 值較高所以在酸性環境中較穩定,不限定餐前服用且可蓄積在壁細胞內部,且其不像PPIs需要H+才可活化,口服後可在2小時內達到最大血中濃度。禁食狀態的血漿半衰期約為7小時,食物對其吸收的影響很小。與其他 PCAB相比,vonoprazan從質子幫浦中解離得更慢,因此有較長的作用時間。vonoprazan 的有效性不受肝臟酵素 CYP2C19 狀態的影響6。在日本和英國的 I 期臨床試驗中首次給予健康受試者服用vonoprazan 40 mg,給藥後胃內達到 pH > 4.0平均約4 小時,抑制胃酸作用可持續24 小時。連續 7 天服用 vonoprazan 40 mg 後,胃中酸度持續維持pH >5的試驗者 比率為100%11。
陸、vonoprazan與PPIs的藥效比較
在日本一個隨機非盲性的研究中比較vonoprazan 20 mg和esomeprazole 20 mg及rabeprazole 10 mg每天服用一次連續七天來觀察胃中pH的變化。vonoprazan:esomeprazole =6.1:4.7,vonoprazan:rabeprazole =6.5:4.8。vonoprazan 組胃內 於24 小時pH 值保持在 4 以上的試驗者有 85.8%。在白種人的受試者中,vonoprazan 20 mg,每天一次持續 7 天,pH 值維持在 4以上者有85.3%,維持在 5 以上有78.6%6。治療中不良事件發生率lansoprazole 15 mg:vonoprazan 10 mg : vonoprazan 20 mg =11.4%:10.4% :10.3%其中鼻咽炎是最常出現的不良事件。對 PPI 治療無效的糜爛性食道炎患者使用vonoprazan 10或 20 mg 每天一次於24 小時能夠維持胃內 pH 值高於4達到 96%-100% 。vonoprazan 20 mg 和 lansoprazole 30 mg 一天一次對心灼熱一天即可改善的比率為31%比12% 6。在日本的研究中,它們採用lansoprazole 30 mg 或 vonoprazan 20 mg + amoxicillin 750 mg + clarithromycin 200 mg 或400 mg(lac組:vac組)一天兩次服用七天來比較幽門螺旋桿菌的清除率,結果vac組:lac組為92.6%(95% 信賴區間為89.2-95.2%):75.9%(95%信賴區間為70.9-80.5%),顯示vonoprazan 不劣於lansoprazole。在另一項隨機控制實驗中針對clarithromycin 有抗藥性的幽門螺旋桿菌的清除率使用lansoprazole比上 vonoprazan組為:40.0% :82.0%。vonoprazan 並無抗幽門螺旋桿菌的活性 最主要的機制還是在於強制抑制胃酸分泌的作用。幽門螺旋桿菌適宜生長於pH 6~8之間,而以細菌蛋白質為靶點的抗生素,如amoxicillin和clarithromycin在此pH值範圍可以有更高的靈敏度11。另外研究也指出若將抗生素clarithromycin換成二線的metronidazole或三線的 sitafloxacin則療效無統計上的差異,可能的原因在於這些抗生素殺菌的機轉不依賴於細菌的細胞分裂11。
柒、結論
研究指出vonoprazan和PPIs比較在胃潰瘍或食道炎等方面都有不劣性甚至更好的療效,但長期強度抑制胃酸分泌所造成的高胃泌素血症可能造成的癌前病變及胃酸過少的疑慮加上目前該藥價格較貴等問題,使得該藥目前普及率不高,但基於其作用速度快持續時間長的特性,相信在不久後定可以成為這些疾病治療的另一種選擇。
New Development of Drugs for Gastroesophageal Reflux
Wen-Tsung Liau1, Min-Ling Tsai2
1Chung Shan Medical University Hospital
2Chung Shan Medical University
Abstract
Eating habits and living stress have increased the incidence of gastroesophageal reflux and gastric ulcers. Current treatment methods are aimed at reducing gastric acid secretion to improve symptoms, except for early aluminum-magnesium antacids, H2 receptor antagonists and proton pump inhibitors. In addition, vonoprazan is a potassium-competitive acid blockers (P-CABs) , which has been shown to be non-inferior to proton pump inhibitors, and has a fast action time and a long duration.It will not competitively inhibit the metabolism of the liver enzyme CYP2C19 and cause drug interaction, which can be used as a new choice for the treatment of hyperacidity and other related diseases.
參考資料:
1. 林弘恩、林毅軒、羅景全:鉀離子競爭性酸抑制劑對胃酸相關疾病的療效。臨床醫學月刊2019;83(4):250-253。
2. Gastroesophageal reflux disease. (2022, May 22). In Wikipedia. https://en.wikipedia.org/wiki/Gastroesophageal_reflux_disease
3. 廖思嘉、葉宏仁、柯忠旺等: 胃食道逆流疾病之處置現況。內科學誌2010;21(6): 381-390。
4. 洪培原:藥物引起之胃食道逆流介紹。台中慈濟藥訊2019;08:2-7。
5. 郭昭宏: 淺談胃食道逆流疾病及其治療。高雄醫師會誌2012;20(4):354-359 。
6. Abdel-Aziz, Y., Metz, D. C., Howden, C. W. (2021). potassium-competitive acid blockers for the treatment of acid-related disorders. Alimentary Pharmacology & Therapeutics, 53(7), 794-809.
7. 台灣消化系醫學會: 胃食道逆流疾病治療共識(2007)。http://www.gest.org.tw/meeting/content.php?type=&id=1&pageNo=1&continue=Y
8. 李敏慈:胃藥分類及機轉說明。永信藥訊2018。https://www.ysp.com.tw/tw/magazine/1129
9. 林淳榮:胃酸相關胃腸疾病之最新診治新進展。內科學誌2015;26(3),123-132。
10. Echizen, H. (2016). The first-in-class potassium-competitive acid blocker, vonoprazan fumarate: pharmacokinetic and pharmacodynamic considerations. Clinical Pharmacokinetics, 55(4), 409-418.
11. Kiyotoki, S., Nishikawa, J., Sakaida, I. (2020). Efficacy of vonoprazan for Helicobacter pylori eradication. Internal Medicine, 59(2), 153-161.
通訊作者:蔡敏鈴/通訊地址:台中市南區建國北路一段110號藥劑科
服務單位:中山醫學大學/聯絡電話:(O) 04-24739595 ext 20167