Vancomycin血中濃度治療監測新觀念
羅紫勻1、盧志魁1、陳惠玉1、蕭旋玲1,2
1林口長庚紀念醫院藥劑部、2長庚大學呼吸治療學系
摘要
臨床上熟知的vancomycin為治療methicillin-resistant
Staphylococcus aureus (MRSA)
感染症的首選藥物之一,然而因為其治療指數狹窄,必須監測血中濃度以避免藥物過度暴露而造成腎損傷或耳毒性。美國衛生系統藥劑師協會與美國感染症醫學會於2020年5月發表新版vancomycin治療監測指引,以AUC/MIC
400-600
mg*h/L取代以往的血中波谷濃度作為監測參數,本文介紹兩種計算方式:Bayesian方法及兩濃度梯形計算法(2-level
calculated trapezoidal
method)供臨床照護人員參考,並討論持續輸注及特殊族群(兒科、肥胖、腎臟替代療法病人)之注意事項,以期更全面的臨床指引能提升病人用藥的有效性及安全性。
關鍵字: vancomycin、AUC/MIC、血中濃度監測
壹、 前言
Vancomycin於1952年在美國婆羅洲的密西西比泥土中被分離出來,1958年正式取得美國FDA核准於臨床運用。Vancomycin常見的副作用包括皮疹、快速輸注引發的red
man syndrome、耳毒性及腎毒性等,為確保vancomycin治療的有效性及安全性,臨床上建議進行血中濃度監測,2009年發布的血中濃度監測指引1,根據藥物動力學/藥效學
(pharmacokinetic/ pharmacodynamics,PK/PD)
方程式計算出之area under the curve over minimum
inhibitory concentration ratio (AUC/MIC) 作為監測vancomycin療效的參數,但以血中波谷濃度
(serum trough concentration) 15-20 mg/L做為AUC/MIC
>400 mg*h/L的替代目標。然而,近年研究發現,欲使波谷濃度達到15
mg/L,通常需要每天給予超過3g的劑量,其AUC之暴露也因此超越600 mg*h/L2。考量目前之實證,美國感染症醫學會與其他學會於2020年共同修訂並發表新版vancomycin血中濃度治療監測指引3,以AUC/MIC作為有效性及腎毒性的參數,並新增持續輸注及特殊族群(兒科、肥胖、腎臟替代療法病人)之使用建議,以下將簡介vancomycin血中濃度監測新觀念。
貳、 指引修訂
新版指引支持針對使用vancomycin治療嚴重MRSA感染之病人進行AUC/MIC監測,且於使用經驗性療法之大部分情況下,須假設其MRSA菌株的minimum
inhibitory concentration (MIC)為1 mg/L,而臨床上大部分MRSA菌株(95.1%)的MIC
≤1 mg/L4。值得注意的是,vancomycin不適用於治療MIC大於1mg/L的MRSA菌株,當vancomycin用於MIC大於1
mg/L的MRSA菌株時,若要達到AUC/MIC ≥400 mg*h/L,其所須的vancomycin劑量可能大於常規劑量,因此可能增加腎毒性之風險。此外,腦膜炎、泌尿道感染和皮膚及軟組織感染(後兩者屬非嚴重MRSA感染)缺乏實證,因此不適用新版指引(見表一)5。針對所有可能發生腎毒性高風險病人(如目前正同時使用具腎毒性藥品之重症病人)、腎功能狀態不穩定(惡化及急遽改善)及接受大於3至5天治療的病人,須進行vancomycin血中濃度監測,而監測頻率應以臨床判斷為依據,血液動力學不穩定之病人,建議可每天進行監測,若為血液動力學穩定者,則建議一周監測一次為原則。
表一、Vancomycin用於嚴重MRSA感染時治療監測指引之適應症及對應監測指標5

一、 成人監測指引
2020監測指引,重點仍然放在AUC/MIC≥400 mg*h/L(MIC由BMD確定),是目前公認關鍵的PK/PD參數,也是避免金黃色葡萄球菌產生耐藥性的主要方法。越來越多實證指出過高的波谷濃度、極端的給藥劑量及過高的AUC與急性腎損傷
(acute kidney injury,AKI) 之間的關聯性。van Hal SJ等人的meta-analysis指出:高於600
mg*h/L的AUC/MIC與波谷濃度>15mg/L相較,有更高的AKI風險性,證明AKI與vancomycin暴露有直接關聯2,因此,為了改善病人腎功能相關的預後,是將監測指標由波谷濃度轉為AUC的主要因素。
二、 速效劑量
速效劑量在2020監測指引中的劑量範圍更廣,由原本的25-30 mg/kg改為20-35
mg/kg,輸注時建議將vancomycin稀釋至<5mg/mL之濃度,輸注時間>60分鐘或輸注速率<10-15mg/min以降低red
man
syndrome發生的風險,而給予速效劑量25-35mg/kg時,宜將輸注時間延長為2-3小時6。對於重症病人,至關重要的是迅速達到血液中vancomycin的目標濃度,以降低治療效果延緩所造成之風險,建議依其實際體重
(actual body weight,ABW)給予每小時至多1g作為速效劑量,但不得超過3g。針對肥胖族群,因分布體積(volume
of distribution,Vd)會隨著體重增加而減少,建議以ABW作為計算速效劑量之基準,其速效劑量為20-25
mg/kg,劑量上限為3g7,維持劑量則是以每日4.5g為上限,當超過每日4g時,須密集監測AUC。
三、 持續輸注
持續輸注是2020年vancomycin監測指引的新領域,當目標AUC無法達成時,可替代傳統間歇給藥方式,且於穩定狀態濃度15-25 mg/L及波谷濃度10-20 mg/L時,其腎毒性風險小於間歇性給藥方式8。AUC的計算在這種情況下比其他方法更簡單,以目標濃度為20-25 mg/L為例,乘以一天24小時,等於濃度-時間曲線下從0到24小時(AUC0-24h)/MIC為480-600 mg*h/L,建議以速效劑量15-20 mg/kg,每日維持劑量30-40 mg/kg,最高至60 mg/kg以達到穩定狀態濃度為20-25 mg/L。連續輸注為難以達到治療濃度或需要比預期更高劑量的病人提供了一種用藥選擇,然而,這代表需要在病人身上建立專用的vancomycin獨立給藥管路,臨床上須衡量其必要性。
四、 腎臟替代療法
Vancomycin於腎功能正常之病人建議劑量為15-20
mg/kg*Q8H-Q12H,關於腎臟替代療法,指引詳細介紹了間歇性血液透析
(intermittent hemodialysis,IHD)、混合型血液透析(hybrid
hemodialysis) 和連續性腎臟替代療法(continuous renal
replacement therapy,CRRT)之影響劑量/監測的具體方式。更新內容包括對於使用vancomycin的洗腎族群,應進行濃度監測,透析前血中濃度維持15-20
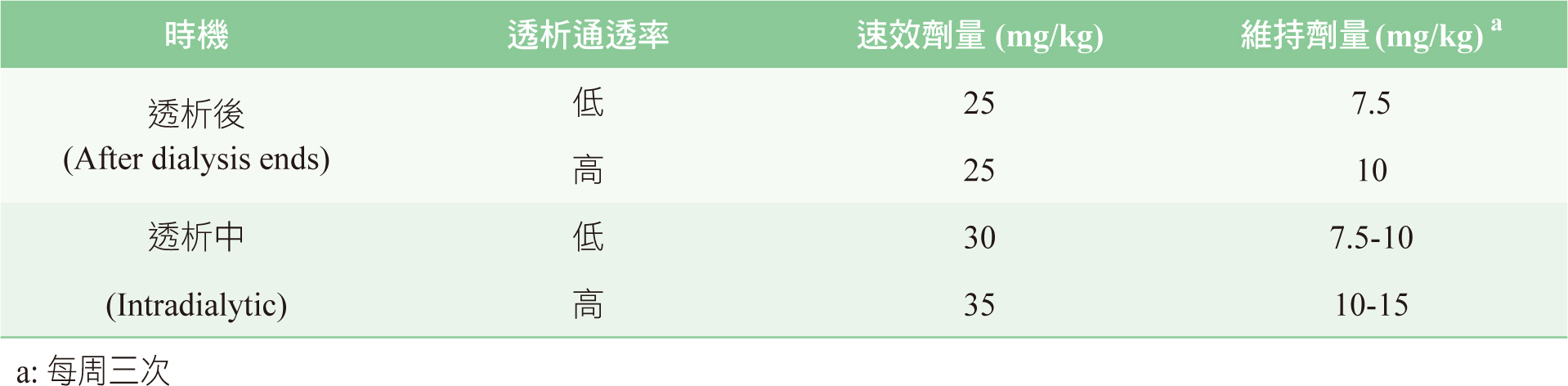
mg/L時,預期可以確保AUC0-24h落於400-600mg*h/L,而速效劑量及維持劑量,按照給藥時間及不同透析膜通透度而有所不同(見表二),以期AUC/MIC可達到400-600
mg*h/L之目標9。若為混合型血液透析,應給予速效劑量20-25
mg/kg,並於洗腎結束前60至90分鐘或是結束後給予維持劑量15 mg/kg。CRRT之病人建議給予速效劑量為20-25
mg/kg,維持劑量為7.5-10 mg/kg
*Q12H。對於洗腎病人需密切監測腎臟替代流速(renal replacement flow
rate),因為這等同於病人的肌酸酐清除率(creatinine
clearance),並且應常規安排vancomycin監測,以確保用藥安全性。
表二、間歇性洗腎病人之劑量建議3
對於兒童族群,Fiorito TM等人的meta-analysis結果指出,當病童的vancomycin波谷濃度>15
mcg/mL時,急性腎損傷發生率增加了2.7倍10。另有回顧性文獻顯示,波谷濃度的監測造成AKI發生機率更高,但波谷濃度與AUC監測相比之療效並無顯著差異,因此建議兒科和新生兒的劑量應該以AUC/MIC
400-600 mg*h/L為目標。根據AUC/MIC,建議經驗性給予維持劑量,對於3個月以上的兒童,以60-80
mg/kg/day,Q6H投予,對於12歲以上的兒童則以60-70
mg/kg/day,Q6H-Q8H投予,此外,速效劑量的部分目前尚未有完整的研究佐證。
參、 AUC0-24h /MIC計算方式
針對AUC0-24h/MIC計算,指引中提供了兩種方法,以軟體計算的Bayesian方法(指引推薦)及使用分析PK方程式的兩濃度梯形AUC計算法
(2-level calculated trapezoidal
method),此兩種方法相關比較整理如表三。Bayesian方法是透過模型更加精準地估算及預測某一段時間內的藥物暴露,利用病人族群給予vancomycin後血中濃度變化建立的PK模型及相關PK參數(如:Vd、清除率)作為Bayesian資料庫
(a priori),而後,將特定病人血中濃度與資料庫預估數值比較,並為病人的AUC、Vd和清除率等PK參數之計算進行修正,即為輸出值
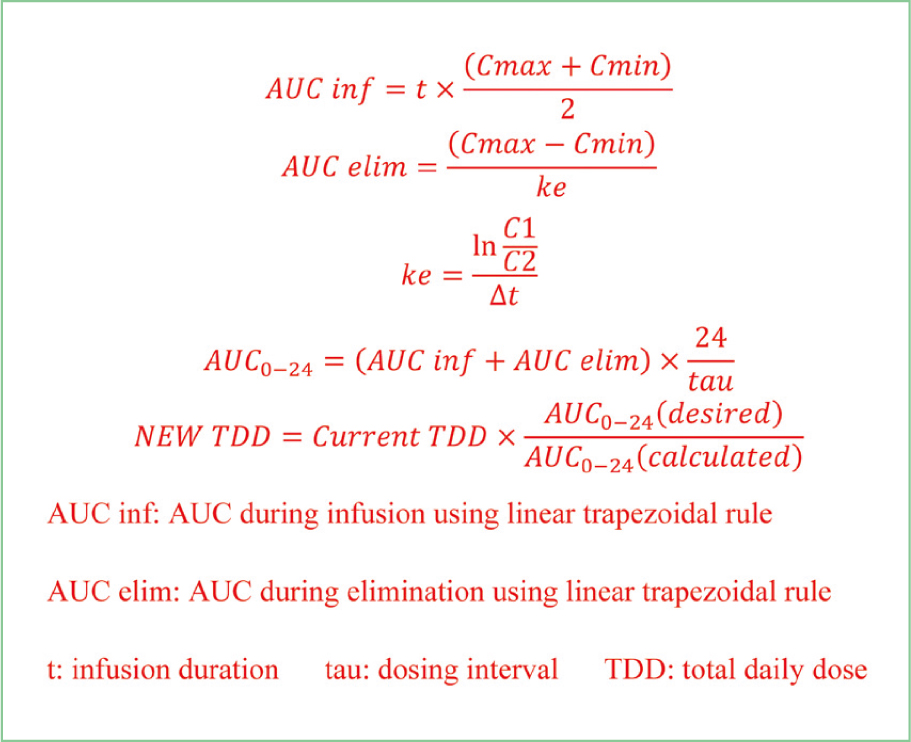
(a posterior),臨床上可利用輸出值結果估算及預測達到目標AUC所需的劑量及給藥間隔,進而擬定特定病人的專屬給藥計畫。Bayesian方法與兩濃度梯形AUC計算法間最大的差異在於抽血時間及所需的抽血次數,我們較為熟悉的兩濃度梯形AUC計算方法,須待血中藥物濃度處於穩定狀態後(給予4個劑量後)連續抽兩次濃度
(peak及trough
level),再利用以下公式(圖一)運算。Bayesian方法則不須於特定時間抽血,且可僅取一個血中濃度就足夠得到AUC估算值,若能取兩個濃度(注射後1至2小時濃度及波谷濃度)則是最準確的,但特定族群(如:肥胖、兒童及加護病房病人)不完全適合以單一濃度進行Bayesian方法計算,指引中仍建議應抽取兩個抽血點的血中濃度以確保準確性,另外,雖然Bayesian方法可用一個濃度就估算出AUC,但若是缺乏其他附近時間點的數據,仍建議以波峰/波谷濃度作為標準。實施以Bayesian方法為基礎的vancomycin給藥策略無疑提升臨床工作者的工作效率,不須等待穩定狀態就可抽血檢測的特性成為最主要的優勢,但必須編列預算購買軟體,人員也需經過教育訓練熟悉軟體操作,目前商用軟體收錄族群皆以西方國家族群之PK數據為主,尚未出現以亞洲族群資料庫建立的模型,因此需要考量無法正確反應準確之預測濃度的可能性,若能克服上述限制,正確使用軟體、結合電子健康資訊系統與快速完成數據輸入和輸出能帶來更大的效益。而兩濃度梯形AUC計算方法,由於需要在特定時間抽血,對於臨床工作者而言,花費的時間成本較高,但因為臨床人員行之有年熟悉操作,且不須額外付出購買軟體成本,是目前多數醫院仍使用此方法的原因。
表三、兩種計算AUC公式之優點比較3
圖一 兩濃度梯形計算方法公式
(2-level calculated trapezoidal method)
肆、 討論
2020年新版指引相較2009年舊版指引提供了更加明確的vancomycin臨床治療建議,其中最重大的變革是藥物監測指標由波谷濃度改為以AUC作為評估依據,即使在舊版指引中就曾提及以AUC/MIC做為評估參數可獲得最佳臨床效果,但考量波谷濃度取得更加直接及精確,當時認為在MRSA
MIC≤1 mg/L的前提下,波谷濃度在15-20mg/L時,可望達到AUC/MIC≥400
mg*h/L之目標,相較於須抽取2個以上血中濃度進行計算的AUC方式,最終因其方便性,以波谷濃度為替代指標作為最終共識。然而,N.E.
Holmes針對以AUC/MIC作為vancomycin監測指標的討論,提及不論菌株種類、感染症種類、年齡及AUC或MIC檢測方式之差異,目前證據顯示AUC/MIC尚未能預測臨床治療成效,因此,根據藥物動力學理論支持AUC/MIC為最佳vancomycin監測指標,但是否廣泛應用仍須斟酌11。雖然於預測治療效果層面未得到理想結果,但目前研究數據顯示,AUC/MIC監測可減少抽血次數及每日vancomycin的劑量,相較於以波谷濃度監測的情況下,更能減少腎毒性的發生12-13。以AUC/MIC評估病人的臨床結果,易受其他不可測量因素影響,如:共病症、抗生素與病原體於感染部位的作用,因此很難定義治療結果成功是完全源於適當的抗生素劑量,但最重要的是決定劑量的同時必須考量療效及毒性的平衡,為病人「客製化」適當療程,精準監控病人的用藥情形,歸功於現今已有商業軟體可進行快速的AUC計算,讓臨床人員可不僅及時,甚至預先進行給藥計畫的調整,同時也期待能建立亞洲甚至台灣族群的PK資料作為研發軟體的基礎,更精準地預測AUC,造福台灣的病患。
此外,相較舊版訂定之vancomycin適應症,目前因無足夠證據以提供臨床建議的AUC治療區間,故將腦膜炎排除,並於新版首次提供腎功能不全、肥胖病人及小兒之治療及監測建議。Vancomycin使用以重症病人為大宗,其中部分病人伴隨腎功能不全,制定不同血液透析方法下,對洗腎病人療效監測及安全性提供建議,亦能進而穩定重症病人的病況。速效劑量及持續輸注亦是vancomycin新版的重要發展,針對需短時間達到治療濃度及難以達到治療目標的病人,補足間歇性給藥模式無法兼顧之處。無論是監測指標的改變、給藥對象狀態或是給藥模式建議,都確實將vancomycin使用安全性大幅提升(表四)。
表四、Vancomycin 血中濃度監測指引之比較
伍、 結論
以AUC/MIC作為vancomycin監測依據的時代已經來臨,AUC的計算方式各有優劣,但不論是新興的軟體運算或是舊有計算公式都可做為臨床調整給藥模式的參考。此外,指引新增針對特定族群及給藥方式的相關建議,讓臨床工作者可以有依據的進行綜合評估,病人的用藥得以兼顧療效及安全性,對於臨床工作人員及病人都是一大福音。
Updating Consensus of Vancomycin Therapeutic
Drug Montoring
Tzu-Yun Lo1, Chih-Kuei Lu1, Hui-Yu Chen1, Hsuan-Ling
Hsiao1,2
1Department of Pharmacy, Linkou Chang Gung
Memorial Hospital
2Department of Respiratory Therapy, Chang Gung
University
Abstract
Vancomycin is one of the well-known drugs of
choice for the treatment of severe methicillin-resistant
Staphylococcus aureus (MRSA) infection in
clinical settings. However, because of its
narrow therapeutic index, therapeutic drug
monitoring should be warranted to avoid kidney
injury and ototoxicity due to overexposure. The
American Society of Health-System Pharmacists
and American Society of Infectious Diseases
released a updated concesus guideline for
therapeutic monitoring of vancomycin for serious
ORSA infection in May 2020 and switched serum
trough level to AUC/MIC 400-600 mg*h/L as the
optimal monitoring target. Two calculation
methods were introduced in this article: the
Bayesian method and the 2-level calculated
trapezoidal method and focused on continuous
infusion and precautions with special
populations (pediatrics, obesity, and patients
with renal replacement therapy), in the hope
that this clinical comprehensive guideline can
improve the efficacy and safety for patients'
therapy.
參考資料:
1. Rybak MJ, Lomaestro BM, Royschafer JC, et al.
Therapeutic monitoring of vancomycin in adult
patients: a consensus review of the American
Society of Health-System Pharmacists, the
Infectious Disease Society of America, and the
Society of Infectious Diseases Pharmacists. Am J
Health Syst Pharm. 2009;66(1):82-98.
2. van Hal SJ, Paterson DL, Lodise TP.
Systematic review and meta-analysis of
vancomycin-induced nephrotoxicity maintain
troughs between 15 and 20 miligrams per liter.
Antimicrob Agents Chemother. 2013;57(2):734-744.
3. Rybak MJ, Le J, Lodise TP, et al. Therapeutic
monitoring of vancomycin for serious methicillin-resistant
Staphylococcus aureus infections: A revised
consensus guideline and review by the American
Society of Health-System Pharmacists, the
Infectious Diseases Society of America, the
Pediatric Infectious Diseases Society, and the
Society of Infectious Diseases Pharmacists. Am J
Health Syst Pharm. 2020;77(11):835-864.
4. Diaz R, Afreixo V, Ramalheira E, et al.
Evaluation of vancomycin MIC creep in
methicillin-resistant Staphylococcus aureus
infections- a systematic review and
meta-analysis. Clin Microbiol Infect.
2017;24(2):97-104.
5. Boisson C, Arnaud S, Vialet R, et al. Severe
community-acquired meningitis. Crit
Care.1999;3(4):R55-R65.
6. Roberts JA, Taccone FS, Udy AA, et
al.Vancomycin dosing in critically ill patients:
robust methods for improved continuous-infusion
regimens. Antimicrob Agents Chemother.
2011;55(6):2704-2709.
7. Grass RL, Dunn R, Hong J, et al. Dosing
vancomycin in the super obese: less is more. J
Antimicrob Chemother. 2018;73(11):3081-3086.
8. Saugel B, Nowack MC, Hapfelmeier A, et al.
Continuous intravenous administration of
vancomycin in medical intensive care unit
patients. J Crit Care. 2013;28(1):9-13.
9. Chaijamorn W, Jitsurong A, Wiwattanawongsa K,
et al. Vancomycin clearance during continuous
venovenous haemofiltration in critically ill
patients. Int J Antimicrob Agents.
2011;38(2):152-156.
10. Fiorito TM, Luther MK, Dennehy PH, et al.
Nephrotoxicity with vancomycin in the pediatric
population: a systematic review and
meta-analysis. Pediat Infect Dis J.
2018;37(7):654-661.
11. N.E. Holmes. Using AUC/MIC to guide
vancomycin dosing: ready for prime time? Clin
Microbiol Infect. 2020;26(4):406-408.
12. Neely MN, Kato L, Youn G, et al. Prospective
trial on the use of trough concentration versus
area under the curve to determine therapeutic
vancomycin dosing. Antimicrob Agents Chemother.
2018;62(2):e02042-17.
13. Finch NA, Zasowski EJ, Murray KP, et al. A
quasi-experiment to study the impact of
vancomycin area under the concentration-time
curve-guided dosing on vancomycin-associated
nephrotoxicity. Antimicrob Agents Chemother.
2017;61(12):e01293-17.
通訊作者:蕭旋玲/通訊地址:桃園市龜山區復興街5號-臨床藥學科
服務單位:林口長庚紀念醫院藥劑部/聯絡電話:(O) 0975367862