淚膜為導向精準化治療乾眼症
陳玟璇、鄭雅庭、黃微瑄、鄧祥邦、蕭惠娟
高雄市立大同醫院藥學科
摘要
乾眼症(dry
eye)是一種多因素疾病,其特徵為淚膜不穩定所導致視覺障礙和眼睛表面受損。而眼睛角膜表面的淚膜層(tear
film)和上皮組織層(epithelium)若其中成分不足或功能障礙皆會影響淚膜之穩定性。因此,近幾年亞洲乾眼症學會提出以淚膜導向診斷(tear-film
oriented diagnosis, TFOD)和淚膜導向治療(tear-film
oriented therapy, TFOT)乾眼症之新概念。依據淚膜導向診斷將乾眼症進一步分為三種類型:蒸發過強型(increased
evaporation)乾眼症、缺水型(aqueous-deficient)乾眼症和濕潤度下降型(decreased
wettability) 乾眼症,且分別對應眼睛角膜表面各層之不足或異常:
脂質層/分泌黏蛋白,水層,膜相關黏蛋白/上皮細胞層。淚膜導向治療為針對各層成分之異常情形給予相對應之治療,用以重建穩定之淚膜結構和功能,對於蒸發過強型乾眼症建議給予含脂眼藥水、Diquafosol
sodium和Rebamipide;缺水型乾眼症建議給予人工淚液、玻尿酸和Diquafosol
sodium;濕潤度下降型乾眼症建議給予Diquafosol sodium、Rebamipide、表皮生長因子(epidermal
growth factor, EGF)和自體血清眼藥水。以淚膜為導向診斷與治療乾眼症提供未來更精準化之治療策略。
關鍵字: dry eye、tear-film oriented therapy (TFOT)、artificial
tears、diquafosol sodium、rebamipide、epidermal
growth factor (EGF)
壹、乾眼症定義與分類
根據2019年淚膜與眼球表面學會(Tear Film & Ocular Surface
Society, TFOS)最新的研究報告,有症狀(symptoms)和無症狀(asymptoms)乾眼症之全球盛行率為5-50%,且隨年齡增長而增加、女性大於男性、亞洲族群大於歐美族群。乾眼症常見症狀為眼睛紅腫、乾澀、搔癢、流眼淚、分泌物黏稠和角膜上皮病變,更嚴重則會影響視力。
乾眼症之定義和診斷根據2017年亞洲乾眼症學會(Asia Dry Eye Society,
ADES)共識,「乾眼症為一種多因素疾病,其特徵為淚膜不穩定導致各種症狀和/或視力損傷,並可能伴有眼睛表面受損1」。眼睛角膜表面由淚膜層(tear
film)和上皮組織層(epithelium)所組成用以維持淚膜穩定性,而淚膜層又包含脂質層(lipid
layer)、水層(aqueous layer)和分泌黏蛋白(secretory mucin);上皮組織層包含膜相關黏蛋白(membrane
associated mucins)和上皮細胞層(epithelial
cells),在這些結構中,若有其中一層成分不足或功能障礙皆會影響淚膜穩定性和進而導致乾眼症。因此,目前亞洲乾眼症學會(ADES)基於以淚膜導向診斷之新概念,將乾眼症分為三種類型:蒸發過強型(increased
evaporation)乾眼症、缺水型(aqueous-deficient)乾眼症和濕潤度下降型(decreased
wettability)乾眼症。
一、蒸發過強型乾眼症
為脂質層或分泌黏蛋白成分不足或異常所導致,其代表性和相關性疾病為縮短淚膜破裂時間(short-break-up
time, S-BUT)型乾眼症、瞼板腺功能障礙(Meibomian gland
dysfunction, MGD)、抑制眨眼。
二、缺水型乾眼症
為水層成分不足所導致,根據淚膜代償性理論,缺水性乾眼症可能伴有非常厚的脂質層用以代償水層的不足,其代表性疾病為修格蘭氏症候群(Sjogren's
syndrome)、移植物對抗宿主疾病(chronic graft-versus-host
disease, cGVHD)和瘢痕性類天皰瘡(ocular cicatricial
pemphigoid, OCP)。
三、濕潤度下降型乾眼症
為膜相關黏蛋白或上皮細胞層成分不足所導致,其代表性和相關性疾病為縮短淚膜破裂時間(S-BUT)型乾眼症和維生素A缺乏症2。2020年亞洲乾眼症學會(ADES)更進一步提出以淚膜逐層(layer-by-layer)診斷與治療之新概念,分別為淚膜導向診斷(tear-film
oriented diagnosis, TFOD)和淚膜導向治療(tear-film
oriented therapy, TFOT),為乾眼症治療提供新里程碑。
貳、淚膜導向診斷(TFOD)
淚膜導向診斷(TFOD)藉由觀察淚膜的動態變化用以鑑別診斷乾眼症類型,臨床上常使用淚膜螢光破裂模式(Fluorescein
breakup patterns),來測量淚膜穩定性3。根據淚膜各層之成分不足和具不同病理生理機制,在病人一次完整瞬目到淚膜出現第一個乾燥斑/黑點的型態與模式,將螢光破裂模式分為五種基本模式,並各自對應到三種乾眼症亞型。
一、蒸發過強型乾眼症
表現為隨機破裂(Random break, RB)模式。RB為不規則和不確定的破裂形狀,其典型的淚膜破裂發生位置通常因個案和每次眨眼而異,且必須發生在螢光向上移動(upward
movement of fluorescein, UMF)停止之後。
二、缺水型乾眼症
表現為區域破裂(Area break, AB)和線性破裂(Line break,
LB)模式。AB於角膜下方區域未觀察到或有限觀察到UMF,其與嚴重的缺水型乾眼症有關。LB於角膜下方區域,UMF過程中的呈垂直線性破裂,其與輕度至中度的缺水型乾眼症有關。
三、濕潤度下降型乾眼症
表現為點狀破裂(Spot break, SB)模式和波紋破裂(Dimple break,
DB)模式。SB為睜眼後,淚膜立即出現點狀破裂,且至少有一個SB於UMF期間沒有被擦去。DB於角膜中央區域,UMF過程中呈不規則但垂直線狀破裂4。除了淚膜螢光破裂模式,其他的檢查和診斷方式也包含淚液分泌檢查(Schirmer
1 test)、瞼板腺功能評估和脂質層評估…等。
參、淚膜導向治療(TFOT)
淚膜導向治療(TFOT)針對淚膜層和上皮組織各層成分異常情形給予相對應的治療方法2。(圖一)
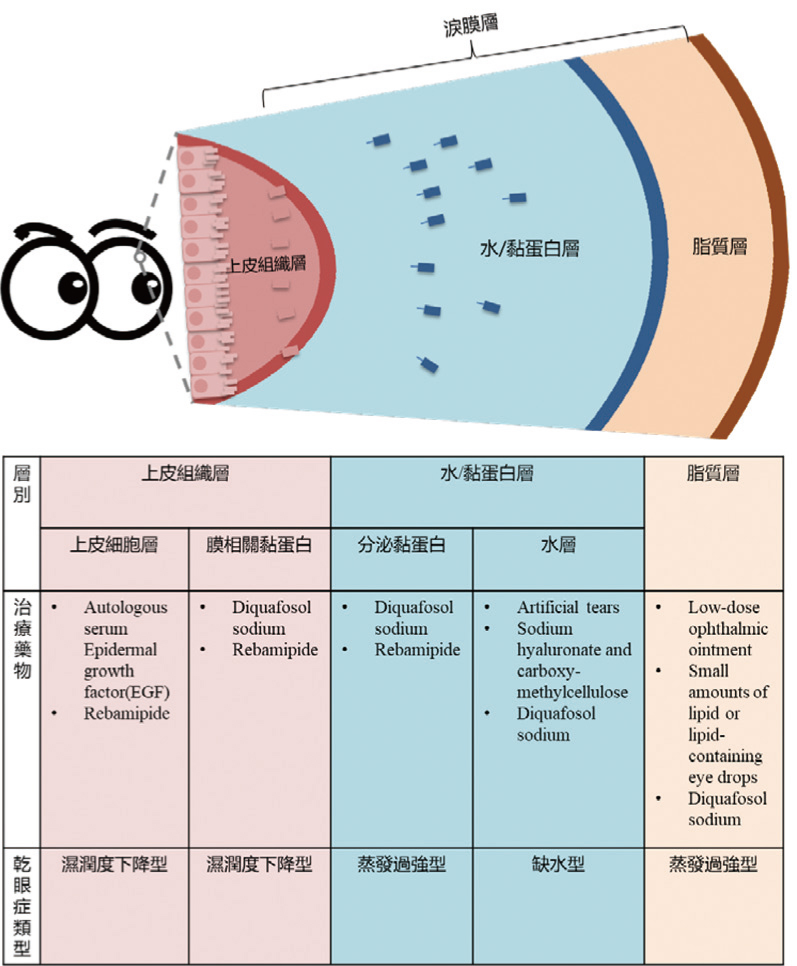
圖一 淚膜導向治療(TFOT)與乾眼症分類
一、脂質層成分不足所導致的蒸發過強型乾眼症
建議可使用眼瞼清潔為治療首選、低劑量眼藥膏、少量脂質或含脂眼藥水、Diquafosol
sodium、熱敷、增加室內溼度、護目鏡和保濕眼鏡治療和減緩乾眼症症狀;而分泌黏蛋白層成分不足所導致的蒸發過強型乾眼症,建議使用Diquafosol
sodium和Rebamipide以促進分泌黏蛋白分泌。
二、水層成分不足所導致的缺水型乾眼症
建議使用人工淚液作為初始治療之首選、玻尿酸和羧甲基纖維素(carboxymethylcellulose,
CMC)等帶負電的高分子聚合物可將水分保留於水層中、Diquafosol
sodium促進水分分泌,若需更快速達到療效時,淚管栓塞為治療的首選,用以減少淚水的流失和維持淚膜層穩定性。
三、膜相關黏蛋白成分不足所導致的濕潤度下降型乾眼症
建議使用Diquafosol sodium和Rebamipide以促進膜相關黏蛋白分泌;而上皮細胞層成分不足所導致的濕潤度下降型乾眼症,建議使用自體血清(autologous
serum)眼藥水、表皮生長因子(epidermal growth factor, EGF)和Rebamipide治療。
肆、淚膜導向治療(TFOT)之藥品介紹
一、人工淚液
人工淚液為常見的第一線乾眼症治療,直接性提供淚膜保濕,內含成分除水外,其他常見成分包含高分子聚合物增稠劑(如羥丙甲纖維素HPMC、羧甲基纖維素CMC、聚乙二醇PEG
400),電解質、滲透壓調節劑(如甘油、赤蘚糖醇、海藻糖等)、脂類與介面活性劑、促進內皮修護與抗發炎成分物質(如陽離子乳液、高分子量玻尿酸)等5,其中增稠劑可用以延長人工淚液在眼球表面的停留時間,電解質與滲透壓調節劑為調節滲透壓之用,避免細胞因高滲透壓導致角結膜細胞凋亡,而脂類與介面活性劑則可穩定淚膜脂層,若為脂質層不足導致蒸發過強者即可選用含脂類成分的人工淚液,如優麗舒加強型眼用乳劑、凱舒諾人工淚液;此外,瓶裝式人工淚液多會額外添加防腐劑,單支包裝者較不會添加,建議需長期使用人工淚液或有配戴隱形需求者,使用前可先與醫師討論選用合適劑型。臨床研究證據顯示,隨機分派臨床試驗中,人工淚液可顯著改善眼表疾病分數(Ocular
surface disease index, ODSI),並顯著增加淚膜破裂時間(TBUT),治療乾眼症效果佳6,然而回歸現實生活,用藥配合度為影響藥品療效的重要因素,觀察性研究指出有高達6成左右病人僅於眼睛不適時才用藥,建議病人遵照醫囑指示用藥,以達到最佳治療效果7。
二、Diquafosol sodium
Diquafosol為P2Y2受體促進劑,作用在眼球表面(ocular
surface)之結膜上皮與杯狀細胞膜上P2Y2受體,藉提升細胞內鈣離子濃度,以促進眼球表面液體與黏蛋白的分泌,作用機轉較不涉及淚腺與淚液的分泌,目前市售藥品採用3%
Diquafosol,建議每日使用六次8。第三期多中心、雙盲、隨機對照臨床試驗,比較3%
Diquafosol及0.1%純化玻尿酸眼藥水,使用四週後Diquafosol組改善角膜螢光染色分數(Corneal
fluorescein staining, CFS)(為一評估角結膜上皮受損之指標)之療效不亞於玻尿酸眼藥水組,且更較玻尿酸眼藥水組顯著下降Rose
bengal staining分數(為一評估角結膜上皮受損之指標) 9。長期使用之療效與安全性而言,前瞻性觀察性研究追蹤使用者至少12個月,可持續顯著降低CFS及增加淚膜破裂時間(tear
film break-up time, TBUT),且無嚴重藥物不良反應10。
三、 Rebamipide及表皮生長因子(epidermal growth factor,
EGF)
Rebamipide可透過向上調節角膜內皮細胞黏液蛋白(MUC16)生合成,加速細胞間緊密連接(tight
junction)、微絨毛(microvilli)復原,與增加杯狀細胞(goblet
cell)等機制,以達到活化角膜內皮細胞分化與促進黏液蛋白分泌等效果11。第三期多中心、雙盲、隨機對照臨床試驗,比較2%
Rebamipide及0.1%純化玻尿酸眼藥水,使用四周後Rebamipide組改善CFS療效不亞於玻尿酸,而改善病人主觀眼睛疼痛與異物感感受,Rebamipide則顯著優於玻尿酸。可改善角膜螢光染色分數(CFS),此外亦可降低病人主觀眼睛乾澀、異物感、畏光等症狀嚴重程度,安全性方面,較常見之不良反應僅輕度苦味味覺障礙及眼部搔癢12。目前台灣尚未核准此藥品。
四、自體血清(autologous serum)眼藥水
自體血清點眼液為客製化血液製劑,點眼液的組成與淚腺分泌之淚液相似,富含豐富的表皮生長因子、維生素A、纖維蛋白、電解質等,製備方法先抽取病人本身的血液,經離心後留下血清,加入等張鹽類稀釋液,稀釋至濃度20-100%,目前臨床文獻中尚無一致的標準化的製備流程。綜述文章收錄多篇自體血清用於嚴重乾眼症及角膜內皮受損族群之小規模試驗及觀察性研究,結果顯示嚴重乾眼症者使用後可增加淚膜破裂時間(TBUT),而角膜內皮受損病人治療後亦可加速內皮癒合程度,然而目前尚待大型臨床試驗證實其療效,安全性而言,因自體血清點眼液製備過程無額外添加防腐劑,需考量微生物汙染等問題,用藥前需特別注意病人使用方式與保存方法13。
伍、附加治療
抗發炎反應(Anti-inflammatory)於乾眼症治療中,扮演重要角色。淚膜之不穩定性會增加眼瞼和眼球間之摩擦力,進而導致眼睛上皮受損和引起發炎反應2。T細胞(T-cells)於乾眼症初期會顯著被活化,免疫抑制劑Cyclosporine可藉由干擾介白素2(interleukin
2, IL-2)和干擾素γ(Interferon-γ, IFN-γ)之釋放,抑制T細胞活化與生長,而有效改善淚膜穩定性、淚液分泌和乾眼症症狀。類固醇(Steroid)可藉由抑制環氧化酶(Cyclooxygenase,
COX),以降低前列腺素之合成和達抗發炎作用。臨床上常短期使用類固醇於乾眼症治療,因長期使用可能反而會造成眼壓升高、增加白內障和感染之風險。根據文獻研究類固醇可改善乾眼症症狀和略微增加淚膜破裂時間(TBUT)
14。此外,5% Lifitegrast於2016年美國食品藥物管理署(FDA)核准上市用於乾眼症治療,Lifitegrast為第一型淋巴球功能相關抗原拮抗劑,可阻斷細胞間黏附因子1
(intercellular adhesion molecule 1,
ICAM-1)與淋巴細胞功能相關抗原1 (lymphocyte
function-associated antigen 1,
LFA-1)之結合,進而影響T細胞遷移和活化。根據Phase 3研究(OPUS-1,
OPUS-2 and OPUS-3),給予Lifitegrast可改善乾眼症症狀和角膜螢光染色分數15,以提供乾眼症治療之新選擇。
陸、結論
淚膜導向診斷(TFOD)與淚膜導向治療(TFOT),為亞洲乾眼症治療的新概念,提倡以淚膜的動態變化鑑別乾眼症類型:脂質層成分不足所導致的蒸發過強型乾眼症、水層成分不足所導致的缺水型乾眼症及膜相關黏蛋白成分不足所導致的蒸發過強型乾眼症,分別投與精準的藥物治療。人工淚液的選用上可考量其內含成分與是否添加防腐劑,挑選合適的藥物劑型、而客製化自體血清點眼液因尚無標準化製備流程,建議至較有經驗的醫療院所開立,並注意點眼液的保存,另外還有3%
Diquafosol與抗發炎治療等安全、有效的治療選擇,此些藥品的發展為乾眼症治療提供新治療里程碑。
Precise Treatment
of Dry Eye Guided by Tear Film Orientation
Wun-Syuan Chen, Ya-Ting Cheng, Wei-Hsuan Huang,
Teng-Hsiang Pang, Hui-Chuan Hsiao
Pharmacy, Kaohsiung Municipal Ta-Tung Hospital
Abstract
Dry eye is a multifactorial disease
characterized by unstable tear film leading to
visual impairment and ocular surface damage.
Insufficient components or dysfunction of the
tear film layer and epithelial tissue layer on
the ocular surface can affect tear film
stability. Therefore, in recent years, the Asian
Dry Eye Society has proposed a new concept for
the diagnosis and treatment of dry eye called
tear-film oriented diagnosis (TFOD) and
tear-film oriented therapy (TFOT). Dry eye is
further classified into three types based on
tear-film oriented diagnosis: increased
evaporation type, aqueous-deficient type and
decreased wettability type, corresponding to the
deficiencies or abnormalities of the lipid laye/mucin,
aqueous layer and membrane-associated mucin/epithelial
cell layer, respectively. Tear-film oriented
therapy aims to provide corresponding treatment
for the abnormal components of each layer to
reconstruct the stable tear film structure and
function. For increased evaporation type dry
eye, lipid-containing eye drops, Diquafosol
sodium and Rebamipide are recommended. For
aqueous-deficient type dry eye, artificial
tears, hyaluronic acid and Diquafosol sodium are
recommended. For decreased wettability type dry
eye, Diquafosol sodium, Rebamipide, epidermal
growth factor (EGF) and autologous serum eye
drops are recommended. Tear-film oriented
diagnosis and treatment provide a more precise
treatment strategy for dry eye in the future.
參考資料:
1. Kazuo Tsubota, Norihiko Yokoi, Jun Shimazaki,
et al: New Perspectives on Dry Eye Definition
and Diagnosis: A Consensus Report by the Asia
Dry Eye Society. Ocul Surf. 2017
Jan;15(1):65-76.
2. Kazuo Tsubota, Norihiko Yokoi, Hitoshi
Watanabe, et al: A New Perspective on Dry Eye
Classification: Proposal by the Asia Dry Eye
Society. Eye Contact Lens. 2020 Jan;46 Suppl
1(1):S2-S13.
3. Norihiko Yokoi, Georgi As Georgiev, et al:
Tear Film–Oriented Diagnosis and Tear
Film–Oriented Therapy for Dry Eye Based on Tear
Film Dynamics. Invest Ophthalmol Vis Sci. 2018
Nov 1;59(14):DES13-DES22.
4. Kazuo Tsubota, Stephen C Pflugfelder, Zuguo
Liu, et al: Defining Dry Eye from a Clinical
Perspective. Int J Mol Sci. 2020 Dec
4;21(23):9271.
5. Labetoulle M, Benitez-Del-Castillo JM,
Barabino S, Herrero Vanrell R, et al:.
Artificial Tears: Biological Role of Their
Ingredients in the Management of Dry Eye
Disease. Int J Mol Sci. 2022 Feb 23;23(5):2434.
6. Aragona P, Benítez-Del-Castillo JM, Coroneo
MT, et al: Safety and Efficacy of a
Preservative-Free Artificial Tear Containing
Carboxymethylcellulose and Hyaluronic Acid for
Dry Eye Disease: A Randomized, Controlled,
Multicenter 3-Month Study. Clin Ophthalmol. 2020
Oct 1;14:2951-2963.
7. Uchino M, Yokoi N, Shimazaki J, Hori Y,
Tsubota K, et al: Adherence to Eye Drops Usage
in Dry Eye Patients and Reasons for
Non-Compliance: A Web-Based Survey. Journal of
Clinical Medicine. 2022; 11(2):367.
8. Keating GM. Diquafosol ophthalmic solution 3
%: a review of its use in dry eye. Drugs. 2015
May;75(8):911-22. doi:
10.1007/s40265-015-0409-7.
9. Takamura E, Tsubota K, Watanabe H, et al:
Diquafosol Ophthalmic Solution Phase 3 Study
Group. A randomised, double-masked comparison
study of diquafosol versus sodium hyaluronate
ophthalmic solutions in dry eye patients. Br J
Ophthalmol. 2012 Oct;96(10):1310-5.
10. Ohashi Y, Munesue M, Shimazaki J, et al:
Long-Term Safety and Effectiveness of Diquafosol
for the Treatment of Dry Eye in a Real-World
Setting: A Prospective Observational Study. Adv
Ther. 2020 Feb;37(2):707-717.
11. Hitoshi Watanabe; Medical Treatment for Dry
Eye in Japan. Invest. Ophthalmol. Vis. Sci.
2018;59(14):DES116-DES120.
12. Kinoshita S, Oshiden K, Awamura et al;
Rebamipide Ophthalmic Suspension Phase 3 Study
Group. A randomized, multicenter phase 3 study
comparing 2% rebamipide (OPC-12759) with 0.1%
sodium hyaluronate in the treatment of dry eye.
Ophthalmology. 2013 Jun;120(6):1158-65.
13. Shtein RM, Shen JF, Kuo AN,et al: Autologous
Serum-Based Eye Drops for Treatment of Ocular
Surface Disease: A Report by the American
Academy of Ophthalmology. Ophthalmology. 2020
Jan;127(1):128-133.
14. Su-Hsun Liu, Ian J Saldanha, Alison G
Abraham, et al: Topical corticosteroids for dry
eye. Cochrane Database Syst Rev. 2022 Oct
21;10(10):CD015070.
15. Gillian M Keating. Lifitegrast Ophthalmic
Solution 5%: A Review in Dry Eye Disease. Drugs.
2017 Feb;77(2):201-208.
通訊作者:蕭惠娟/電子信箱:h930103@gmail.com

