對晚期EGFR突變肺癌腦膜轉移案例之化療藥物臨床處置
方暉、邵暐超、張玉慧
國立臺灣大學醫學院附設醫院新竹臺大分院生醫醫院藥劑部
摘要
本文探討本院表皮生長因子受體基因突變 (EGFR mutation) 肺癌病人,發生腦膜轉移(leptomeningeal
metastases, LM) 後,脊髓鞘內 (intrathecal, IT) 注射化療藥物methotrexate和pemetrexed對LM的臨床療效和耐受性。近期臨床研究文獻證實IT注射化療藥物methotrexate和pemetrexed對於非小細胞肺癌
(NSCLC) 發生腦膜轉移的成效,限於缺乏相關隨機對照試驗文獻,本文探討EGFR突變NSCLC-LM病人接受脊髓鞘內給藥後的住院天數、存活期和預後分析等,以作成臨床建議及病人照護的參考。結果發現methotrexate
10mg、pemetrexed 25mg與pemetrexed
50mg,經IT治療後,病人頭痛改善並恢復意識,有助於改善生活品質。
關鍵字: 表皮生長因子受體基因突變、腦膜轉移、脊髓鞘內給藥
壹、前言
EGFR突變肺癌腦膜轉移的病徵為癌細胞經由血液或淋巴播散,進而阻礙CSF流動並導致腦積水或顱內壓升高,這是晚期癌症中嚴重的併發症,病人預後不佳將會導致臨床症狀惡化及危害性命,其中以EGFR突變NSCLC-LM發病率居高1,2。以往治療NSCLC-LM,不外乎EGFR-TKIs(酪氨酸激酶抑制劑,tyrosine
kinase inhibitors,TKIs)、全身性化療 (docetaxel,
paclitaxel, carboplatin, pemetrexed, bevacizumab)
、免疫治療等3。由於口服或靜脈注射化療藥物對NSCLC發生LM的療效有限,且缺乏系統性治療的隨機對照試驗
(randomized controlled trial, RCT)
,目前尚無最佳治療方案。根據哈佛醫學院2018年指出LM發病率因腫瘤類型而異,肺癌、黑色素瘤、轉移性乳腺癌則分別是9~25%、6~18%、5~8%
4。60~70%
的LM病人有全身性症狀,如噁心和嘔吐、吞嚥困難、精神變化、步態困難、顱神經麻痺伴有複視、聽力損失、頸部和背部疼痛、無法站立與尿失禁等疑似馬尾症候群
(cauda equina syndrome, CES)等2。最新文獻顯示IT投予化療藥是治療實體瘤的最佳方式之一,本文報導2位EGFR突變型NSCLC-LM個案的臨床特徵並評估IT注射化療藥物methotrexate和pemetrexed的治療結果。
貳、案例報告
個案分別於2020/12/13、2022/03/01皆因步態不穩、虛弱無力、眩暈、噁心和嘔吐、頭痛與意識變化等入本院急診。疑似有LM特徵,如:個案1情緒躁動,推測因為腦膜轉移造成顱內壓上升
(open pressure 26 cmH2O (20 mmHg)) ,先由腰椎穿刺
(lumbar puncture, LP) 引流腦脊髓液12 mL緩解;個案2出現無法站立與尿失禁等疑似馬尾症候群。兩案例的核磁共振影像學
(magnetic resonance imaging, MRI) 報告均顯示leptomeningeal
seeding,推測罹患腦膜轉移。兩位案例自NSCLC肺癌治療中進展到LM的時間,分別是35個月與30個月。數據收集包括神經理學檢查、評估診斷LM、評估腦脊髓液細胞學病理報告、癌胚原抗原指數
(carcinoembryonic antigen, CEA) 、甲狀腺轉錄因子第一型
(thyroid transcription factor-1, TTF-1) 、診斷LM前的EGFR基因突變NSCLC標靶治療、核子放射醫學影像、LM治療方式、住院天數、身體評估等,相關臨床檢測與神經理學評估項目詳見表1~2。接續鑑別腦膜轉移的模式,依據美國東岸癌症臨床研究合作組織
(Eastern Cooperative Oncology Group, ECOG)
評估個案發生LM時的體能狀態 (performance status, PS)
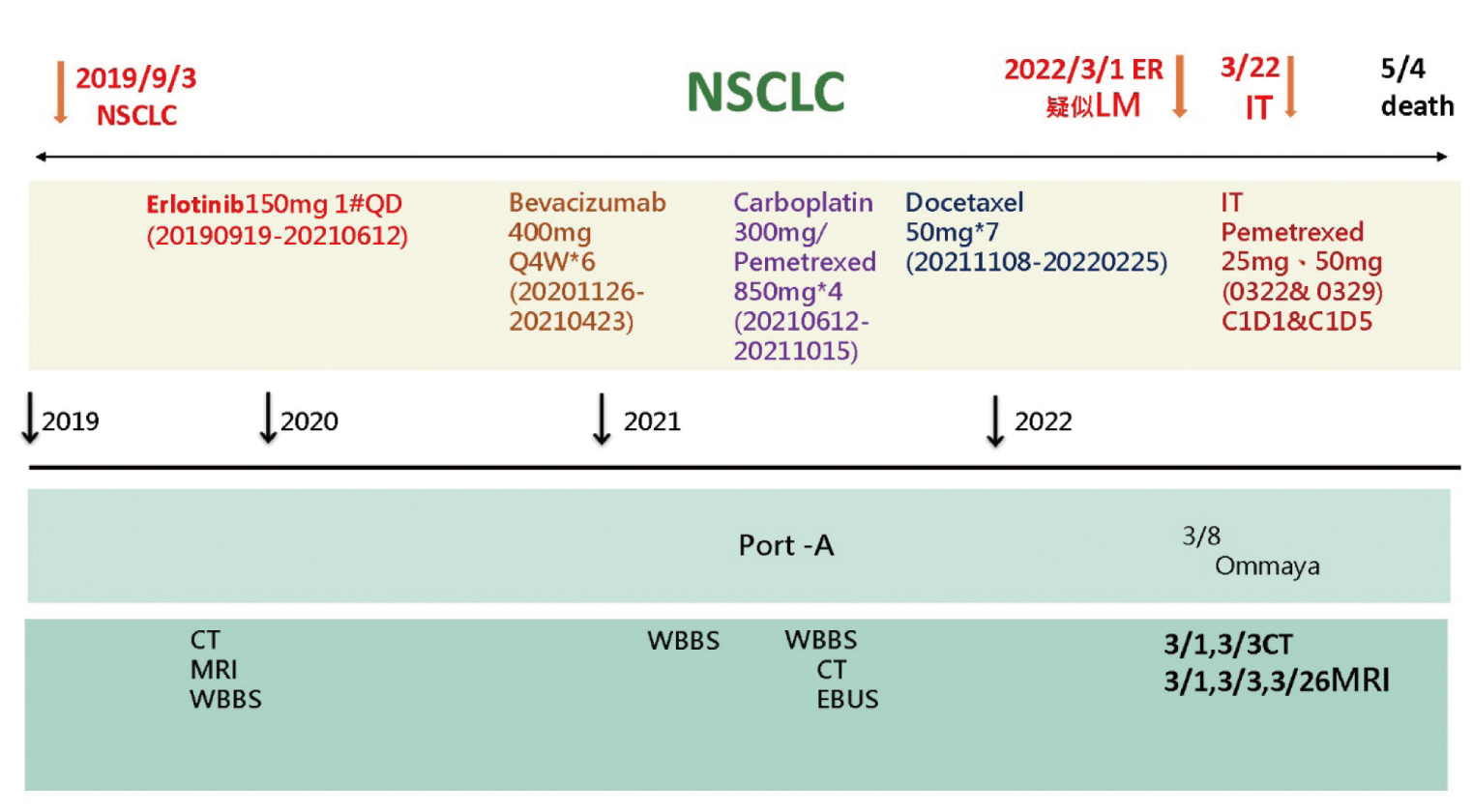
評分,均是2分,表3,腦脊髓液相關生化值與藥物治療見表4~6。診斷LM前,案例均接受表皮生長因子基因受體抑制劑、血管內皮生長因子受體抑制劑與全身性化療等治療,藥歷等相關治療詳見圖1、圖2。住院期間均接受2次IT給藥治療,住院天數分別是23天與35天;存活期分別是23天與44天。首先評估腦脊髓液相關生化值由
(+) 轉為 (-)
,再進行護理評估功能中的身體神經系統評估與危險跌倒性評估,評估項目包括了意識與認知、知覺、運動與活動、體能狀態等。評估結果發現個案1經IT治療後,其頭痛、平衡與步態不穩、認知與知覺有所改善、意識由躁動恢復至正常等;個案2則是記憶力與時間地點認知不佳、平衡與步態不穩,經IT治療後有所改善,且意識由混淆恢復至正常等,其治療結果詳見表2。個案1於注射methotrexate時,發生Grade
I嘔吐與Grade
I疲勞,經休息後緩解疲憊;個案2於2022/04/11~2022/04/21期間,其血小板數值低達26~65
K/μL (正常值150~378) ,推測係pemetrexed誘發Grade
3/4血小板低下(thrombocytopenia) 。
表1 疑似發生腦膜轉移的臨床檢測
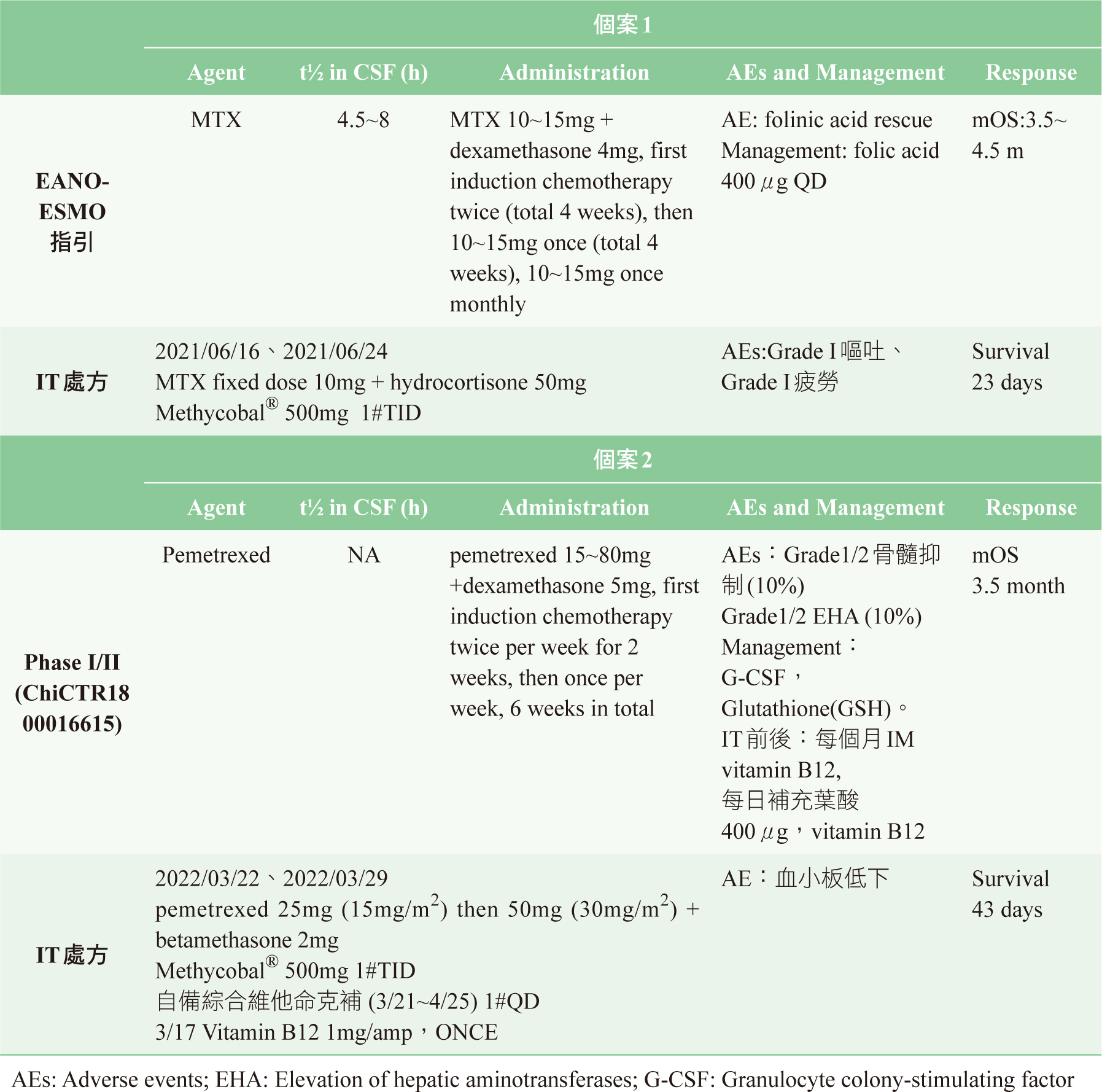
表5 腦膜轉移的藥物治療
圖1 個案1藥歷與相關治療
LM病人的預後不佳,若接受治療,從診斷時起的總存活期約為2至4個月。未經治療,在4至6週內可能因神經功能惡化而死亡。綜觀相關治療的療效、副作用等,分述如下:
一、第三代EGFR-TKI5
osimertinib的中位數無惡化存活期 (progression free
survival, PFS) 為8至11個月。個案1疑似發生LM後,首選osimertinib
160mg治療6個月,約7個月後惡化。
二、 高劑量脊髓鞘內methotrexate治療6
methotrexate
10~15mg療程是4週,每週頻率1至2次,每次劑量10~15mg,持續4週誘導性治療,最後每月注射1次維持性治療。Raquel
Olmos-Jiménez等人研究顯示methotrexate在CSF中不易排除,其起始排除半衰期
(t½) 為4.5小時,最終排除半衰期 (t½) 為14小時,藥效約可以維持4天。由於methotrexate會代謝成為methotrexate
polyglutamate,進而蓄積於CSF而導致副作用,如黏膜發炎、嘔吐、頭痛、頸部僵硬等,大多數病人在3~4週內可緩解。個案1於治療期間僅出現Grade
I嘔吐、Grade
I疲勞等現象。鑒於此副作用發生機轉,建議可於治療前後,每日補充葉酸400μg。
三、 高劑量脊髓鞘內pemetrexed治療7,8
pemetrexed為新一代抑制多重標靶酵素的葉酸拮抗劑,比MTX有更佳的耐受性,經IT給藥的療效大於注射給藥。劑量
10~50mg療程6週,前兩週是每週頻率2次,後4週則是每週1次。DiGeng等人的研究顯示,15~30
mg高劑量pemetrexed的IT療效佳,LM的中位存活期 (median overall
survival, mOS)
20個月。給藥頻率是每週2次或每月2~4次,劑量依據LM臨床表現與相關症狀緩解程度而調整。常見的副作用有Grade
1/2骨髓抑制 (10%) 、Grade 1/2 肝臟轉胺酶昇高 (elevation of
hepatic aminotransferases, EHA) (10%)、神經根炎 (radiculitis)
、血小板低下等,可皮下注射白血球生長激素 (G-CSF) 與麩胱甘肽 (glutathione)
予以預防或緩解。個案2於IT前注射vitamin B12,IT後補充Methycobal®
(mecobalamin)500mg 1#TID及自備綜合維他命克補
(3/21~4/25,含葉酸400μg) ,但治療期間發生Grade
3/4血小板低下,推測是提高pemetrexed劑量至50mg而導致副作用發生。
四、類固醇
目前尚未有IT化療藥物與類固醇併用的人體CSF試驗報告。類固醇可以減少IT化療後引起的腦膜刺激和神經疼痛,CALGB-8811等研究提到類固醇methylprednisolone、dexamethasone、hydrocortisone、prednisolone等均可以降低腦脊髓腔腫瘤細胞發炎反應,提高IT治療有效性與止吐作用等,其藥物選擇與劑量尚無標準依據。研究發現dexamethasone半衰期長,與血漿蛋白的結合較低,具有較高的CSF滲透性,電解質失衡風險低等特性6。
肆、結論
鑑於本次收案樣本數量少,推測人種、族群、基因、年齡大於50歲、ECOG
PS均2分、肺癌原發性腫瘤是預後與存活不良等因素,導致存活期為23天和44天,遠低於文獻資料。考量目前台灣尚未有系統性相關研究分析,希望未來持續評估LM病人以IT合併全身性化療的療效與安全性,前瞻性探索IT最佳介入治療的時間與劑量、給藥頻率或IT療程。期盼未來技術可以改善LM的診斷與治療,達到改善病人生活品質並延長存活期。
附錄 專有名詞縮寫
A Case Study of
Intrathecal Chemotherapy for Leptomeningeal
Metastases of Lung Cancer
Hui Fang, Wei-Chao Shao, Yu-Huey Chang
Department of Pharmacy, National Taiwan
University BioMedical Park Hospital
Abstract
Two cases were conducted on the clinical
efficacy and tolerance of chemotherapy drugs
methotrexate and pemetrexed on leptomeningeal
metastases (LM) through intrathecal (IT)
administration following the occurrence of LM in
a lung cancer patient with Epidermal Growth
Factor Receptor (EGFR) mutation at this
hospital. Recent clinical research literature
has confirmed the effectiveness and tolerance of
the IT administration of chemotherapy drugs
methotrexate and pemetrexed against the
occurrence of leptomeningeal metastasis in
non-small cell lung cancer (NSCLC). Limited by
the lack of relevant literature on randomized
controlled trials, this paper explored inpatient
admission days, survival, prognosis analysis,
etc., after NSCLC-LM patients with EGFR mutation
received IT administration, which served as
clinical recommendations and references for
patient care. Results show that, after IT
treatment with 10mg of methotrexate, 25mg of
pemetrexed, and 50mg of pemetrexed, the patient
showed improvement in headaches and regained
consciousness, which helped in improving
patient's quality of life.
參考資料:
1. Choi M, Keam B, Ock CY, et al: Pemetrexed in
the treatment of leptomeningeal metastasis in
patients with EGFR-mutant lung cancer. Clin Lung
Cancer 2019;20(4):442-51.
2. Le Rhun E, Guckenberger M, Smits M Le Rhun,
et al: EANO-ESMO Clinical Practice Guidelines
for diagnosis, treatment and follow-up of
patients with leptomeningeal metastasis from
solid tumours. Ann Oncol 2017;8(Suppl 4):84-99.
3. Nayar G, Ejikeme T, Chongsathidkiet P, et al:
Leptomeningeal disease: current diagnostic and
therapeutic strategies. Oncotarget
2017;8(42):73312-28.
4. Wang N, Bertalan MS, Brastianos PK:
Leptomeningeal Metastasis From Systemic Cancer:
Review and Update on Management. Cancer
2018;124(1):21-35.
5. Pellerino A, Internò V, Muscolino E, et al:
Leptomeningeal metastases from non-small cell
lung cancer: state of the art and recent
advances. J Cancer Metastasis Treat
2020;6(1):41-60.
6. Olmos-Jiménez R, Espuny-Miró A,
Cárceles-Rodríguez C, et al: Practical aspects
of the use of intrathecal chemotherapy. Farm
Hosp. 2017;41(1):105-29.
7. Geng D, Guo Q, Huang S, et al: A
Retrospective study of intrathecal pemetrexed
combined with systemic therapy for
leptomeningeal metastasis of lung cancer.
Technol Cancer Res Treat 2022;21(1):1-9.
8. Fan C, Zhao Q, Li L, et al: Efficacy and
Safety of Intrathecal Pemetrexed Combined With
Dexamethasone for Treating Tyrosine Kinase
Inhibitor-Failed Leptomeningeal Metastases From
EGFR-Mutant NSCLC-A Prospective, Open-Label,
Single-Arm Phase 1/2 Clinical Trial (Unique
Identifier: ChiCTR1800016615). J Thorac Oncol
2021;16(8):1359-68.
通訊作者:張玉慧/電子信箱:fangsmallhui@gmail.com