淺談軟組織肉瘤的治療新選擇—Trabectedin
郭文蓉1、畢淑娟1、項怡平2
1義大醫療財團法人義大癌治療醫院藥劑科、2義大醫療財團法人義大醫院藥劑部
摘要
平滑肌肉瘤 (leiomyosarcomas, LMS) 和脂肪肉瘤 (liposarcomas,
LPS) 是繼胃腸道間質瘤 (gastrointestinal stromal tumors,
GIST) 之後,軟組織肉瘤 (soft tissue sarcomas, STS)
中最常見的亞型,是一種固態腫瘤。可以從多種不同的組織發展而來,脂肪、神經、血管、骨骼、肌肉和深層皮膚是最常見的起源部位。對於表淺性、中低惡性度的STS,建議用手術切除,或再合併放射治療或化療有良好成效。晚期或轉移性肉瘤的患者預後較差,估計中位存活期
(median survival)
約12至15個月,所以治療目標是延遲疾病進展、延長生命跟提升生活品質。Trabectedin是一種烷基化藥物,也為晚期軟組織肉瘤
(advanced soft tissue sarcomas, ASTS)患者帶來治療新選擇。
關鍵字:
平滑肌肉瘤、脂肪肉瘤、軟組織肉瘤、anthracycline、trabectedin、dacarbazine
壹、前言
STS是一種來自於結締組織很罕見的惡性腫瘤,除了GIST,LMS和LPS是最常見的STS,共佔約所有固態腫瘤的1%1,然而卻佔兒童惡性腫瘤的7~10%。絕大多數的發生原因不明,但隨著年齡增加,發展成STS的危險因子也增加,通常好發於50歲以上成年人,好發部位遍及全身,常見於四肢(50%)、腹膜後腔(40%),或頭頸部(10%)。STS通常在沒有疼痛的情況下發展,從症狀開始到確定診斷平均延遲6~12個月,因此初期不易被診斷,此時常容易誤診為囊腫、良性腫瘤、瘀青、或膿瘡,如果進一步壓迫到鄰近的神經或血管,則會導致神經麻痺、淋巴水腫、靜脈瘀血。隨著疾病進展,腫瘤會於皮下組織持續增大或深入到肌肉內以三度空間方式散佈,但是最大的微量擴散
(greatest microscopic extension) 似乎是沿著筋膜平面 (fascial
plane)
發生。轉移到區域淋巴結的相當少見,主要轉移位置是在肺臟,另外也有轉移到肝臟和其他軟組織位置及中樞神經系統的報告2。依腫瘤分期,五年無惡化存活期
(progression free survival)
為51.77~86.13%2。治療預後取決於包括患者的年齡和腫瘤大小、深度、組織學分級和分期3。
貳、治療
一、一線藥物
目前STS的治療需評估其組織學、臨床分期及患者的體能狀況,主要治療包含有手術治療、放射治療與化學治療。手術治療是目前大部分STS的主要治療方式,但有些無法手術的患者就必須接受化學治療或可合併放射治療以控制病情。至今為止,doxorubicin或以doxorubicin為主的化學治療,是ASTS的主要標準治療藥物2。一般來說,合併藥物治療與單一doxorubicin治療比較,並沒有顯著改善OS,且毒性也較大4。其中對於無法切除的
STS 患者的初始化療最常見為anthracycline類 (doxorubicin) 或gemcitabine,其他如dacarbazine、ifosfamide也常使用。而在轉移性STS中,doxorubicin與ifosfamide合併會比單獨使用doxorubicin有更好的反應率
(response rate, RR) ,但會增加嚴重毒性產生,且對整體存活期 (overall
survival, OS) 沒有助益(分別為14.3個月及12.8個月HR=0.83,
P=0.076)5;另一篇研究中,合併gemcitabine與docetaxel會比單獨使用gemcitabine有更好的OS
(分別為17.9個月及11.5個月),但同時也會增加藥品毒性6。不過,各個STS類別對化學治療的敏感度不同,就LMS而言,胃腸道的LMS很少對化療有反應,子宮的LMS對anthracycline為主和ifosfamide的化療反應很好,而其他類型的LMS對anthracycline/
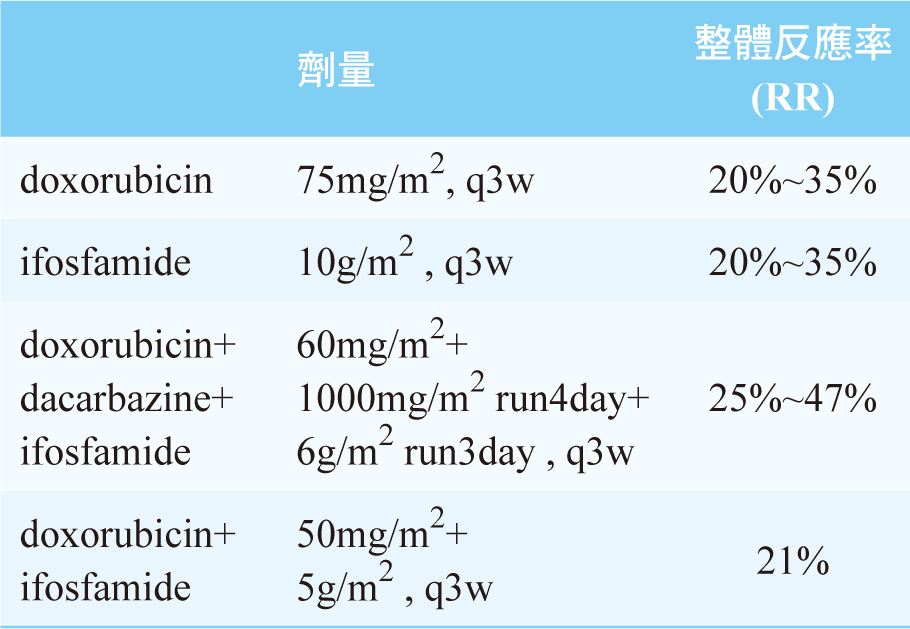
dacarbazine為主的化療反應很好2。有關傳統化學治療藥物劑量及反應率如表一。
表一 ASTS單一藥物與複方化學治療其治療劑量及整體反應率2
二、二線藥物
適用於一線藥物治療失敗或惡化的ASTS患者,如表二。
表二 用於一線藥物治療失敗或惡化的二線藥物2,7,8,9
參、Trabectedin用於ASTS
一、適應症
適用於治療患有無法切除或轉移性LPS或LMP,且曾接受一種含anthracycline療程的患者10。
二、機轉
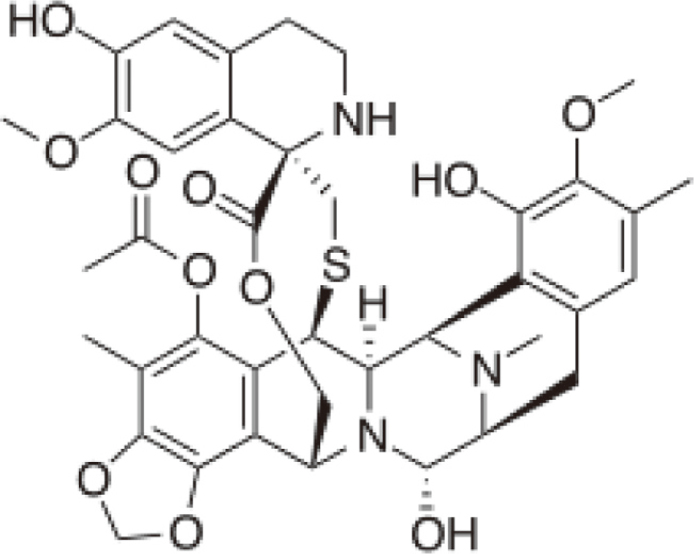
Trabectedin (Yondelis®)
於2007年在歐盟和許多國家核准使用,是為從加勒比海鞘 (Ecteinascidin
turbinate)
萃取出來的一種抗DNA烷化劑(圖一),與傳統烷化劑不同的是,它跟DNA小溝槽(minor
groove)內的鳥嘌呤殘基共價結合,使DNA螺旋彎向大溝槽(major
groove),干擾DNA轉錄作用,讓細胞週期停止在G2/M期,進而造成細胞凋亡,達到抗腫瘤作用,可抑制腫瘤生長、血管增生和腫瘤之轉移11,12。
Trabectedin建議劑量為1.5mg/m2每21天一次,但於亞洲人的建議劑量為1.2mg/m2,因亞洲人的曝藥量(曲線下面積)較高於西方人。配製方法為1mg/vial以20ml無菌注射用水溶解後加入500
ml
0.9%氯化鈉溶液或5%葡萄糖注射液,透過中央靜脈導管於24小時內輸注完畢。每次給藥前30分鐘,需靜脈注射dexamethasone
20
mg,其抗炎作用可降低肝毒性。針對不良反應(表三)建議劑量調整,第一次降低劑量至1.0mg/m2,第二次降低劑量至0.8mg/m2。一旦降低使用劑量,不應在後續治療週期再增加劑量10,13。如出現表四情況,應永久停用trabectedin。
表三 不良反應建議劑量調整10
表四 永久停用trabectedin10
四、藥物動力學
Trabectedin與人類血漿蛋白結合率約為97%,平均廓清率為31.5L/hr,半衰期約為175小時。將患者以3小時或24小時時間經C14標記的trabectedin靜脈輸注完畢後,在24天內收集到64%放射性總給藥劑量,其中58%於糞便中排除,6%於尿液中排除10。
五、不良反應
疲勞、噁心和嘔吐最為常見。最常見的grade
3/4血液學毒性是嗜中性白血球減少症,其次是血小板減少症和貧血,而常見的grade
3/4生化學毒性則為轉胺酶 (AST、ALT) 升高,其次是肌酸磷酸肌酶 (CPK)
升高。相對於其他軟組織肉瘤的治療藥物,發生黏膜炎和掉髮情況較低,也較沒有蓄積毒性而限制持續治療時間1,10,14。
六、交互作用
trabectedin主要經由肝臟CYP3A4代謝,建議謹慎與CYP3A4誘導劑或抑制劑的藥物同時並用。如臨床需要,可預防性使用止吐藥,但不建議與aprepitant/fosaprepitant同時給藥,因其為CYP3A4抑制劑。另外,在每次輸注trabectedin後最多
72 小時內不得使用降低肝血流量或可能影響其清除率的藥物13。
七、臨床試驗療效
在一項2011年5月至2013年9月執行的第三期臨床試驗中,518名受試患者(LMP378名,LPS140名),以2:1隨機分配方式接受每3週靜脈輸注trabectedin
(n = 345) 或dacarbazine (n = 173)
治療。在先前處置中,88%患者至少接受過兩次化療,超過90%患者曾接受過手術治療,50%患者曾接受過放療。trabectedin的治療中位週期數(四個週期)是dacarbazine(二個週期)的兩倍,而trabectedin持續接受治療至第六
(34% v 17%) 和第十二週期(10% v 2%)比例也較高。trabectedin
1.5mg/m2每3週一次24小時連續靜脈輸注與dacarbazine
1000mg/m2每3週靜脈輸注一次(20至120分鐘)比較,trabectedin能降低45%之疾病惡化或死亡風險
(HR=0.55, 95%CI 0.44-0.70, P<0.001),中位無惡化存活期
(median progression-free survival, mPFS)
分別為4.2個月與1.5個月。ORRs則分別為9.9%與6.9%。而OS在中期分析
(interim analysis) 時,其中位OS分別為12.4個月與12.9個月
(HR=0.87, P=0.37) 。仍在接受trabectedin (28%)
治療的患者比例約為dacarbazine (15%)
的兩倍。疾病惡化是終止研究治療的最常見原因,分別為55%與68%,因不良反應或死亡而終止治療的比例,分別為12.6%與7.7%1。而2015年1月OS在持續追蹤的結果中,trabectedin改善LPS和LMS的疾病控制,但仍沒有觀察到OS的顯著改善,最終中位OS
trabectedin為13.7個月、dacarbazine為13.1個月 (P
=0.49)15。
安全性方面,產生grade 3/4的血液學不良反應,以及AST、ALT上升,trabectedin和dacarbazine個別對於LMS的不良反應發生率和對LPS是差不多的。嗜中性白血球減少合併發燒在trabectedin發生率分別為LMS:4%、LPS:7%,dacarbazine則各為2%15。
綜觀結果,trabectedin在OS上雖無顯著改善,並未達到統計學上的意義,但接受治療的中位週期數比dacarbazine高(四個
v 二個週期) (≧六個週期:42% v 22%)15,使患者較能耐受長期的治療。
肆、結論
這些正在接受化療治療的STS患者中,近一半中高度惡性的STS會發生轉移,5年存活期只有約50%11。儘管採用常規的化學藥物治療,晚期或轉移性肉瘤患者的預後仍然很差,估計從一線藥物治療開始,其中位存活期約只有1年時間13。其多樣的特徵及複雜的組織分類,也使得在藥物治療的研究發展上較為困難。trabectedin是第二種海洋衍生藥物被核准用於治療癌症,如STS、乳癌、卵巢癌及其他類型的固態腫瘤,且FDA已於2015年核准用於治療ASTS,對於STS各類別都有觀察到廣泛的活性,其中以LPS和LMS的活性最大11。是現有標準治療失敗後,控制晚期肉瘤患者
(advanced sarcomas)
的新選擇14,然目前尚無健保給付,需自費且價格昂貴,期許未來健保可給付,也為患者帶來治療新契機。
A New Treatment for Soft Tissue Sarcomas-Trabectedin
Wen-Jung Kuo1, Shu-Chuan Pi1, Yi-Ping Hsiang2
1Department of Pharmacy, Department of Pharmacy,
E-Da Cancer Hospital
2Department of Pharmacy, Department of Pharmacy,
E-Da Hospital
Abstract
Soft tissue sarcomas (STSs) are a group of solid
tumors. Among all the STS histologies, the most
frequent is gastrointestinal stromal tumor,
followed by leiomyosarcoma and liposarcoma.
Sarcomas can develop from multiple different
tissues, with fat, nerves, vessels, bones,
muscle and deep skin tissues being the most
common site of origin. For superficial lesions,
low and moderate grade STS, surgical resection
or combined with radiotherapy or chemotherapy is
recommended, and has achieved good results. The
prognosis of patients with advanced or
metastatic STS remains poor, with an estimated
median survival of 12 to 15 months. The goal of
treatment is to delay progression, extend and
improve the quality of life. Trabectedin (an
alkylating agent) also brings new treatment
options for patients with advanced sarcomas.
參考資料:
1. George DD, Margaret VM, Robin LJ, et al:
Efficacy and safety of trabectedin or
dacarbazine for metastatic liposarcoma or
leiomyosarcoma after of conventional
chemotherapy: results of a phase III randomized
multicenter clinical trial, J Clin Oncol
2016;34(8):786-94. doi: 10.1200/JCO.2015.62.4734
2. 廖繼鼎:晚期軟組織肉瘤的化學治療,臨床腫瘤學初版二刷。臺北,合記圖書出版社,
2003:912-32。
3. Julian FG, Monica P, Erikas S, et al: Cost
effectiveness of first-line treatment with
doxorubicin/ifosfamide compared to trabectedin
monotherapy in the management of advanced soft
tissue sarcoma in Italy, Spain, and Sweden,
Sarcoma 2013;263-81.
4. Frédéric A, Domenica L, Alexander M, et al:
Management strategies in advanced uterine
leiomyosarcoma: focus on trabectedin, Sarcoma
2015;203-16.
5. Judson I, Verweij J, Gelderblom H, et al:
Doxorubicin alone versus intensified doxorubicin
plus ifosfamide for first-line treatment of
advanced ormetastatic soft-tissue sarcoma: a
randomized controlledphase III trial, Lancet
Oncol 2014;15:415-23.
6. Maki RG, Wathen JK, Patel SR, et al:
Randomized phase II study of gemcitabine and
docetaxel compared with gemcitabine alone in
patients with metastatic soft tissue sarcomas:
results of sarcoma alliance for research through
collaboration study 002 [corrected], J Clin
Oncol 2007;25:2755-63.
7. 廖繼鼎:晚期軟組織肉瘤的化學治療,臨床腫瘤實戰初版。臺北,合記圖書出版社,
2013:759-60。
8. Anastasios K, Michalis L, Ioannis NS, et al:
The systemic treatment of uterine
leiomyosarcomas, Medicine 2021;100(13):1-5.
doi:10.1097/MD.0000000000025309
9. Schoffski P, Chawla S, Maki RG, et al:
Eribulin versus dacarbazine in previously
treated patients with advanced liposarcoma or
leiomyosarcoma: a randomised, open-label,
multicentre, phase 3 trial, Lancet
2016;387:1629–37.
10. Yondelis®藥品仿單,版本:USPI Dec2018_v1901。
11. Csaba G, Anthony E: Trabectedin: safety and
efficacy in the treatment of advanced sarcoma,
Clinical Medicine Insights: Oncology
2011;5:35–43. doi:10.4137/CMO.S4907
12. 李耀泰、陳福民、郭宗正:Trabectedin在婦癌治療的應用。婦癌醫學期刊2021;53:6-10。
13. Samuels BL, Chawla S, Patel S, et al:
Clinical outcomes and safety with trabectedin
therapy in patients with advanced soft tissue
sarcomas following failure of prior
chemotherapy: results of a worldwide expanded
access program study, Ann Oncol 2013;24:1703-9.
doi:10.1093/annonc/mds659
14. George DD, Sant PC, Margaret VM, et al:
Efficacy and safety of trabectedin in patients
with advanced or metastatic liposarcoma or
leiomyosarcoma after failure of prior
anthracyclines and ifosfamide: results of a
randomized phase II study of two different
schedules, J Clin Oncol 2009;27(25):4188-96.
doi:10.1200/JCO.2008.21.0088
15. Shreyaskumar P, Margaret VM, Damon RR, et
al: Overall survival and histology-specific
subgroup analyses from a phase 3, randomized
controlled study of trabectedin or dacarbazine
in patients with advanced liposarcoma or
leiomyosarcoma, Cancer 2019;125:2610-20. doi:
10.1002/cncr.32117